Лечение хронического цистита
«Клиника АВС» действительно помогает вылечить хронический цистит и это хорошая новость для тех, кто живет с этой проблемой и не знает, как избавиться от нее. Хронизация процесса значительно снижает качество жизни, ограничивает человека во многом. Опытные специалисты клиники подберут грамотное лечение. Реабилитационные мероприятия ускорят выздоровление.
Крымкин Юрий Михайлович
Заведующий урологическим отделением, врач-уролог, хирург-андролог
Кармолиев Рустам Рафикович
Корнеева Лариса Николаевна
Врач-уролог высшей категории, кандидат медицинских наук
Этиология хронического цистита у женщин
Рецидивы болезни как раз проявляются обострениями, то есть возвратом всех симптомов. Отягощают анамнез при хроническом цистите венерические заболевания, воспаление почек, уретры. Кроме того, усугубляют состояние камни, дивертикулы и другие образования.
В климактерический период, а также во время беременности возникает гормональный дисбаланс. Он также влияет на проявлении заболевания.
Симптомы хронического цистита
Согласно статистике, в 3 случаях из 10 острый цистит переходит в хроническую форму. Воспалительный процесс затягивается до 2 месяцев. За это время поражается слизистая оболочка органа и ткани, расположенные под ней. Данные изменения приводят к деформации мочевого пузыря. Лечение хронического цистита трудно поддается терапевтическому воздействию.
Диагностические мероприятия
Способы лечения
После получения результатов проведенной диагностики, врач определяет, как лечить хронический цистит. Подбирается этиотропная терапия (то есть воздействующая непосредственно на возбудителя). Продолжительность лечения рассчитано на длительный срок (иногда до одного месяца). Антибиотикотерапии бывает недостаточно. Пациенту выписываются препараты, укрепляющие иммунитет, а также спазмолитики, средства растительного происхождения, которые подавляют жизнедеятельность бактерий. Закрепляется терапевтический эффект назначением нитрофуранов. Данной группой препаратов лечение может продолжаться до 6 месяцев. Все зависит от выраженности патологического процесса, в который вовлечены слои стенки пузыря.
Как лечить хронический цистит, если в анамнезе имеется заболевание, на фоне которого возникло воспаление мочевого пузыря? Параллельно с терапией проводится лечение основного заболевания. Например, если имеются камни, полипы, то от них избавляются хирургическим путем.
Ускоряет выздоровление физиотерапевтическое лечение. С помощью процедур удается улучшить местное кровообращение, обменные процессы, уменьшить боль, воспаление. «Клиника АВС» поможет диагностировать основную причину заболевания. Специалисты грамотно подберут схему лечения, которое поможет в дальнейшем предупредить обострения.
Препараты, назначаемые для лечения
Для лечения заболевания назначаются препараты разных групп.
Препараты назначаются при продолжительном воспалении. Терапевтический эффект проявляется, если употреблять их продолжительное время и непрерывно. Эффективность связана с низкой резистентностью бактерий.
Способствуют улучшению обменных процессов в тканях. Продолжительность лечения рассчитана на 10-14 дней. Представителем группы является «Солкосерил 200».
4. Нестероидные противовоспалительные средства.
Уменьшают боль, дискомфорт – то есть неприятные симптомы, которыми сопровождается заболевание. Длительное время их принимать не рекомендуется.
Вышеперечисленный список представлен для ознакомления, но не для самолечения. Чем лечить хронический цистит расскажет врач (нефролог, уролог, терапевт).
Диета при заболевании
Профилактика и прогноз
Своевременные профилактические мероприятия помогут предотвратить возникновение обострений. Как правило, они возникают осенью и весной. В это время необходимо обращаться за квалифицированной помощью, чтобы были назначены антибиотики, растительные диуретики.
Следует избегать переохлаждения, укреплять иммунитет и организм. Соблюдение режима дня, правил здорового образа жизни в этом помогут. По возможности проходить санаторно-курортное лечение.
Прогноз заболевания во многом зависит от тактики специалиста, а также от причины, провоцирующих факторов, которые привели к хронизации процесса. Важно помнить, что самолечение часто приводит к печальным последствиям, из-за которых все равно придется обратиться за помощью врача. Поэтому, лучше сделать это вовремя. Только правильно поставленный диагноз и своевременные мероприятия помогут вылечить цистит без последствий.
«Клиника АВС» приглашает на прием всех, кто имеет в анамнезе хронический цистит. Специалисты после диагностики, подберут грамотное лечение.
Лечение рецидивирующего цистита и профилактика его обострений у женщин
Неймарк А.И., Раздорская М.В., Оберемок П.А.
Сведения об авторах:
Согласно статистическим данным, в России регистрируют 26-36 миллионов случаев заболевания острым циститом в год 3. Установлено, что у 50% женщин после эпизода цистита в течение года развивается рецидив, у 27% молодых женщин рецидив возникает в течение 6 месяцев, причем у 50% больных рецидивы наблюдают более трех раз в год [1,5-9]. В настоящее время хронический цистит у женщин является распространенным заболеванием и отличается длительным упорным течением [10,11]. Несмотря на пристальный интерес урологов к лечению хронического цистита, эта задача по-прежнему далека от окончательного решения. Сложность данной проблемы заключается в полиэтиологичной природе заболевания и множественности факторов, поддерживающих течение патологического процесса в стенке мочевого пузыря [3,12-15].
У женщин молодого и среднего возраста рецидивирующий цистит может приводить к длительной или повторной нетрудоспособности вследствие частых обострений [8,16]. Нарушения уродинамики нижних мочевых путей, микроциркуляции в слизистой мочевого пузыря и наличие бактериального агента во многом способствуют развитию и поддержанию воспалительного процесса в мочевом пузыре [17,18]. Причиной недостаточной эффективности лечения больных с хроническим циститом и частого рецидивирования заболевания является отсутствие рационального подхода к проведению лечебных мероприятий [2,9,19,20].
Целью исследования явилась оценка эффективности фосфомицина у женщин с хроническим циститом.
МАТЕРИАЛЫ И МЕТОДЫ
Нами проведено обследование 40 женщин с хроническим циститом. Все пациентки в зависимости от вида проводимого лечения разделены на основную и контрольную группы по 20 человек. Женщины основной группы получали фосфомицин каждые 7 дней на протяжении 6-9 недель. Пациентки контрольной группы получали фосфомицин 2 раза с промежутком 24 или 48 часов. Возраст пациенток в обеих группах колебался от 20 до 68 лет (средний возраст 45±2,7 лет).
Длительность заболевания в исследуемых группах составила от десяти месяцев до двадцати лет (табл. 1).
Таблица 1. Длительность заболевания у пациенток с рецидивирующим циститом
| Критерий | Контрольная группа (n=20) | Основная группа (n=20) |
|---|---|---|
| До 5 лет | 8 | 11 |
| До 10 лет | 8 | 4 |
| Более 10 лет | 4 | 5 |
Многие пациентки неоднократно получали лечение как в амбулаторных, так и в стационарных условиях. Терапия включала в том числе и инстилляции в мочевой пузырь. Длительность безрецидивного течения заболевания составляла от трех месяцев до пяти лет.
Диагностика заболевания проводилась на основании совокупности анамнестических и объективных клинических данных, лабораторноинструментальных методов, а также уродинамического обследования.
При первом обращении на каждую пациентку заводилась специальная карта, в которой отмечались особенности анамнеза жизни и заболевания, данные дополнительныхметодов обследования. При сборе жалоб уделяли внимание интенсивности и выраженности болевого синдрома, частоте мочеиспускания, чувству неполного опорожнения мочевого пузыря. Анамнез заболевания включал длительность заболевания, предшествующие возникновению заболевания факторы, виды проводимого ранее лечения, а также их эффективность и длительность безрецидивного периода. Тщательно анализировался гинекологический статус. Отмечали наличие очагов хронической инфекции как возможного источника инфицирования мочевого пузыря нисходящим путем.
Всем женщинам двукратно до курса терапии и после проводилось исследование показателей клинического анализа крови по общепринятой методике; общего анализа мочи для выявления наличия лейкоцитурии, бактериурии, гематурии; бактериологического посева мочи с определением чувствительности к антибиотикам. Биохимический анализ крови включал определение мочевины и креатинина.
В течение двух суток приема препарата и за двое суток до окончания курса пациентки основной группы вели дневник мочеиспускания. В контрольной группе заполнение дневников осуществлялось в первые двое суток и через 1 месяц. По результатам кратности мочеиспусканий и объема выделяемой мочи исходно и в конце лечения судили о динамике дизурических явлений.
Важным звеном в обследовании пациенток являлось уродинамическое исследование. Диагностика проводилась на аппарате Delphis IP, посредством которого выполнялась урофлоуметрия и цистометрия для оценки сократительной способности детрузора и выявления расстройств мочеиспускания. Для исключения ошибочных результатов уродинамический мониторинг выполнялся перед цистоскопией.
Неотъемлемой частью обследования являлась цистоскопия для определения состояния слизистой мочевого пузыря. Эндоскопическое исследование выполняли всем пациенткам эндоскопом фирмы Storz. При осмотре слизистой мочевого пузыря обращали внимание на зоны гиперемии, кровоизлияний, наличие эрозивных и язвенных дефектов, состояние слизистой в зоне треугольника Льето и шейки мочевого пузыря, выраженность сосудистого рисунка.
После проведенного обследования пациентки получали лечение по выше приведенной схеме.
Через 1 месяц все пациентки были повторно обследованы для оценки эффективности проведенного лечения, которая определялась по результатам контрольного бактериологического посева мочи, купированием воспалительного процесса по данным общего анализа мочи, исчезновением клинических симптомов у пациенток. Динамика исходных показателей уродинамики определялась при повторном проведении уродинамического мониторинга по окончании курса проводимой терапии. Изменения слизистой мочевого пузыря оценивались по результатам повторной цистоскопии через месяц. Еще через один месяц все пациентки являлись на прием для анкетирования и установления факта возможного обострения заболевания за данный период времени.
Сравнительный анализ количественных переменных, характеризующих клинико-лабораторное и функциональное состояние мочевыделительной системы, проводился методом описательной статистики с использованием непараметрического критерия УилкоксонаМанна-Уитни. Обработка и графическое представление данных проводилась с помощью компьютерных программ Statisticа 6.0 и Excel 2003.
РЕЗУЛЬТАТЫ
Наиболее частыми жалобами пациенток были боли в проекции мочевого пузыря, частое мочеиспускание малыми порциями, чувство дискомфорта в уретре, болезненное или с чувством дискомфорта мочеиспускание, чувство неполного опорожнения мочевого пузыря (табл. 2).
Таблица 2. Жалобы пациенток при поступлении
| Симптомы | Кол-во | % |
|---|---|---|
| Поллакиурия | 36 | 90 |
| Боли в надлобковой области | 32 | 80 |
| Жжение в уретре | 18 | 45 |
| Рези при мочеиспускании | 29 | 72,5 |
| Чувство неполного опорожнения мочевого пузыря | 21 | 52,5 |
| Боли в поясничной области | 2 | 5 |
| Повышение температуры тела | 3 | 7,5 |
Показатели клинического анализа крови у пациенток обеих групп были в пределах нормы. Показатели азотовыделительной функции почек не превышали нормальные пределы.
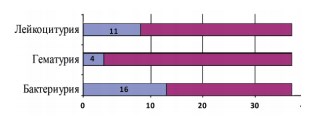
При изучении результатов общего анализа мочи имела место лейкоцитурия, бактериурия, микрогематурия. При исследовании мочи, содержание лейкоцитов более 10 в поле зрения наблюдалось у 11 (27,5%) больных; у 4 (10%) пациенток отмечалось наличие эритроцитов, при микроскопии бактериурия была выявлена в 16 (40%) случаях. У остальных пациенток моча была без изменений (рис. 1).
Рис. 1. Показатели общего анализа мочи в исследуемых группах
Всем пациенткам выполнялось бактериологическое исследование мочи с определением вида микроорганизма и микробного числа мочи. При этом, у 24 (60%) больных моча была стерильной. У остальных пациенток выявлялась следующая флора: Е. Coli – 8 (20%), Enteroccocus – 4 (10%), Staphylococcus haemolyticus – 1 (2,5%), Staphylococcus aureus – 3 (7,5%).
При выполнении цистоскопического исследования отмечены изменения, характерные для обострения хронического цистита – гиперемия, отек, в некоторых случаях имели место пролиферативные изменения слизистой (плоскоклеточная метаплазия по результатам патолого-гистологического исследования). При анализе эндоскопической картины с высокой частотой отмечались участки диффузной гиперемии, имелись разрастания слизистой мочевого пузыря. В основном изменения затрагивали область мочепузырного треугольника и шейки мочевого пузыря. Покровный эпителий в пораженных участках терял блеск, приобретал темно-красный цвет, становился отечным, легко кровоточил. Наиболее часто встречающиеся изменения слизистой оболочки мочевого пузыря представлены в таблице 3.
При выполнении цистоскопического исследования отмечены изменения, характерные для обострения хронического цистита – гиперемия, отек, в некоторых случаях имели место пролиферативные изменения слизистой (плоскоклеточная метаплазия по результатам патолого-гистологического исследования). При анализе эндоскопической картины с высокой частотой отмечались участки диффузной гиперемии, имелись разрастания слизистой мочевого пузыря. В основном изменения затрагивали область мочепузырного треугольника и шейки мочевого пузыря. Покровный эпителий в пораженных участках терял блеск, приобретал темно-красный цвет, становился отечным, легко кровоточил. Наиболее часто встречающиеся изменения слизистой оболочки мочевого пузыря представлены в таблице 3.
Таблица 3. Исходные данные цистоскопического исследования
| Критерий | Контрольная группа (n=20) | Основная группа(n=20) |
|---|---|---|
| Гиперемия шейки мочевого пузыря | 18(90) | 17(85) |
| Ворсинчатые разрастания в зоне треугольника Льето | 8(40) | 9(45) |
| Фолликулярные разрастания | 7 (35) 1 | 11 (55) |
| Белесоватые разрастания в области шейки мочевого пузыря | 2(10) | — |
| Трабекулярная исчерченность слизистой мочевого пузыря | — | 1(5) |
| Петехиальные кровоизлияния | 1(5) | 3(15) |
| Буллезный отек слизистой | 3(15) | 5(25) |
Выраженность дизурических явлений отражалась пациентками в дневниках мочеиспускания, которые они вели на протяжении двух суток с момента начала и за двое суток до окончания курса лечения (табл. 4).
Таблица 4. Данные дневников мочеиспускания в первые двое суток лечения
| Показатель | Контрольная группа (n=20) | Основная группа (n=20) |
|---|---|---|
| До 10 микций за сутки | 7 (35%) | 5 (25%) |
| До 15 микций за сутки | 9 (45%) | 10 (50%) |
| Более 15 микций за сутки | 4 (20%) | 5 (25%) |
При проведении цистометрии у ряда пациенток выявлены признаки гиперактивности. Цистометрическая емкость мочевого пузыря у пациенток в среднем составила от 200-300 мл. Результаты урофлоуметрии показали наличие обструктивного типа мочеиспускания у 12 (30%) пациенток, что вероятно было обусловлено явлениями тригонита. У 28 (70%) женщин уродинамических нарушений выявлено не было.
Через один месяц после проведенного лечения пациентки вновь были обследованы. В результате беседы и заполнения шкалы качества жизни пациентки основной группы отмечали снижение интенсивности клиники заболевания и выраженности дизурических явлений, что так же подтверждалось результатами дневников мочеиспускания в конце лечения.
У пациенток обеих групп не было обнаружено изменений показателей клинического и биохимического анализа крови. В моче 2 (10%) женщин контрольной группы и у 1 (5%) пациентки основной группы выявлена лейкоцитурия без клинических проявлений заболевания.
Согласно результатам бактериологического посева мочи лишь у 1 (5%) пациентки контрольной группы микрофлора была представлена Staphylococcus epidermidis. Остальные пробы мочи были стерильными.
При проведении повторной урофлоуметрии восстановление нормального мочеиспускания к концу лечения отмечено у всех пациенток исследуемых групп.
По результатам контрольной цистоскопии после курса лечения в основной группе в сравнении с контрольной отмечены более выраженные изменения слизистой оболочки в лучшую сторону (уменьшение гиперемии, петехиальных кровоизлияний, буллезного отека), что свидетельствует о выраженном противовоспалительном эффекте фосфомицина при еженедельном приеме.
На протяжении исследования у пациенток основной группы на фоне лечения непереносимости компонентов препарата или побочных явлений отмечено не было.
По результатам третьего посещения через месяц после проведенного лечения у 2 (10%) пациенток контрольной группы и у 1(5%) пациентки основной группы отмечался кратковременный эпизод обострения цистита, который был купирован приемом уросептиков.
ОБСУЖДЕНИЕ
По результатам исследования у женщин контрольной группы в более ранние сроки отмечено снижение клинических проявлений заболевания, купирование дизурических явлений.
По результатам бактериологического исследования на фоне лечения фосфомицином, принимаемым 1 раз в неделю на протяжении 6 – 9 недель, отмечается стойкий противомикробный эффект.
У пациенток основной группы отмечается восстановление уродинамики нижних мочевых путей, происходит устранение гиперактивности, о чем свидетельствуют показатели уродинамического исследования.
Согласно анализу результатов цистоскопических исследований отмечено положительное действие длительного приема фосфомицина на регресс эндоскопической картины при хроническом цистите у женщин.
Наблюдение пациенток через месяц после проведенного лечения указывает на низкий процент повторного возникновения заболевания у женщин основной группы.
В конечном итоге длительная схема лечения фосфомицином является эффективной и предупреждает рецидивы заболевания.
ЗАКЛЮЧЕНИЕ
Антибактериальный препарат фосфомицин оказывает противомикробное, противовоспалительное действие, способствует нормализации уродинамики нижнихмочевых путей, снижает риск повторных рецидивов хронического цистита. Препарат хорошо переносится пациентками. За время проведения исследования побочных эффектов на фоне лечения у пациенток выявлено не было. Таким образом, фосфомицин может быть рекомендован в качестве антибактериального препарата для лечения обострений хронического цистита, а так же средства для профилактики рецидивов данного заболевания.
ЛИТЕРАТУРА
Статья опубликована в журнале «Экспериментальная и клиническая урология» №2 2019 г., стр. 92-97
Хронический цистит: новое в диагностике и лечении
Рост хронических инфекционно-воспалительных заболеваний мочеполовой сферы, характеризующихся вялым, рецидивирующим течением, устойчивым к этиотропной терапии, представляет серьезную медицинскую проблему. Наиболее частым их проявлением является цистит
Рост хронических инфекционно-воспалительных заболеваний мочеполовой сферы, характеризующихся вялым, рецидивирующим течением, устойчивым к этиотропной терапии, представляет серьезную медицинскую проблему. Наиболее частым их проявлением является цистит. Цистит — изменение слизистой оболочки мочевого пузыря воспалительного характера, сопровождающееся нарушением его функции [1, 2]. Как правило, циститом страдают женщины трудоспособного возраста. В случае распространения воспалительного процесса глубже слизистой оболочки процесс приобретает хроническое течение. По данным литературы хронизация процесса выявлена более чем в трети случаев. Возникает она на фоне органических и функциональных изменений мочевого пузыря или у людей с серьезными сопутствующими заболеваниями [3, 4]. Хронический цистит сопровождается в той или иной мере выраженным болевым симптомом, приводит к социальной дезадаптации пациентов, временной или постоянной потере трудоспособности, а реабилитация требует дополнительных бюджетных вложений [5]. Большинство рецидивов возникают в первые 3 месяца после излечения предшествующего эпизода [6]. Более 60% случаев острого неосложненного цистита остается без должного лечения. В случае самопроизвольного излечения неосложненного цистита заболевание рецидивирует в течение года почти у половины женщин [7].
Этиология и патогенез
Мочевой пузырь у женщин обладает значительной резистентностью, которая обусловлена наличием ряда антибактериальных механизмов, постоянно и эффективно действующих у здоровых женщин. Инвазия бактерий в мочевой пузырь не является основным условием развития воспалительного процесса, что имеет большое число клинических и экспериментальных подтверждений. Нормальный ток мочи и своевременное опорожнение мочевого пузыря предотвращают инфицирование мочевых путей. Своевременное выделение даже инфицированной мочи снижает риск адгезии бактериальной клетки к рецепторам слизистой оболочки.
Слизистая оболочка мочевого пузыря обладает бактериостатической активностью, особенно по отношению к кишечной палочке, благодаря выработке специфических мукополисахаридов и секреторного IgA. Кроме того, моча может содержать специфические и неспецифические ингибиторы роста бактерий, иммуноглобулины класса А и G. Неповрежденный уротелий обладает значительной фагоцитарной активностью. При возникновении цистита в организме человека первоначально происходит активация местного и гуморального иммунитета в виде выработки антител. Известно, что при хронических заболеваниях возникает транзиторная дисфункция иммунной системы [9], в то же время в большинстве случаев цистит является вторичным, то есть осложняет течение имеющихся заболеваний мочевого пузыря, уретры, почек, половых органов [1].
Нередко рецидивы обусловлены персистенцией инфекции, но в подавляющем большинстве случаев объясняются реинфекцией [10]. Под персистирующей инфекцией понимают наличие инфекции одного вида или штамма, и рецидив возникает, как правило, в течение 1–2 недель после прекращения лечения. Реинфекция это повторный инфекционный процесс, обусловленный другим возбудителем. Обычно она развивается через несколько недель после окончания терапии [5, 11].
Ведущую роль в патогенезе любых хронических воспалительных заболеваний играет гипоксия тканей и транзиторная дисфункция иммунной системы [9, 12]. Под хроническим воспалением понимают процессы, протекающие недели и месяцы, при которых повреждающий фактор, реактивные изменения и рубцевание развиваются одновременно [13]. Традиционно по времени возникновения хронического воспалительного процесса считается срок более 60 дней.
Специфической предпосылкой хронического воспалительного процесса является невозможность завершения острого воспаления регенерацией, протекающей на фоне нарушенного тканевого гомеостаза [14]. В результате при хроническом воспалении нередко имеет место смена фаз затихания и обострения процесса, что накладывает отпечаток и на его морфологию. Если при остром течении воспалительных процессов на первое место выступают альтеративные и сосудисто-экссудативные изменения, то при подостром и хроническом — пролиферативные, завершающиеся новообразованием соединительной ткани, то есть склерозом [15]. Подслизистые структуры в стенке мочевого пузыря играют основополагающую роль, поскольку между эпителиальными клетками нет капилляров, и жизнедеятельность клеток эпителия зависит от эффективности диффузии кислорода и питательных веществ из подлежащей соединительной ткани (через ее межклеточное вещество и базальную мембрану) [16].
Наличие очагов хронического воспаления зависит от возрастных и конституциональных особенностей эпителиальных тканей, модифицирующих как клеточную устойчивость, так и метаболический фон, на котором развивается процесс воспаления. Развитию хронического воспаления содействуют в первую очередь возрастное увеличение чувствительности клеток к окислительному стрессу. В то же время при гипоксии ускорятся процесс мобилизации и деления незрелых эпителиальных клеток [12], блокируется их созревание. Известно, что незрелый эпителий обладает повышенной способностью клеток к бактериальной адгезии. Баткаев Э. А., Рюмин Д. В. (2003) в исследованиях, когда возбудителем цистита была кишечная палочка, обратили внимание на возраст пациенток. Так, у женщин до 55 лет рецидивы болезни в течение года происходили в 36%, в то время как рецидивы у женщин старше этого возраста возникли в 53% [17].
Классификация хронических циститов [18]:
В зависимости от характера и глубины морфологических изменений хронический цистит делится на катаральный, язвенный, полипозный, кистозный, инкрустирующий, некротический.
Клиническая картина
Хронический цистит в фазу обострения проявляется теми же симптомами, что и острый цистит. Кроме того, могут играть роль симптомы основной патологии, послужившей хронизации процесса (симптомы камня мочевого пузыря, атонии и т. д.). При обострении заболевания наиболее частой причиной жалоб пациенток является учащенное болезненное мочеиспускание. При хронических заболеваниях, в зависимости от степени поражения мочевого пузыря, боль может быть постоянной, иногда с мучительными позывами на мочеиспускание; локализуется в области лобка либо в глубине малого таза. Боль может появляться или усиливаться в связи с актом мочеиспускания. В последнем случае она возникает либо перед началом мочеиспускания вследствие растяжения стенок мочевого пузыря, либо во время акта мочеиспускания, но чаще всего — в его конце. Следует помнить о том, что боль в мочевом пузыре с нарушением акта мочеиспускания может возникнуть при воспалительных заболеваниях женских половых органов [19].
Диагностика хронических циститов является сложной проблемой, требующей от врача использования ряда клинических и параклинических методов, аналитического подхода к их результатам. Клинический этап обследования должен включать тщательный сбор анамнеза, с учетом данных о состоянии половой сферы пациентки, связи заболевания с половой жизнью; осмотр в «зеркалах» для исключения вагинизации уретры, наличия уретрогименальных спаек. Базово-диагностический этап включает лабораторные исследования, обязательной составляющей которых является бактериологическое исследование мочи, определение чувствительности флоры к антибиотикам; УЗИ и при необходимости рентгеновское исследование органов малого таза и верхних мочевых путей, исследование пациенток на наличие ИППП. Анализ результатов бактериологических посевов мочи, выполненных в нашей клинике, у больных хроническим рецидивирующим циститом показал, что традиционно принятый диагностический критерий бактериурии 10 5 КОЕ в 1 мл средней порции мочи был выявлен только в 21,3%. Многие исследователи обращают внимание на то, что в клинической практике феномен «малой бактериурии» недооценен [11, 20]. У пациенток с наличием хронического цистита и угрозой рецидива мы принимаем во внимание бактериурию 10 3 КОЕ в 1 мл.
Завершающим и обязательным этапом обследования является эндоскопическое обследование. Для выяснения причины хронизации процесса выполняется цистоскопия. Однако это достаточно субъективный метод, при котором часто возникают трудности в интерпретации визуальной картины поверхности слизистой оболочки мочевого пузыря [20]. Кроме того, хроническое воспаление сопровождается хронической индукцией регенерационного микроокружения, идентичного опухолевому, то есть в эпителии могут появляться гистологические изменения, относящиеся к предраковым: гиперплазия, дисплазия, метаплазия [12]. Многие авторы признают необходимость выполнения мультифокальных биопсий для понимания и правильной морфометрической характеристики процессов, происходящих в стенке мочевого пузыря [2, 21].
При хронических воспалительных заболеваниях в мочевом пузыре оптимально от 8 до 15 биоптатов, хотя эффективность рандомных биопсий в свете онконастороженности оспаривается некоторыми авторами [22, 23]. Биопсия — всегда дополнительная травма, провоцирующая воспалительные изменения, а в редких случаях кровотечения и перфорации стенки мочевого пузыря.
Дифференцировать явления хронического цистита от неопластических изменений, а также объективно оценить изменения состояния слизистой и подслизистой структур мочевого пузыря позволяет оптическая когерентная томография (ОКТ) и ее вариант кросс-поляризационная ОКТ (КП ОКТ) [24, 25]. Метод ОКТ демонстрирует оптические свойства ткани в поперечном сечении. Изображение может быть получено в реальном времени с разрешением 10–15 мкм. Принцип ОКТ подобен B-скану ультразвука. Оптическое изображение формируется за счет различия оптических свойств внутритканевых слоев или структур — коэффициента обратного рассеяния тканей [22, 23]. КП ОКТ несет большую информацию о ткани, поскольку ряд компонентов слоистой структуры органов (например, коллаген) способен рассеивать зондирующее излучение не только в основную поляризацию (нижнее изображение), совпадающую с поляризацией зондирующей волны, но и в ортогональную (верхнее изображение). Компактный переносной оптический томограф, созданный в Институте прикладной физики РАН Нижнего Новгорода, оснащен съемным зондом, совместимым с эндоскопическим оборудованием. Во время эндоскопических манипуляций гибкий зонд — сканер оптического когерентного томографа c торцевой оптикой (внешний диаметр 2,7 мм) проводится через инструментальный канал 8 Ch операционного цистоскопа 25 Ch и прижимается под контролем зрения к интересующему участку стенки мочевого пузыря. Исследование ОКТ выполняется последовательно в правой и левой гемисферах, нижнем, среднем и верхних сегментах мочевого пузыря. Время получения одного изображения — 1–2 секунды. Визуально измененные зоны изучаются прицельно. При необходимости из оптически подозрительных зон выполняются прицельные биопсии. Анализ клинических данных показал, что ОКТ с хорошей чувствительностью (98–100%) и специфичностью (71–85%) выявляет неоплазию в мочевом пузыре. В результате мониторирования хронических циститов с ОКТ, проведенных в нашей клинике, выполнение биопсии снизилось на 77,6% (рис. 1). На рис. 1 а цистоскопическое изображение, зонд — сканер оптического когерентного томографа под устьем: отек и умеренная гиперемия под устьем мочевого пузыря. На рис. 1 б оптическое изображение до лечения: эпителиальный слой утолщен, подслизистые структуры плохо дифференцируются от верхнего эпителиального слоя за счет инфильтрации; изображение отнесено к подозрительным на неоплазию в результате очаговой потери слоистости. На рис. 1 в динамическое исследование после комплексного лечения через 5 недель: эпителиальный слой нормальной толщины, подслизистые структуры хорошо дифференцируются.
Включение методов оптической визуализации ОКТ и КП ОКТ в исследование стенки мочевого пузыря на наш взгляд является перспективным, поскольку позволяет проводить дифференциальную диагностику хронического цистита с заболеваниями, имеющими сходную клиническую симптоматику, исключая/или минимизируя выполнение биопсий. Выявление на ОКТ-изображениях очаговой пролиферации эпителия, а также изображений с нарушенной структурной организацией (граница эпителий/подслизистые структуры нечеткая или неровная) позволяет выделить пациенток, требующих пристального внимания в отношении угрозы малигнизации и, следовательно, их длительного мониторинга.
Наличие тонкого/атрофичного эпителиального слоя слизистой оболочки мочевого пузыря на ОКТ-изображении позволяет заподозрить эстрогенный дефицит, направить больного на консультацию к гинекологу. У женщин в постменопаузе эстрогенный дефицит является причиной урогенитальных расстройств.
У пациенток, длительно страдающих хроническим циститом, на КП ОКТ-изображении выявляется выраженное утолщение подслизистых структур, имеющих повышенный контраст, что свидетельствует о склеротическом процессе в стенке мочевого пузыря (рис. 2). На рис. 2 а КП ОКТ-изображение нормального мочевого пузыря: эпителиальный слой нормальной толщины, подслизистые структуры, мышечный слой в норме. На рис. 2 б КП ОКТ-изображение мочевого пузыря при хроническом рецидивирующем цистите: эпителиальный слой атрофичен (прямая поляризация — нижнее изображение), подслизистые структуры разволокнены; слой, содержащий колагеновые волокна, менее контрастен, расширен и определяется практически на весь кадр изображения (обратная поляризация — верхнее изображение). На рис. 2 в КП ОКТ-изображение мочевого пузыря пациентки с травмой позвоночника. Изменения идентичны изображению 2 б.
Таким образом, КП ОКТ позволяет объективно оценивать изменения, происходящие в подслизистых структурах стенки мочевого пузыря, и в зависимости от этого проводить коррекцию лечения.
Лечение
Если диагноз хронического бактериального цистита в большинстве случаев не вызывает затруднений, то лечение не всегда оказывается эффективным, а прогноз не всегда благоприятным, так как в ряде случаев не удается выявить, а затем и устранить причину возникновения заболевания. Лечение хронических циститов требует от врача широкого кругозора, знаний проблем гинекологии, неврологии, иммунологии. В период становления болезни структурные изменения опережают клинические проявления, и, наоборот, в процессе выздоровления нормализация нарушенных функций наступает раньше восстановления поврежденных структур, т. е. морфологические проявления запаздывают по сравнению с клиническими [16]. Только зрелые эпителиоциты резистентны к бактериям, в то время как барьерная функция эпителия при наличии эпителиоцитов с умеренно дифференцированной ультраструктурой нарушена. Для лечения и профилактики хронических рецидивирующих инфекций нижних мочевых путей применяется этиотропная антибактериальная терапия 7–10-дневными курсами. Исследования Возианова А. Ф., Романенко А. М. с соавт. (1994) показали, что полное восстановление зрелых поверхностных клеток эпителия мочевого пузыря после их повреждения длится не менее 3 недель [26]. Таким образом, при отсутствии настороженности у лечащего врача и отсутствии должного внимания к длительности патогенетического лечения, очередной рецидив может наслоиться на репаративную фазу предыдущего процесса. Это в свою очередь приводит к усилению коллагенообразования, дискорреляциям и склерозу подэпителиальных структур, играющих основную роль в гомеостазе слизистой оболочки мочевого пузыря, его иннервации [27]. Таким образом возникает замкнутый круг: неадекватное лечение — хроническое воспаление — реактивные изменения и рубцевание подслизистых структур — гипоксия ткани — незавершенная регенерация эпителия — очередное обострение процесса.
Лечение хронических рецидивирующих циститов:
Этиологическое лечение — это антибактериальная терапия, основанная на следующих принципах: длительность (до 7–10 дней); выбор препарата с учетом выделенного возбудителя и антибиотикограммы; назначение антибиотиков с бактерицидным действием. Препаратами, к которым выделен наибольший процент чувствительных штаммов возбудителей мочевой инфекции в России, являются: фосфомицин — 98,6%, мециллинам — 95,4%; нитрофурантоин — 94,8% и ципрофлоксацин — 92,3% [28]. Наиболее предпочтительными являются норфлоксацин, ципрофлоксацин, пефлоксацин и левофлоксацин из-за отсутствия нежелательных побочных реакций.
Выбор антибактериального препарата должен производиться на основе данных микробиологического исследования. Если при остром неосложненном цистите предпочтение следует отдавать коротким курсам антибактериальной терапии (3–5-дневным), то при хроническом рецидивирующем — продолжительность антибактериальной терапии должна составлять не менее 7–10 дней для полной эрадикации возбудителя, который при хронических циститах может локализоваться в подслизистых структурах стенки мочевого пузыря [1, 5].
Антибактериальная терапия. Препаратами выбора являются фторхинолоны (ципрофлоксацин, офлоксацин, норфлоксацин, левофлоксацин, ломефлоксацин), которые обладают очень высокой активностью в отношении E. сoli и других грамотрицательных возбудителей уроинфекций. Нефторированные хинолоны — налидиксовая, пипемидовая, оксолиновая кислоты утратили свое лидирующее значение, в связи с высокой резистентностью к ним микрофлоры, и не могут являться препаратами выбора при рецидивирующих инфекциях мочевых путей [18, 29].
Выбор фторхинолонов обусловлен широким спектром антибактериальной активности, особенностями фармакокинетики и фармакодинамики, созданием высоких концентраций в крови, моче и тканях. Биодоступность фторхинолонов не зависит от приема пищи, они обладают длительным периодом полувыведения, что позволяет принимать препараты 1–2 раза в сутки. Их отличает хорошая переносимость и возможность применения при почечной недостаточности. Для норфлоксацина период полувыведения 3–4 часа, для лечения обострения цистита рекомендуется принимать по 400 мг 2 раза в день 7–10 дней. Ципрофлоксацин считается наиболее мощным антибиотиком из группы фторхинолонов, поскольку, обеспечивая бактерицидный эффект в небольших концентрациях, обладает широким спектром антибактериальной активности и быстро распределяется и накапливается в тканях и биологических жидкостях с высокими интрацеллюлярными концентрациями в фагоцитах (принимают 500 мг 2 раза в день). В настоящее время созданы препараты, обеспечивающие удобство приема — 1 раз в день. Примером может быть Ифиципро ® ОД, который является новой формулой с постепенным высвобождением ципрофлоксацина.
При выявлении ИППП необходим курс антибактериальной терапии с включением макролидов, тетрациклинов, фторхинолонов, направленный на эрадикацию возбудителя, с последующим контролем микрофлоры.
Патогенетическое лечение начинают с рекомендаций по соблюдению режима труда и отдыха и назначения соответствующего питания. Назначают обильное питье. Усиленный диурез способствует вымыванию бактерий и других патологических примесей. Уменьшаются дизурические явления вследствие действия концентрированной мочи на слизистую оболочку мочевого пузыря. Пища должна быть полноценной по содержанию белков и витаминов и способствовать кишечной перистальтике. В настоящее время разработаны патогенетически обоснованные алгоритмы консервативной терапии воспалительных заболеваний нижних мочевых путей [18].
Наличие современных антибиотиков и химиотерапевтических препаратов позволяет быстро и эффективно вылечивать рецидивы инфекций мочевыводящих путей и проводить профилактику их возникновения. Необоснованность и нерациональность антибактериальной терапии являются факторами, приводящими к хронизации процесса и нарушениям иммунорегуляторных механизмов с развитием иммунодефицитных состояний. Важно, что иммунодефицитное состояние может не иметь клинических проявлений [30]. Понятие «иммунодефицит» включает состояния, при которых наблюдается отсутствие или снижение уровня одного или нескольких факторов иммунитета. Исследования, проведенные в нашей клинике, показали, что у пациенток с хроническими циститами имеются отклонения в иммунном статусе в виде повышения или понижения показателей от среднестатистической нормы у 33,3%. Альтернативой назначению антибактериальных препаратов является стимуляция иммунных механизмов организма пациента при назначении иммунотерапевтических препаратов. Одним из таких препаратов является лиофилизированный белковый экстракт, полученный путем фракционирования щелочного гидролизата некоторых штаммов E. coli. Препарат выпускается в капсулах, имеет торговое наименование Уро-Ваксом. Стимуляция неспецифических иммунных защитных механизмов Уро-Ваксомом является приемлемой альтернативой низкодозной длительной химиопрофилактике инфекций мочевыводящих путей [31].
Заслуживает внимания применение поливалентных бактериофагов в лечении хронического рецидивирующего цистита, что особенно актуально для пациентов с поливалентной аллергией к антибактериальным препаратам или наличием полирезистентных возбудителей. Несмотря на отсутствие плацебо-контролируемых исследований применения пиобактериофагов, клиническая эффективность указанных препаратов не вызывает сомнений [18].
Важнейшим звеном патогенетической терапии цистита, способной предотвратить хронизацию воспаления, является иммуномодулирующая терапия. Регуляторами иммунных реакций являются цитокины, основная их составляющая — интерфероны (ИНФ). Функции ИНФ в организме разнообразны, однако наиболее важной функцией ИНФ является антивирусная. Кроме того, ИНФ участвуют также в антимикробной защите, обладают антипролиферативными, иммуномодулирующими свойствами. ИНФ способны модулировать активность и других клеток, например нормальных киллеров, увеличивать лизис клеток-мишеней, продукцию иммуноглобулинов, фагоцитарную активность макрофагов и их кооперативное взаимодействие с Т- и В-лимфоцитами. Гамма-ИНФ ингибирует рост опухолевых клеток и подавляет внутриклеточное размножение бактерий и простейших [9, 30]. Существуют препараты, содержащие экзогенные ИНФ. Однако индукторы ИНФ имеют преимущества перед ними, поскольку лишены антигенных свойств, синтез их в организме всегда строго сбалансирован и, таким образом, организм огражден от перенасыщения интерферонами [32]. Впервые для комплексного лечения хронических рецидивирующих циститов нами был применен тилорон, торговое название препарата «Лавомакс ® » (таблетки 125 мг). Прием препарата «Лавомакс ® » позволил добиться ремиссии заболевания у 90%, эрадикация микрофлоры в моче достигнута в 66,7%. Результаты наших исследований показали несомненную перспективность использования Лавомакса ® не только для лечения, но и для профилактики хронических циститов.
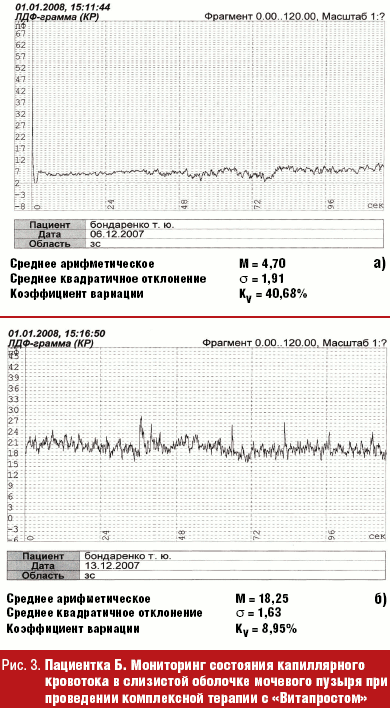
Хронический процесс, с учетом сопутствующей патологии пациенток, требует обязательного применения препаратов для борьбы с гипоксией тканей — антигипоксантов (Солкосерил 200 мг по 1 таблетке 2 раза в день, курс 14 дней); венотоников (Эскузан 20); антиагрегантов, которые улучшают «текучесть» крови по капиллярам. Типичным представителем группы антиагрегантов является Трентал, оказывающий сосудорасширяющее, антиагрегантное, ангиопротективное действие (100 мг 2–3 раза в сутки, курсом до 30 дней), действующее вещество — пентоксифиллин. Пентоксифиллин-Акри удобен в приеме, так как имеет таблетированную форму 100 мг, улучшает микроциркуляцию и снабжение тканей кислородом в основном в конечностях, центральной нервной системе, в меньшей степени в почках. Существует масса препаратов, улучшающих артериальное и венозное кровообращение. Однако на сегодняшний день есть препарат, который способен восстанавливать микроциркуляцию и тонус мышц мочевого пузыря; доказано его благотворное влияние на показатели иммунитета. Это хорошо зарекомендовавший себя в лечении заболеваний предстательной железы Простатилен — комплекс полипептидов, выделенных из тканей предстательной железы крупного рогатого скота [33]. Нас заинтересовала способность пептидов (цитомединов) выступать в организме в качестве биорегуляторов. Действие их предположительно осуществляется через рецепторы, расположенные на поверхности клеток. В результате их введения в организм происходит выброс эндогенных регуляторных пептидов, пролонгируется эффект цитомединов [34]. Традиционно используемый в лечении патологии мужской половой сферы препарат «Витапрост ® » (суппозитории ректальные 50 мг) был впервые применен в клинике урологии Нижнего Новгорода для лечения хронических рецидивирующих циститов у женщин. Изучая капиллярный кровоток в слизистой мочевого пузыря у пациенток с хроническим рецидивирующим циститом методом лазерной допплеровской флоуметрии (ЛДФ) [35, 36], мы получили объективно доказанный эффект от применения этого препарата (рис. 3). На рис. 3 а мониторинг до лечения, показатель микроциркуляции (ПМ) — 4,7 перфузионных единицы. На рис. 3 б мониторинг после лечения (ПМ — 18,25 перфузионных единицы).
До лечения у больных выявлялся застойный тип кровотока со сниженной активностью компонентов микроциркуляторного русла и ишемией тканей. Примененный в качестве патогенетической терапии в лечении хронических циститов биостимулирующий препарат «Витапрост ® » способствовал быстрому исчезновению воспалительного процесса, стимуляции регенераторных процессов, что мы контролировали КП ОКТ. Назначенный препарат позволил достичь быстрого эффекта анальгезии, помог достичь социальной адаптации пациенток в достаточно в короткий срок.
Лечение рецидивирующих инфекций нижних мочевых путей, протекающих на фоне ИППП, при наличии диспластических процессов в задней уретре, зоне шейки мочевого пузыря, мочепузырного треугольника должно быть направлено на эрадикацию атипичных возбудителей, восстановление муцинового слоя уротелия. Образование мукополисахаридного слоя, покрывающего в норме эпителий мочевого пузыря, считается гормонально-зависимым процессом: эстрогены влияют на его синтез, прогестерон на его выделение эпителиальными клетками. Применение женских половых гормонов интравагинально ведет к пролиферации влагалищного эпителия, улучшению кровоснабжения, восстановлению транссудации и эластичности стенки влагалища, увеличению синтеза гликогена, восстановлению популяции лактобацилл во влагалище, кислого рН. Примером эстрогена для лечения урогенитальных нарушений является препарат эстриола — Овестин, имеется таблетированная форма 2 мг и в виде вагинальных свечей по 0,5 мг. При использовании любой формы Овестин назначается 1 раз в сутки.
При наличии выраженного болевого синдрома назначают нестероидные противовоспалительные препараты, подавляющие синтез простагландинов, оказывающие выраженное обезболивающее действие. Назначают индометацин, диклофенак и другие. Препараты используются в обычных дозах в течение 10–21 дня, поддерживающие дозировки до 2 месяцев. Эффект от нестероидных противовоспалительных препаратов, как правило, сохраняется в течение 3–4 месяцев после их отмены [1].
Назначение антигистаминных и антисеротониновых препаратов необходимо для устранения этиологического и патогенетического факторов. Это может быть препарат «Перитол» — блокатор Н1-гистаминорецепторов с выраженным антисеротониновым действием. Он также стабилизирует тучные клетки и препятствует их дегрануляции с освобождением биологически активных веществ. Антихолинэстеразная активность его сказывается на накопительной функции мочевого пузыря. Препарат принимают с 2 мг — 1 раз в день, постепенно увеличивая дозу до 4 мг — 3 раза в сутки в течение 3–4 недель. Задитен (кетотифен) назначается в дозе 0,5–1 мг — 2 раза в сутки 2–3 месяца. Назначаются и другие антигистаминные препараты (Диазолин, Тавегил, Кларитин) в обычном режиме в течение 1–3 месяцев.
Местное лечение
Выраженным антигистаминным действием, а также способностью восстанавливать гликоз — амино-гликановый компонент муцина обладает природный мукополисахарид — Гепарин, который можно вводить внутрипузырно по 10 000 ЕД 3 раза в неделю в течение 3 месяцев. Местная противовоспалительная терапия включает инстилляции различных лекарственных препаратов или их сочетаний в мочевой пузырь. Для инстилляции используются растворы Диоксидина, нитрата серебра в разведении 1:5000, 1:2000, 1:1000 в 1–2% концентрации. Для инстилляции широко используются растворы коллоидного серебра. Антимикробный эффект коллоидного серебра зарегистрирован в отношении более чем 650 видов микроорганизмов, среди которых грамположительные и грамотрицательные бактерии, вирусы, простейшие, спорообразующие, анаэробы. Коллоидное серебро активно в отношении различных видов протея и синегнойной палочки, бактерии Коха [1, 5, 37].
Следует отметить, однако, что применение без достаточных показаний катетеризации мочевого пузыря является опасным, поскольку доказано, что 80% нозокомиальных инфекций связаны с введением уретральных катетеров [38].
Немедикаментозные методы лечения, такие как лечебная физкультура, физиотерапевтические процедуры, направлены на укрепление мышц тазового дна и нормализацию тазового кровообращения.
Профилактика
В качестве профилактики обострений у женщин с рецидивирующей инфекцией нижних мочевых путей рекомендованы в субингибирующих дозах ежедневно или после полового акта ципрофлоксацин 125 мг, нитрофурантоин 50 мг, норфлоксацин 200 мг, фосфомицин по 3 г каждые 10 дней в течение 6 месяцев. У женщин в постменопаузе применение заместительной гормональной терапии эстриолом ведет к снижению риска обострения заболевания до 11,8 раза по сравнению с плацебо [19, 28].
Анализ обращаемости пациенток по поводу обострений хронического цистита, проведенный на нашей кафедре, показал, что пик приходится на конец мая, начало июня, а также октябрь-ноябрь. В связи с этим целесообразно рекомендовать курсы профилактического лечения именно в эти периоды.
Таким образом, универсальный метод лечения хронических рецидивирующих циститов отсутствует. От лечащего врача требуется дифференцированный подход к методам лечения, адекватным этиологическим и патогенетическим факторам, а также индивидуальным особенностям течения заболевания пузыря у каждой пациентки.
По вопросам литературы обращайтесь в редакцию.
О. С. Стрельцова, кандидат медицинских наук
В. Н. Крупин, доктор медицинских наук, профессор
ГОУ ВПО «НижГМА», Нижний Новгород