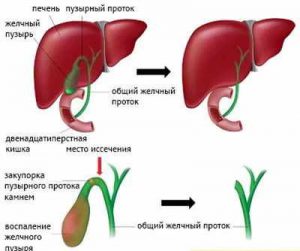
После удаления желчного пузыря
Полноценная жизнь после удаления желчного пузыря
Нарушения работы пищеварительной системы в той или иной степени встречаются у каждого человека. Вместе с тем существуют заболевания, которые буквально делят жизнь на до и после. Именно к таким относится желчнокаменная болезнь, требующая хирургического вмешательства.
По статистике, ЖКБ встречается примерно у 10―20% взрослого населения нашей страны в зависимости от региона. Орган играет важную роль в процессе пищеварения, поэтому жизнь без желчного пузыря требует соблюдения ряда правил и ограничений, о которых мы расскажем далее.
Функции желчного пузыря

За сутки печень вырабатывает около полутора литров желчи, однако ее состав и свойства меняются при попадании в желчный пузырь. В нем почти в 10 раз повышается концентрация желчных кислот, билирубина и холестерина за счет всасывания воды и других элементов через стенки органа.
Работа желчного пузыря обеспечивает следующие процессы:
Причины появления камней в желчном пузыре

Симптомы желчнокаменной болезни

Желчнокаменная болезнь диагностируется на основании лабораторных анализов, УЗИ, КТ, МРТ, а также рентгенологического исследования.
Выявление камней в желчном пузыре не всегда требует специфического лечения. Если у пациента нет осложнений, то врачи прибегают к выжидательной тактике. Помимо этого, разработаны методы растворения песка и камней с помощью ряда препаратов, но подобная терапия не является панацеей от ЖКБ. Со временем камни образуются снова.
Удаление ЖП показано при появлении осложнений, таких как острый или хронический калькулезный холецистит. При успешном хирургическом лечении пациент избавляется от негативных симптомов без каких-либо серьезных последствий для качества жизни.
Что происходит в организме после операции по удалению желчного пузыря?

В 95% случаев хирургическое лечение приносит только облегчение и пациент начинает себя чувствовать так, словно вмешательства не было. Вместе с тем удаление органа пищеварительной системы не может пройти бесследно. После операции в организме происходит как минимум 3 важных изменения:
1. Желчи больше негде скапливаться, поэтому она начинает непрерывно поступать в двенадцатиперстную кишку.
2. Образующийся в печени секрет оказывает давление на протоки.
3. Желчь больше не очищается от избытка воды, хлора и натрия, поэтому постепенно меняется состав микрофлоры кишечника.

Ухудшение самочувствия и другие негативные последствия могут наблюдаться у пациентов с заболеваниями двенадцатиперстной кишки или поджелудочной железы, в остальных случаях у операции больше плюсов, чем минусов.
Пищеварение после удаления желчного пузыря


Восстановление после удаления желчного пузыря

На вторые сутки разрешено пить травяные отвары, нежирный кефир, можно есть жидкое картофельное пюре на воде. Далее на протяжении недели в меню постепенно вводятся протертые каши, легкие бульоны, нежирное мясо и рыба, ржаные сухари.
Важно! Желчь выводится из протоков только во время приема пищи, поэтому пациенту необходимо перейти на дробное питание. Кушать необходимо 5―6 раз в день. При соблюдении этого правила желчь не будет застаиваться, следовательно, в протоках не образуются новые камни и не начнется воспалительный процесс.

Лекарства после удаления желчного пузыря

«Холосас» — сироп растительного происхождения с широким терапевтическим эффектом. Действующий компонент препарата — экстракт плодов шиповника, богатый витаминами и минералами.
Сироп, как указано в инструкции, усиливает секрецию желчи, стимулирует перистальтику кишечника, оказывает мягкое противовоспалительное действие, активизирует работу поджелудочной железы, повышает устойчивость организма к инфекционным и бактериальным заболеваниям.
«Аллохол» — желчегонное средство растительного происхождения, в состав которого входят экстракты крапивы, чеснока, пчелиный воск, а также сухая желчь животных.
Препарат, в соответствии с аннотацией, способствует стимуляции работы печени, восстановлению моторных функций органов пищеварения, устранению воспалительных процессов, выведению токсических веществ из кишечника.

Препарат, согласно инструкции, способствует очищению печени от токсинов, нормализации работы мочевыделительной и желчегонной системы. Многие пациенты отмечают на фоне приема «Хофитола» нормализацию артериального давления и улучшение аппетита.

Применение этого средства позволит устранить боль в правом подреберье, тошноту, изжогу. «Одестон», как сказано в аннотации, усиливает синтез и эвакуацию желчи, снижая риск образования камней, а также снимает спазмы гладкой мускулатуры кишечника.
Помимо этого, врач может назначить гепатопротекторы — лекарства, которые необходимо принимать после удаления желчного пузыря. Это группа препаратов, направленных на нормализацию работы печени и других органов пищеварения.

«Карсил», согласно инструкции, обладает мембраностабилизирующим и антигипоксическим свойствами. Кроме этого, средство препятствует жировому перерождению клеток печени и нарушению оттока желчи. Препарат способен значительно облегчить симптоматику заболеваний печени, при этом его часто назначают вместе с другими лекарствами.

Как сказано в инструкции, действующее вещество лекарственного средства снижает концентрацию холестерина в желчных протоках. Благодаря этому в желчи повышается содержание желчных кислот, которые способствуют растворению конкрементов. Помимо этого, препарат усиливает секрецию желудка и поджелудочной железы.

Согласно инструкции «Эссенциале Форте Н» регулирует процессы углеводного и жирового обмена в организме, а также усиливает дезинтоксикационные функции печени. Фосфолипиды предотвращают жировую дистрофию органа, снижают вероятность образования новых камней в протоках. Это один из немногих препаратов, которые врачи иногда назначают беременным женщинам при проблемах с пищеварением.

Препарат, в соответствии с аннотацией, оказывает выраженный гепатопротекторный и желчегонный эффект, а также умеренное антиоксидантное действие. После курса приема «Гепабене» многие пациенты отмечают избавление от дискомфорта и спазмов в животе, устранение отрыжки и изжоги.

Препарат содержит растительные экстракты расторопши, листьев артишока, витамины группы В, лецитин и другие вещества, улучшающие работу системы пищеварения. Вместе с тем «Гепатрин» не может применяться как самостоятельное лекарство, его назначают в составе комплексной терапии.
Важно! Несмотря на то, что многие перечисленные препараты изготовлены на основе натуральных растительных компонентов, их применение должно согласовываться с лечащим врачом. Бесконтрольный прием гепатопротекторных лекарств может привести к ухудшению самочувствия пациента, перенесшего операцию по удалению желчного пузыря.
Диета после удаления желчного пузыря
Жизнь после удаления желчного пузыря: важные советы
Питание. Помимо дробного приема пищи, пациентам рекомендуется выпивать в день до 2 литров воды без газа. Запивать еду при этом нежелательно, чтобы не снижать концентрацию пищеварительных ферментов. Следует ограничивать употребление растительного и сливочного масла, сладостей и консервированных продуктов. Алкоголь и курение также под запретом.
Физическая активность. Несмотря на то, что интенсивные занятия спортом первые полгода не допускаются, движение необходимо для нормальной работы пищеварительной системы. Первые тренировки можно начинать на 6 неделе после операции. Сначала это может быть ходьба, затем по нарастающей легкий бег и упражнения в тренажерном зале.
Лекарства. Жить полноценно после удаления желчного пузыря помогает прием препаратов, стимулирующих выработку пищеварительных ферментов. Схему лечения должен составлять врач в соответствии с индивидуальными особенностями организма пациента. Самолечение и прием БАДов без согласования со специалистом не допускается.
Болевой синдром. Многие пациенты после холецистэктомии жалуются на боли в области печени. Этот орган лишен нервных окончаний, поэтому дискомфорт связан с операцией. Если боль не проходит, это может свидетельствовать о развитии постхолецистэктомического синдрома, или ПХЭС. Такое состояние вызвано нарушением работы билиарной системы и требует наблюдения у врача.
Помните, что даже после удаления желчного пузыря возможно образование новых камней в протоках, поскольку изначально эта проблема связана с изменением физико-химических свойств желчи. Для того чтобы не допустить осложнений, пациенту необходимо пересмотреть особенности питания и образа жизни, только в этом случае ситуацию можно взять под контроль и добиться улучшения самочувствия.
ПХЭС: к чему быть готовым после удаления желчного пузыря?
Постхолецистэктомический синдром (ПХЭС) – явление не самое распространённое в гастроэнтерологии. Принято считать, что ПХЭС относится к группе заболеваний желчного пузыря. В действительности это даже не болезнь, а собирательное название комплекса симптомов, которые проявляются сразу или вскоре после операций на желчные протоки или удаления (резекции) желчного пузыря.
Симптомы постхолецистэктомического синдрома
По своей сути ПХЭС является следствием операции по резекции (удалению) желчного пузыря. Это значит, что после резекции у пациента могут проявиться неприятные симптомы, такие, как:
При ПХЭС возможны и другие симптомы, обусловленные обострившимися болезнями:
Причины развития постхолецистэктомического синдрома
Диагностика постхолицистэктомического синдрома
Сложности в точном определении причин, приведших к развитию ПХЭС, и размытость самого определения синдрома требуют тщательного обследования пациента. Чтобы правильно выбрать лечение, необходимо четко установить, что привело к появлению ПХЭС.
Вот почему эффективная диагностика постхолицистэктомического синдрома включает сразу несколько методов:
Лечение постхолицистэктомического синдрома
Так как ПХЭС – это не самостоятельное заболевание, лечение синдрома всегда определяется его причинами. Не зная, как правильно лечить постхолицистэктомический синдром, можно лишь усугубить состояние и усилить неприятную симптоматику.
Принципы лечения ПХЭС включают два ключевых момента:
Лечение в основном строится на:
Применение ферментных препаратов при постхолицистэктомическом синдроме
В некоторых случаях ПХЭС может сопровождаться нарушениями со стороны пищеварительной системы. Это связано с тем, что сигналом для выработки желчи и панкреатических ферментов становится приём пищи. Если сигнал не поступает или поступает с перебоями, последующие события также нарушаются. В результате пища не обрабатывает должным образом, и организм недополучает полезные вещества. Это может сказываться на общем состоянии организма и проявляться тяжестью после еды, дискомфортом, вздутием или диареей.
Постхолецистэктомический синдром
Постхолецистэктомический синдром (ПХЭС) — состояние после операции удаления желчного пузыря (холецистэктомии) по поводу хронического калькулезного холецистита. ПХЭС — это условное обозначение различных нарушений, повторяющихся болей и диспепсических проявлений, которые возникают у больных после холецистэктомии.
Постхолецистэктомический синдром. Причины
Функциональные нарушения сфинктерного аппарата желчевыводящих путей
В настоящее время считается доказанным факт, что после удаления желчного пузыря наблюдается повышение тонуса сфинктера Одди, причиной которого является исключение регулирующей роли сфинктера желчного пузыря и мышечной активности желчного пузыря на сфинктер Одди.
После удаления желчного пузыря включаются механизмы приспособления к работе желчевыводящих путей без желчного пузыря. Изменение моторной функции сфинктера Одди является одной из причин формирования острой или хронической боли в животе и диспепсического синдрома в послеоперационном периоде. Перестройка работы желчевыводящих путей после холецистэктомии может продолжаться до 1 года после операции.
Дисфункция сфинктера общего желчного протока и других сфинктеров желчевыводящей системы может приводить к повышению давления в протоках, застою желчи в них, что проявляется болями в правом подреберье или в подложечной области. Если преобладает дисфункция панкреатического протока, то появляется клиническая картина, характерная для панкреатита.
Разнообразие клинических проявлений ПХЭС затрудняет не только определение типа функциональных нарушений сфинктерного аппарата желчевыводящей системы, но затрудняет диагностику ПХЭС.
Нарушения печени, поджелудочной железы и кишечного тракта после холецистэктомии
Удаление желчного пузыря перестраивает процессы желчеобразования и желчевыделения.
Вследствие этого, обострения хронического панкреатита после удаления желчного пузыря встречаются достаточно часто — от 5 до 90 %. Такой разброс объясняется тем, что до операции не проведено достаточное обследование для оценки состояния поджелудочной железы, но в ряде случаев имеет место гипердиагностика хронического панкреатита.
В медицинской практике отмечается, что чем дольше существуют камни в желчном пузыре, тем чаще возникает хронический панкреатит.
В поджелудочной железе снижается объем секреции ферментов, развивается внешнесекреторная недостаточность функции поджелудочной железы, нарушаются процессы пищеварения. Холецистоэктомия, вовремя проведенная, способствует улучшению или нормализации показателей ферментативной функции поджелудочной железы.
После удаления желчного пузыря нередко нарушается функция 12-перстной кишки, что подтверждается появлением дуоденогастрального рефлюкса, т.е., заброс содержимого 12-перстной кишки в желудок, и вызывающего морфологические изменения в выходном отделе желудка и формирование хронического рефлюкс-гастрита (желчного).
После удаления желчного пузыря нарушается функция тонкой кишки (всасывания пищевых компонентов) и моторная функция толстой кишки (запоры, поносы).
Постхолецистэктомический синдром. Диагностика
Диагностика направлена на выявление различных заболеваний желудочно-кишечного тракта, которые пациент имел до операции, возникших после операции, возможные послеоперационные осложнения.
Диагноз устанавливается на основе:
Постхолецистэктомический синдром. Лечение и профилактика
В раннем послеоперационном периоде большое значение имеет лечебное питание, которое предусматривает часто дробное питание до 6 раз в день, небольшими порциями с ограничением жиров до 60-70 г в сутки.
С целью более быстрой адаптации пищеварительной системы к новым физиологическим условиям – функционирование без желчного пузыря, с учетом сопутствующих болезней рекомендуется более раннее расширение питания близкого к рациональному.
Постхолецистэктомический синдром. Лекарственная терапия по показаниям
С целью улучшения качества желчи, продуцируемой печенью, назначакются препараты урсодезоксихолевой кислоты (Урсосан, Урсофальк, Урсодез, Ливодекса, Эксхол, Холудексан, Урсодокса и др.). Доза продолжительность приема препарата определяется лечащим врачом.
Для связывания избытка желчи в кишечник и особенно наличие холагенной диареи назначаются сорбенты (Смекта) и антациды (Фосфалюгель, Маалокс, Алььагел и др.) по 1 пакету 3-4 раза в день через 1 час после еды в течение 7- 14 дней, режим приема и продолжительность определяется индивидуально.
При наличии боли в верхних отделах живота назначаются спазмолитики (например, Дюспаталин по 1 капсуле 2 раза в день, Дицетел по 50-100 мг 3 раза в день в течение 2-4 недель).
При наличии дуоденита, папиллита, появлении условно-патогенной флоры в посевах кала проводится 7-дневный курс антибактериальных препаратов. Препаратами выбора могут быть Эрцефурил, Интетрикс, Фуразолидон и др., реже антибиотики в общепринятых дозах.
При наличии сопутствующей патологии (панкреатит и др.) по показаниям назначаются ферментные препараты (Панкреатин, Мезим форте, Креон и др.).
Постхолецистэктомический синдром. Профилактика
Профилактика ПХЭС начинается уже в процессе подготовки к операции с целью выявления и своевременного лечения заболеваний гепатопанкреатодуоденальной зоны (заболеваний печени, панкреатита, дуоденита и эрозивно-язвенного процесса в 12-перстной кишке).
Особенно врача беспокоит состояние поджелудочной железы, и если до операции выявлен хронический панкреатит, необходимо провести курс лечения (антисекреторные препараты, спазмолитики, ферментные препараты, препараты урсодезоксихолевой кислоты). Эти мероприятия снижают риск возникновения обострений панкреатита в послеоперационный период в 2.5-3 раза.
Реабилитация
Опыт показывает, что признаки постхолецитэктомического синдрома чаще возникают в первый год наблюдения в период адаптации пищеварительного тракта в новых анатомических условиях.
Через 3-6 месяцев, хотя в настоящее время имеются сведении об успешном применении минеральных вод низкой минерализации после 10 дня после операции, показан прием минеральных вод, оптимальнее в условиях гастроэнтерологического питьевого курорта (Железноводск, Кашин, Дорохово, Карловы Вары и др.) с повторением курса минеральной воды в домашних условиях через полгода.
Диспансерное наблюдение пациентов проводится в течение первого года после операции.
Постхолецистэктомический синдром: диагностика и лечение
Желчнокаменная болезнь (ЖКБ) чрезвычайно распространена в цивилизованных странах, в том числе и в России. Особенно высока заболеваемость среди женщин в возрасте 35–40 лет и старше. ЖКБ характеризуется образованием желчных
Желчнокаменная болезнь (ЖКБ) чрезвычайно распространена в цивилизованных странах, в том числе и в России. Особенно высока заболеваемость среди женщин в возрасте 35–40 лет и старше. ЖКБ характеризуется образованием желчных камней в билиарной системе, главным образом в желчном пузыре, и осложнениями, возникающими в связи с прогрессированием патологического процесса.
Основным методом лечения данного заболевания является холецистэктомия. У 25% перенесших холецистэктомию больных или сохраняются, или через некоторое время появляются абдоминальные боли и диспепсические расстройства, требующие лечения. Адекватная терапия больных зависит от правильного понимания патогенеза клинических симптомов, развивающихся после холецистэктомии. Особенности их формирования связаны, с одной стороны, с нарушениями в обмене холестерина, присущими желчнокаменной болезни, с другой — тем обстоятельством, что патологический процесс протекает в новых анатомо-физиологических условиях, т. е. при отсутствии желчного пузыря.
Известно, что удаление желчного пузыря по поводу калькулезного холецистита не избавляет больных от обменных нарушений, в том числе от печеночно-клеточной дисхолии, которая сохраняется и после операции. У большинства больных после холецистэктомии определяется литогенная желчь с низким холатохолестериновым коэффициентом. Выпадение физиологической роли желчного пузыря, а именно концентрация желчи в межпищеварительный период и выброс ее в двенадцатиперстную кишку во время еды, сопровождается нарушением пассажа желчи в кишечник и расстройством пищеварения. Изменение химического состава желчи и хаотическое ее поступление в двенадцатиперстную кишку нарушают переваривание и всасывание жира и других веществ липидной природы, уменьшают бактерицидность дуоденального содержимого, что приводит к микробному обсеменению двенадцатиперстной кишки, ослаблению роста и функционирования нормальной кишечной микрофлоры, расстройству печеночно-кишечной циркуляции и снижению общего пула желчных кислот. Под влиянием микрофлоры желчные кислоты подвергаются преждевременной деконъюгации, что сопровождается повреждением слизистой оболочки двенадцатиперстной, тонкой и толстой кишки с развитием дуоденита, рефлюкс-гастрита, энтерита и колита. Дуоденит сопровождается дуоденальной дискинезией и, в первую очередь, дуоденальной гипертензией с развитием дуодено-гастральных рефлюксов и забросом содержимого в общий желчный проток и проток поджелудочной железы.
В результате формируются дискинезии сфинктера печеночно-поджелудочной ампулы, желчного и панкреатического протоков (сфинктера Одди), а деконъюгированные желчные кислоты обусловливают развитие диареи. Таким образом, у больных с удаленным желчным пузырем имеющиеся клинические проявления могут быть связаны с изменением химического состава желчи, нарушенным пассажем ее в двенадцатиперстную кишку, дискинезией сфинктера Одди, а также с избыточным бактериальным ростом в кишечнике, синдромами мальдигестии и мальабсорбции, дуоденитом и другими патологическими нарушениями в системе пищеварения. Кроме того, у ряда больных могут сохраняться или развиваться вновь органические препятствия для оттока желчи, связанные с проведенной холецистэктомией. Патологические состояния, которые наблюдаются у больных после холецистэктомии, можно разделить на 3 группы.
В настоящее время термином «постхолецистэктомический синдром» принято обозначать только дисфункцию сфинктера Одди, обусловленную нарушением его сократительной функции и препятствующую нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий. При этом предлагается, вместо принятых ранее определений «постхолецистэктомический синдром», «билиарная дискинезия» и др., использовать термин «дисфункция сфинктера Одди».
Клинические проявления дисфункции сфинктера Одди зависят, в первую очередь, от вовлечения в процесс той или иной его структуры. При изолированной дисфункции сфинктера холедоха развиваются билиарные, при преимущественном вовлечении в процесс сфинктера панкреатического протока — панкреатические, а при патологии общего сфинктера — сочетанные билиарно-панкреатические боли. Для дисфункции сфинктера Одди характерны рецидивирующие приступы сильных или умеренных болей продолжительностью 20 и более минут, повторяющиеся в течение 3 и более месяцев. При билиарном типе боль локализуется в эпигастрии или правом подреберье с иррадиацией в спину и правую лопатку, при панкреатическом типе — в левом подреберье с иррадиацией в спину уменьшающаяся при наклоне вперед, при сочетанном типе — имеет опоясывающий характер. Боль может сочетаться со следующими признаками: а) начало после приема пищи; б) появление в ночные часы; в) тошнота и/или рвота.
Однако оценка только клинических симптомов недостаточна для исключения органической патологии билиарной системы. С этой целью используются ряд скрининговых и уточняющих методов (табл.).
Неинвазивные методы, позволяющие предположить дисфункцию сфинктера Одди, включают определение в крови уровня билирубина, щелочной фосфатазы, аминотрансфераз, амилазы и липазы. Лабораторные исследования необходимо проводить во время или не позднее 6 ч после окончания болевого приступа, а также в динамике. Транзиторное повышение в 2 и более раз уровня печеночных или панкреатических ферментов в период не менее чем при 2 последовательных приступах болей является важным в подтверждении дисфункции сфинктера Одди.
Аналогичное значение имеет провокационный морфино-простигминовый тест, когда парентеральное введение препаратов провоцирует развитие болевого приступа, чаще смешанного билиарно-панкреатического типа в сочетании с повышением в крови уровня аминотрансфераз, щелочной фосфатазы, панкреатических ферментов. Однако диагностическая ценность данного теста ограничена его низкой чувствительностью и специфичностью.
При УЗИ важное значение придается расширению холедоха и главного панкреатического протока, которое свидетельствует о нарушении тока желчи и панкреатического секрета на уровне сфинктера Одди. В то же время у 3-4% больных, перенесших холецистэктомию и не имеющих симптомов, отмечается расширение общего желчного протока. Определенное значение имеет ультразвуковое исследование диаметра общего желчного протока с использованием жирных завтраков, стимулирующих выработку эндогенного холецистокинина и увеличивающих холерез. После пробного завтрака измерение диаметра холедоха проводится каждые 15 мин в течение 1 ч. Увеличение его диаметра на 2 мм и более по сравнению с исходным позволяет предположить наличие неполной обтурации холедоха как в результате дисфункции сфинктера Одди, так и из-за органической патологии билиарной системы.
Для оценки состояния панкреатических протоков используется проба с введением секретина в дозе 1 мг/кг. В норме после стимуляции панкреатической секреции секретином при УЗИ отмечается расширение панкреатического протока в течение 30 мин с последующим его уменьшением до исходного уровня. Если проток остается расширенным более 30 мин, это свидетельствует о нарушении его проходимости.
При билисцинтиграфии о наличии дисфункции сфинктера Одди свидетельствует увеличение времени транзита радиофармпрепарата от ворот печени до двенадцатиперстной кишки, при этом оно пропорционально уровню базального давления сфинктера Одди. В то же время при расширенном холедохе данное исследование малоинформативно для оценки функции сфинктера Одди.
К инвазивным методам оценки функции сфинктера Одди относится непрямой способ — эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ). Косвенными признаками повышения тонуса сфинктера Одди являются диаметр холедоха более 12 мм, задержка контраста в холедохе свыше 45 мин. О дисфункции сфинктера главного панкреатического протока свидетельствуют расширение последнего до более чем 5 мм и замедление эвакуации контраста из его просвета. Однако аналогичные изменения могут наблюдаться и при наличии органической патологии.
Наиболее точным методом, подтверждающим дисфункцию сфинктера Одди, является манометрия. При этом возможно канюлирование раздельно холедоха и вирсунгова протока с проведением манометрии их сфинктеров, что позволяет выделить преимущественно билиарный или панкреатический тип расстройств, а также установить этиологию рецидивирующих панкреатитов у больных, перенесших холецистэктомию и папиллотомию. Признаками дисфункции сфинктера Одди при манометрическом исследовании являются:
Манометрия сфинктера Одди показана далеко не всем больным. Выбор данного исследования основывается на оценке тяжести клинических проявлений и эффективности консервативной терапии.
Таким образом, предположить, что речь идет о дисфункции сфинктера Одди можно в следующих ситуациях:
Примерные формулировки диагнозов у больных, перенесших холецистэктомию:
Диагноз: желчнокаменная болезнь, холецистэктомия в 1994 г. (для случаев, при которых отсутствуют клинические симптомы).
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1999 г.
Диагноз: хронический рецидивирующий (обструктивный) панкреатит с внешнесекреторной и инкреторной недостаточностью в фазе обострения.
Сопутствующее заболевание: желчнокаменная болезнь, холецистэктомия в 1994 г.
Диагноз: синдром раздраженного кишечника с преобладанием запоров в фазе обострения.
Сопутствующий диагноз: желчнокаменная болезнь, холецистэктомия в 1994 г.
Ведение больных, перенесших холецистэктомию. Цель лечения: восстановить нормальное поступление желчи и панкреатического секрета из билиарных и панкреатических протоков в двенадцатиперстную кишку. Задачи лечения: нормализовать химический состав желчи; восстановить проходимость сфинктера Одди; восстановить нормальный состав кишечной микрофлоры; нормализовать процессы пищеварения и моторику тонкой кишки для профилактики дуоденальной гипертензии.
Для профилактики образования желчных сладжей или камней во внепеченочной билиарной системе рекомендуется:
Медикаментозное лечение дисфункции сфинктера Одди направлено на снятие спазма гладкой мускулатуры последнего. С этой целью используется ряд препаратов, обладающих спазмолитическим эффектом. Нитраты: нитроглицерин используется с целью быстрого купирования болей, нитросорбит — для курсового лечения. Механизм действия нитратов сводится к образованию в гладких мышцах свободных радикалов оксида азота (NO), которые активируют гуамилатциклазу и увеличивают содержание цГМФ, что приводит к их расслаблению. Однако выраженные кардиоваскулярные эффекты, побочные действия и развитие толерантности делают их малоприемлемыми для длительной терапии дисфункции сфинктера Одди.
Антихолинергические средства блокируют мускариновые рецепторы на постсинаптических мембранах органов-мишеней. В результате происходит блокада кальциевых каналов, прекращается вход ионов кальция в цитоплазму гладкомышечных клеток и, как следствие, достигается снятие мышечного спазма. В качестве спазмолитиков используются как неселективные (препараты красавки, метацин, платифиллин, бускопан и др.), так и селективные М-холиноблокаторы (гастроцепин и др.). Однако при приеме препаратов данной группы может наблюдаться достаточно широкий спектр побочных эффектов: сухость во рту, задержка мочеиспускания, нарушения зрения, повышение внутриглазного давления, тахикардия, запоры, сонливость. Сочетание довольно низкой эффективности с широким спектром побочных действий ограничивает применение препаратов этой группы при дисфункции сфинктера Одди.
Блокаторы медленных кальциевых каналов — фенилалкиламины (верапамил, галлопамил), 1,4-дигидроперидины (нифедипин, амлодипин) и бензотиазепины (дилтиазем и др.) закрывают кальциевые («медленные») каналы клеточных мембран, препятствуют входу ионов кальция в цитоплазму клеток гладкой мускулатуры и вызывают ее релаксацию. Препараты обладают многочисленными кардиоваскулярными эффектами, в первую очередь вазодилатирующими, в связи с чем не нашли широкого применения при лечении дисфункции сфинктера Одди. Имеются лишь единичные публикации по использованию нифедипина при дисфункции сфинктера Одди, и целесообразность их применения требует дальнейшего изучения.
Миотропные спазмолитики, механизм действия которых сводится к ингибированию фосфодиэстеразы, или к активации аденилатциклазы, или к блокаде аденозиновых рецепторов, что приводит к снижению тонуса и двигательной активности гладкой мускулатуры. Представителями данной группы препаратов являются дротаверин (но-шпа, но-шпа форте), бенциклан (галидор), дицикловерин (триган-Д), альверин (метеоспазмил) и др.
Основными недостатками препаратов всех вышеуказанных групп являются:
В отличие от них, гимекромон (одестон) обладает избирательным спазмолитическим действием на сфинктер Одди и сфинктер желчного пузыря. Кроме того, препарат не повышает давление в желчных путях, не оказывает влияния на секреторную функцию пищеварительных желез и процессы кишечной абсорбции.
В восстановлении нормального оттока желчи при отсутствии желчного пузыря, наряду с проходимостью сфинктера Одди, большое значение имеет уровень давления в двенадцатиперстной кишке. Если он превышает секреторное давление желчи и панкреатического сока, они будут депонироваться в билиарных и панкреатических протоках с соответствующими последствиями.
В связи с этим разрешение дуоденальной гипертензии считается непременным условием ведения больных с дисфункцией сфинктера Одди. При выборе тактики лечения следует учитывать, что основным патогенетическим механизмом развития дуоденальной гипертензии является избыточное содержание жидкости и газа в просвете двенадцатиперстной кишки в результате бродильно-гнилостных процессов, обусловленных микробной контаминацией.
Для деконтаминации двенадцатиперстной кишки проводятся 1-2 семидневных курса антибактериальной терапии со сменой препарата при очередном курсовом лечении. Препаратами выбора являются: доксициклин 0,1 г 2 раза в день, тетрациклин 0,25 г 4 раза в день, бисептол 960 мг 2 раза в день, фуразолидон 0,1 г 3 раза в день, эрсефурил 0,2 г 4 раза в день, ципрофлоксацин 250 мг 2 раза в день, метронидазол 0,25 г 4 раза в день, интетрикс 1 капсула 4 раза в сутки, реже — левомицетин 0,25 г 4 раза в день.
Подбор лекарственных средств проводится, как правило, эмпирически. При выраженных симптомах диспепсии назначаются сразу 2 препарата, один из которых должен действовать преимущественно на анаэробную микрофлору (например, метронидазол). Одновременно с приемом кишечных антисептиков в ряде случаев назначаются пребиотики: при наличии поносов — хилак форте 60 капель 3 раза в день в течение 1 нед, затем по 30 капель 3 раза в день в течение 2 нед; в случаях преобладания запоров — лактулоза по 1-2 столовые ложки 1 раз в день до нормализации стула.
После окончания антибактериальной терапии показаны пробиотики (препараты, содержащие нормальные штаммы кишечной флоры). Одним из известных представителей группы пробиотиков является бифиформ, содержащий в одной капсуле, покрытой энтерорастворимой оболочкой, энтерококки 107, бифидумбактерии 107 и питательную среду, способствующую их росту в тонкой и толстой кишке. Назначается препарат по 1 капсуле 2 раза в день в течение 2 нед. В комплексе с антибактериальными средствами необходимо назначать алюминийсодержащие буферные антациды (алюгастрин, алюмаг, маалокс, фосфалюгель, смекта и др.). Любой из препаратов принимается по 1 дозе через 1 ч после завтрака, обеда и ужина и перед сном (не сочетаются с хилаком форте). Продолжительность лечения составляет 5–7 дней. Целесообразность использования данных препаратов обусловлена следующими их способностями:
Наличие у большинства больных относительной ферментной недостаточности в результате разрушения пищеварительных ферментов дуоденальной и тонкокишечной микрофлорой, снижения интрадуоденального уровня рН, а также нарушения процесса смешивания их с пищевым химусом является обоснованием назначения ферментных препаратов. При склонности к поносам назначаются препараты панкреатина: мезим форте, креон, ликреаза, панцитрат и другие по 1 дозе 2-3 раза в день в начале еды; при склонности к запорам — комбинированные средства, содержащие панкреатин, желчные кислоты, гемицеллюлозу: фестал, энзистал, дигестал по 1 драже 2-3 раза в день в конце приема еды. Продолжительность лечения индивидуальна и, как правило, не превышает 10 дней.
Приведем ориентировочные схемы ведения больных с дисфункцией сфинктера Одди.
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1996 г.
Диагноз: дисфункция сфинктера Одди билиарного типа. Желчнокаменная болезнь, холецистэктомия в 1989 г. Сопутствующие заболевания: хронический катаральный, преимущественно дистальный дуоденит. Синдром избыточного бактериального роста в тонкой кишке.
Таким образом, своевременная и правильная оценка клинической симптоматики, развивающейся у больных после операции холецистэктомии, дает возможность подобрать адекватную терапию и в результате существенно улучшить качество жизни пациентов с заболеваниями гепатобилиарной системы.
По вопросам литературы обращайтесь в редакцию.
П. Я. Григорьев, доктор медицинских наук, профессор, Э. П. Яковенко, доктор медицинских наук, профессор
Н. А. Агафонова, кандидат медицинских наук, А. С. Прянишникова, кандидат медицинских наук
И. П. Солуянова, кандидат медицинских наук, З. В. Бекузарова, А. В. Яковенко, кандидат медицинских наук
РГМУ, Москва