Названы 10 причин отсутствия антител после вакцины от коронавируса
Не всегда это повод для волнения
Если раньше после прививок никто из нас не бежал делать тесты для подтверждения формирования антител к тому или иному вирусу, то сейчас все поменялось. Сдача анализов после вакцинации от COVID-19 уже вошло в привычку. А жалобы на отсутствие антител после стали встречаться все чаще. Мы проконсультировались со специалистами в группе Watching COVID-19 в социальной сети и узнали, всегда ли появляются антитела и стоит ли волноваться, если их нет после прививки от коронавируса.
Первая (самая вероятная) причина – вы сделали не тот тест. Имейте в виду, что многие лаборатории делают тексты на белок нуклеокапсид – они более информативны для переболевших, а не для привитых. Тесты после вакцинации нужно сдавать не на любые антитела к коронавирусу, а на нейтрализующие, то есть, на S-белок (уточните этот момент в лаборатории). Кроме того, можно пересдать тест в другой лаборатории. Уже немало примеров, когда в одной лаборатории тесты показывают отсутствие антител, а в другой – их огромное количество.
Вторая. Антитела могут появиться не сразу, а через какое-то время. Кроме того, титр антител может колебаться – сегодня их много, а завтра они не определяются в крови. Нужно просто немного подождать – и потом пересдать тест заново.
Третья. Если тест не показывает антител после вакцинации прививкой на аденовирусных векторах (таких в мире несколько), это может означать, что, возможно, что у привившегося есть иммунитет к используемым аденовирусам-носителям, которые доставляют белок коронавируса в клетку. И аденовирусы уничтожаются, не успев попасть в клетки и выработать защитный спайк-белок. В этом случае хорошо бы проверить наличие иммунитета к используемым аденовирусам лабораторными тестами и, если он есть, сделать другую вакцину (на других векторах или вообще на другой платформе).
Четвертая. Даже отсутствие антител после всех анализов не исключает наличия клеточного иммунитета после вакцинации. Исследования на Т-клеточный иммунитет в России проводятся в нескольких лабораториях и стоят довольно дорого, что делает эти тесты не очень доступными.
Пятая. Прием некоторых препаратов мешает выработке антител на фоне вакцинации. К ним относятся, например, кортикостероиды, цитостатики, а также биологическая иммуносупрессивная терапия.
Шестая. При некоторых заболеваниях антител к коронавирусу после вакцинации не образуется. Речь идет о довольно серьезных патологиях: ВИЧ, лимфолейкоз.
Седьмая. Это – целый спектр причин, которые можно объединить в условную группу «образ жизни». Например, дефицит тех или иных микроэлементов в организме (прежде всего, у веганов); злоупотребление спиртным; стресс; изматывающие физические нагрузки уровня марафона.
Восьмая. Антител выработалось настолько мало, что тесты их не улавливают или показывают нижнюю границу нормы. Но! Сегодня никто не знает, какое количество антител может защитить от болезни – возможно, даже микроскопическое. «Нарастить» количество антител, как показывает практика, иногда можно после повторной вакцинации.
Девятая. Отсутствие антител после вакцинации может быть связано с индивидуальными особенностями лимфоцитов пациента. Разнообразие рецепторов лимфоцитов, которые потенциально смогут узнать чужеродные белки, появляется в результате процесса рекомбинации ДНК. Так возникает пул клеток с самыми разными рецепторами. Чтобы иммунный ответ возник, нужен хотя бы один, а на самом деле несколько лимфоцитов, рецепторы которых узнали бы чужака. И у малого процента людей оказывается, что среди всего разнообразия лимфоцитов нет таких, которые узнали бы COVID-19 и стали бы размножаться, дифференцироваться и производить антитела. Поскольку рекомбинация идет как случайная рулетка, то можно сказать, что человеку просто не повезло.
Таких людей, по официальным данным, не более 2%. Антитела у них не появляются ни после болезни, ни в ответ на прививку. В этом случае остается одно – ждать коллективного иммунитета.
Десятая. Проблемы с иммунным статусом. Врачи отмечают, что в редких случаях, когда несколько разных тестов на протяжении пары месяцев показывают полное отсутствие антител после вакцины, не мешает сдать общий анализ крови с лейкоцитарной формулой и обратиться к иммунологу.
А иные вирусологи советуют вообще не беспокоиться и не тратиться на исследования антител после прививки. По их мнению защита будет вам обеспечена в любом случае.
«После вакцинации нет антител»: врач объяснил проблему
Что делать тем, кто привился от коронавируса и недоволен своим анализом
С 28 июня столичные рестораны и кафе объявляются COVID-free. Посещать их смогут только посетители, прошедшие вакцинацию, переболевшие COVID-19 в течение последних шести месяцев либо имеющие отрицательный ПЦР-тест, действительный в течение трех дней. Все это должно стимулировать людей скорее вакцинироваться.
Ну а среди свежевакцинированных крайне популярны тесты на антитела. Такого ажиотажа с их измерением не было никогда. Вряд ли кто-то из россиян знает уровни антител после прививки от кори или черной оспы, а вот свои антитела к коронавирусу пристально изучают все.
Каждый провакцинированный считает своим долгом непременно пойти в лабораторию и сдать тест на антитела. Но иногда обнаруживается, что их нет. И начинаются паника, истерика и разочарования. Защиты нет, вакцина не работает, все кончено. Но всегда ли антитела говорят об иммунитете? Как понять, защитила ли вас вакцина, и что делать, если этого все же не произошло? Ситуацию проанализировал «МК».
Москвичка Тамара рассказывает, что ее 76-летняя мама сдала тест на антитела, как и положено, через 42 дня после вакцинации. Каково же было ее удивление, когда тест показал уровень защиты ниже пороговых значений. «Вакцину мама перенесла хорошо, без побочных. Но получается, что она была для нее бесполезна?» — недоумевает Тамара.
Однако еще через месяц вдруг случилось чудо — новый тест в другой лаборатории показал положительный результат. «Ничего не понимаю, — недоумевает дочь. — Получается, что вакцина все же работает?»
С такими ситуациями сегодня, по статистике различных экспертных источников (групп вакцинированных, лабораторных специалистов и пр.), сталкиваются в среднем от 3% до 10% привитых. Какие могут быть причины?
Первая — она же самая распространенная. Вы сделали неправильный анализ. Поскольку вакцины ведут к выработке антител к шиповидному белку вируса (S-белку), в лабораториях нужно искать тесты, которые диагностируют антитела именно к S-белку. Если же вы сдадите тест к нуклеотидному белку (N-белку) коронавируса, это будет бессмысленно. А возможно, в лаборатории просто ошиблись (эксперты рассказывают, что иногда сданная на анализы кровь сворачивается и лаборанты платных клиник пишут просто норму, чтобы не возвращать деньги или не переделывать еще раз бесплатно анализ). «Только в РФ свыше 200 наименований антительных тестов, большинство из которых по большому счету непонятно что измеряют. Поэтому к выбору теста надо подходить предельно внимательно», — говорит врач-терапевт амбулаторного звена, который «провел» более трехсот пациентов с коронавирусом, Игорь Соколов.
Вторая причина ведет к тому же выводу, что и первая, — тест нужно пересдать. Но не потому, что вы выбрали неправильную тест-систему, а потому, что антитела у вас еще не успели выработаться. У некоторых людей (особенно пожилых) процесс формирования иммунной защиты может занять больше времени, чем ожидается, то есть не 42 дня, а, например, 60–70.
Третье. Если вы делали вакцину на аденовирусных векторах (на них в клетку доставляется материал коронавируса), нельзя исключить, что у вас есть иммунитет к какому-то из аденовирусов, из которых сформированы векторы вакцины. Организм распознает его на подступах к клетке, поэтому иммунной защиты от SarsCov2 сформировано не будет. Узнать о том, есть ли у вас иммунитет к аденовирусам, можно, но сложно: такие тесты делают далеко не во всех лабораториях. В этом смысле молекулярные биологи рекомендуют попробовать ревакцинацию другой вакциной.
Четвертое. Увы, вам могли вколоть препарат, который хранился с нарушениями, например, без выдерживания температурного режима.
Пятое. Причиной может быть прием ряда лекарственных средств, которые препятствуют выработке иммунной защиты при вакцинации. К примеру, это кортикостероиды, цитостатики, а также биологическая иммуносупрессивная терапия.
Шестое. Возможно, у вас есть какое-то заболевание, которое не дает выработаться антителам после вакцинации. К ним относятся вирус иммунодефицита человека и некоторые виды рака крови. Кроме того, могут быть проблемы с иммунным статусом вообще — если антитела не появляются, возможно, стоит навестить врача-иммунолога.
Седьмое. Иногда отсутствие антител в анализе не равно отсутствию их в организме. Просто их спектр настолько низок, что анализаторы не способны их отловить. Хорошая новость в том, что в мире так никто и не знает, какой титр антител можно считать защитным. С другой стороны, уже известны случаи заболевания даже на фоне «запредельных» антител.
Восьмое. Повлиять на формирование иммунной защиты после прививки может и ваше поведение. Система питания, которой вы придерживаетесь, вредные привычки, стрессы, чрезмерные физические нагрузки — все может сыграть свою роль.
Девятое. Самое неприятное — в очень редких случаях встречаются люди, не способные выработать антительный ответ ни на какие прививки. Правда, одновременно они же обладают важным качеством легче справляться с опасными инфекциями. Например, от кори люди с такой особенностью не умирают. Таких людей, по официальным данным, не более 2%. Антитела у них не появляются ни после болезни, ни в ответ на прививку.
Игорь Соколов отмечает, что тема антител после вакцинации сложная и неоднозначная и многих ответов медицина еще не знает. «Так надо ли эти антитела вообще контролировать? — говорит доктор Соколов. — Мнения разделились, одни врачи (особенно западные) улыбаются: а зачем? Другие (многие российские) — что вполне нормально контролировать уровень иммунного ответа. Это вызывает состояние «подвешенности» у обычного, вдумчивого человека. Ведь антитела, даже большие, — не показатель защиты, болеют после вакцинации и с большими антителами, но все же реже, чем с маленькими. Большие антитела — это хорошо, но тоже не всегда. При определенных условиях, возможно, именно они могут способствовать воспалению в легочной ткани».
Говорить о том, что антитела — не показатель иммунного ответа, конечно, нельзя. Но можно говорить о том, что это не единственный показатель. Все уже знают про клеточный иммунитет, который при встрече с вирусом начинает стимулировать гуморальный (выработку антител). Поэтому иногда более важным представляется анализ на клеточный иммунитет, который, увы, у нас малодоступен и стоит очень дорого.
«И все же было бы неправильно говорить, что антитела вообще ни при чем, — продолжает Игорь Соколов. — Существует достаточное количество работ, показывающих, что определенные антитела, определенная их концентрация, предотвращают болезнь. Поэтому определение антител, конечно, даст какую-то информацию об уровне вашей защиты, но вряд ли ее можно назвать полной».
Врач признает, что сейчас многие рекомендации составляются на глазок и вакцинироваться рекомендуют всем, включая переболевших, хотя есть много убедительных работ по формированию защиты после перенесенного заболевания на ближайшие 6–8 месяцев, а может быть, и больше.
Так нужно ли бежать и сдавать антитела после вакцинации? «Мое мнение — делать это не обязательно, но если делаете, получаете ряд преимуществ — можете отследить динамику защиты и, вероятно, разные уровни антител по разным вакцинам, чтобы понимать свою реакцию на них и знать, чем ревакцинироваться в будущем. Количество объективных критериев в этой области растет и далее будет только увеличиваться».
СПРАВКА «МК»
С 28 июня в Москве вступает в силу новый временный порядок посещения заведений общепита. Об этом сообщил в своем блоге мэр Москвы.
Вначале власти города совместно с представителями общепита провели эксперимент по созданию точек, «свободных от ковида», который признали успешным и решили распространить на все рестораны и кафе. Теперь посещать заведения общественного питания смогут только посетители, имеющие защиту от заболевания: прошедшие вакцинацию; переболевшие COVID-19 в течение последних 6 месяцев; либо имеющие отрицательный ПЦР-тест, действительный в течение 3 дней. Пройти ПЦР-тестирование необходимо в одной из лабораторий города Москвы, передающих сведения в систему ЕМИАС.
Наличие защиты от коронавируса подтверждается специальным QR-кодом. Никакие бумажные справки или сертификаты приниматься не будут. Предприятия общественного питания, не выполняющие эти требования, смогут работать только на вынос или доставку.
Опубликованы первые данные по инактивированной вакцине против COVID-19 «КовиВак»
Вступление
Продолжающаяся в настоящее время пандемия новой коронавирусной инфекции 2019 года (COVID-19), вызванная коронавирусом 2 тяжелого острого респираторного синдрома SARS-CoV-2, унесла более 4 миллионов жизней (по данным на март 2021 года [1, 2]), и необходимость быстрого внедрения безопасных и эффективных вакцин против данного вируса остается очень высокой. Беспрецедентное в новейшей истории повсеместное распространение пандемии требует применения всех существующих вакцинных платформ, чтобы в конечном счете обеспечить доступность вакцин против SARS-CoV-2 для жителей каждой страны мира.
SARS-CoV-2 относится к подроду Sarbecovirus рода Betacoronavirus и семейству Coronaviridae [3]; в качестве основного рецептора для проникновения в клетки человека вирус использует ангиотензинпревращающий фермент 2 (АПФ2) [4, 5]. Диаметр заключенного в оболочку вириона SARS-CoV-2 составляет 100–150 нм; сам вирион имеет сферическую форму. В нем содержится несколько структурных белков: шипиковый гликопротеин (S), мембранный белок (M), белок оболочки (E), расположенный на поверхности, и белок нуклеокапсида (N), который связан с РНК внутри вирусной частицы. S-белок представляет собой трансмембранный белок слияния I типа, который во время синтеза подвергается значительному гликозилированию; протеаза хозяина расщепляет его на два фрагмента — S1 и S2. Фрагмент S1 содержит рецептор-связывающий домен (РСД), который взаимодействует с рецептором клетки хозяина (т.е. АПФ2). Фрагмент S2 необходим для слияния мембран после еще одного расщепления протеазами клетки хозяина и дальнейших структурных перестроек [6]. Благодаря этим свойствам шипиковый белок и его РСД являются основными мишенями для нейтрализующих антител организма хозяина (НАт) в процессе развития иммунного ответа [7].
Иммунный ответ на инфекцию SARS-CoV-2 активно изучается с целью разработки и улучшения как диагностики заболевания, так и создания и совершенствования вакцин. Как было выявлено в ходе экспериментов, титры НАт являются одними из основных маркеров защиты от SARS-CoV-2, поскольку адоптивный перенос очищенных IgG, которые были получены от выздоравливающих макак-резусов, дозозависимо способствовал формированию иммунной защиты от заражения SARS-CoV-2 у наивных макак-реципиентов [8]. Легкая или средняя степень тяжести течения COVID-19 приводит к выработке НАт, концентрация которых коррелирует с титрами IgG к РСД, определенными методом ELISA; данные титры НАт сохраняются примерно от двух-трех [9, 10] до пяти месяцев [11]. Учитывая возможность снижения концентраций антител после заражения, пристально исследуется более трудный для изучения клеточный компонент иммунитета.
Для разработки вакцин против COVID-19 тестируются многочисленные методы. В настоящее время наиболее часто применяются инактивированные вирусные векторные вакцины, вакцины на основе нуклеиновых кислот (РНК, ДНК) и белковые (субъединичные, вирусоподобные (ВПВ)) вакцины [12]. В качестве основных антигенов, вызывающих синтез НАт, в большинстве вакцин используются S-белок и РСД. Различные передовые технологии разработки вакцин уже продемонстрировали свой потенциал в плане предотвращения развития COVID-19, и несколько таких препаратов, таких как вакцины на основе мРНК и аденовирусные векторные вакцины, после успешного завершения клинических испытаний были одобрены для использования по всему миру [13, 14]. Тем не менее, разработка инактивированных вакцин как более традиционный метод является надежным и экономичным способом, имеющим долгую и успешную историю применения [15, 16]. В Центре Чумакова на культуре клеток Vero были успешно разработаны две инактивированные вакцины против клещевого энцефалита и полиомиелита [22, 23]. Таким образом, вакцина против COVID-19 создавалась на основе ранее отработанной платформы для культивирования клеток с использованием уже отлаженных методов.
Во всем мире разрабатывается несколько инактивированных вакцин против инфекции SARS-CoV-2, и по крайней мере пять из них успешно прошли доклинические и клинические испытания, и их применение было одобрено [17–20]. Тем не менее, несмотря на множество высококачественных публикаций о клинических испытаниях различных вакцин, подробных сведений об общей токсичности, репродуктивной токсичности, профилактической эффективности, иммуногенности и устойчивости иммунного ответа на животных моделях крайне мало.
В данной работе авторы провели оценку безопасности, иммуногенности и устойчивости иммунного ответа на вакцину «КовиВак», созданную на основе цельного вириона, инактивированного β-пропиолактоном, у грызунов и нечеловеческих приматов. У исследованных видов животных не было обнаружено признаков острой/хронической, репродуктивной, эмбрио- и фетотоксичности, тератогенного действия, а также аллергенных свойств. Вакцина привела к формированию стабильного и сильного гуморального иммунного ответа как в виде специфических IgG к SARS-CoV-2, так и НАт у мышей линии BALB/c, сирийских хомячков и обыкновенных игрунок. В течение года титры НАт существенно не снизились. Профилактическая эффективность вакцины изучалась на сирийских хомячках. Надежность производственного процесса была продемонстрирована путем оценки четырех партий вакцины и сравнения их иммуногенных свойств на мышах.
Результаты
Производство и описание вакцины
Ранее был представлен процесс выделения и генетического описания вакцинного штамма AYDAR-1 [21]. Вирус удалось профильтровать на третьем пассаже и дополнительно очистить путем разбавления. Были созданы первичные, основные и рабочие посевные серии штамма (а именно пассажи под номерами 7, 8 и 9), которые были охарактеризованы в соответствии с национальными руководствами по производству вакцин.
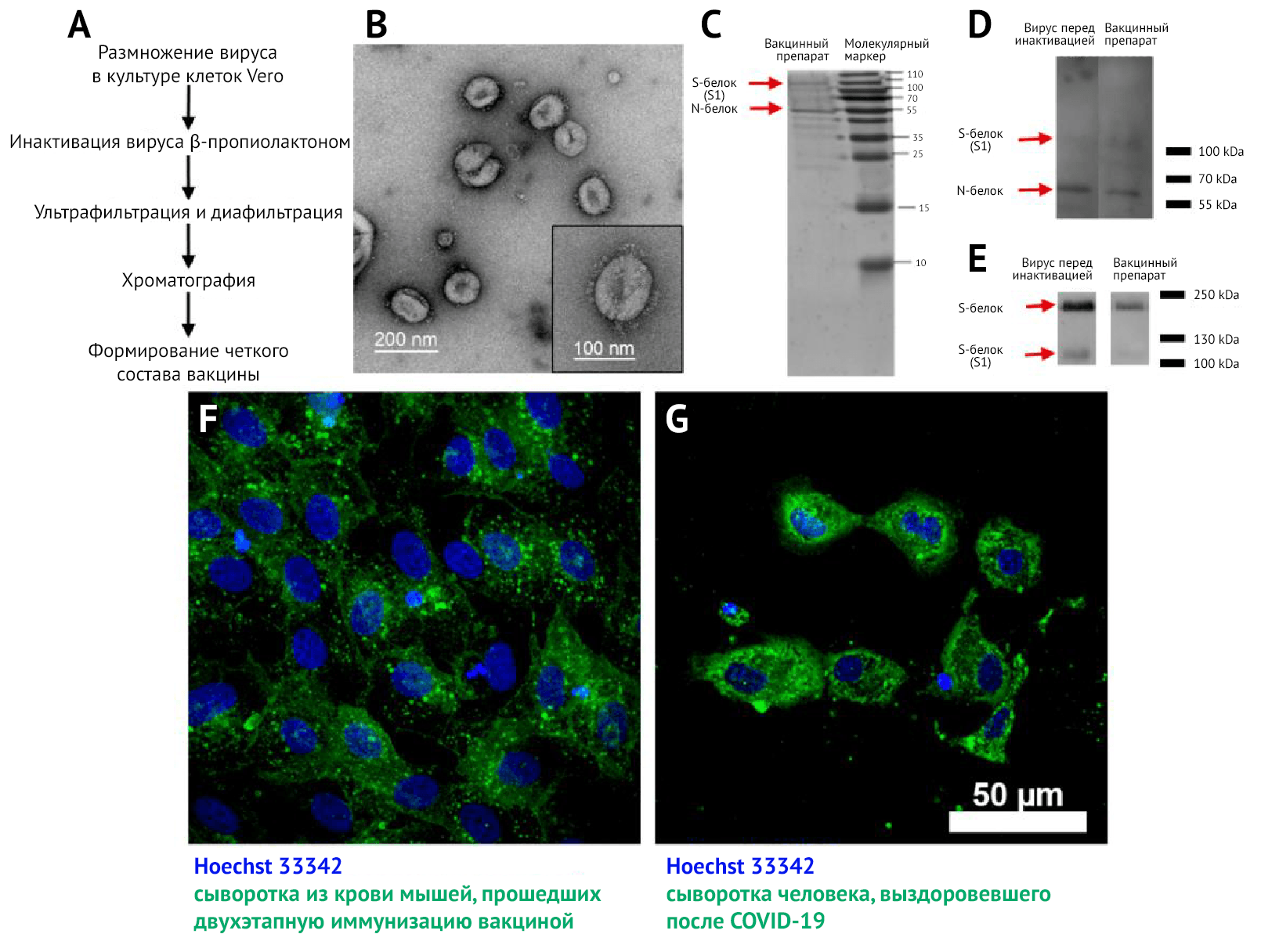
Благодаря трансмиссионной электронной микроскопии (ТЭМ) (рис. 1B) с негативным контрастированием концентратов были обнаружены плеоморфные сферические вирусные частицы диаметром около 120 нм, покрытые шиповидными структурами длиной 16–20 нм.
Методом ТЭМ (рис. 1B) были подтверждены гомогенность и чистота вакцинного препарата и выявлены вирионы с шипиковыми белками, соотносящиеся по форме и размеру с таковыми, выявляемыми в других исследованиях [26, 27].
В ходе электрофореза SDS-PAGE и вестерн-блоттинга (ВБ) концентратов вакцин перед инактивацией и после хроматографии, окрашенных сыворотками реконвалесцентов после COVID-19 (рис. 1 C и D), были выявлены два основных белка в концентратах: N и S, которые должны содержаться и в препарате вириона. С помощью окрашивания сывороткой анти-S-белка (рис. 1E) были обнаружены две формы S-белка в вирусных препаратах до и после инактивации: S1 и полноразмерный S-белок. Это свидетельствует о том, что в вакцинном препарате присутствует антиген-мишень для индукции синтеза НАт.
Специфичность реактивности антител подтверждается отсутствием свечения (флуоресценции) в неинфицированных клетках культуры Vero.
Изучение эмбрио-, фетотоксичности и тератогенных эффектов в антенатальном и постнатальном периодах развития
Беременные крысы линии Wistar (N = 60) были случайным образом распределены в три группы и иммунизированы внутримышечно на 2, 9 и 16 дни беременности. Крысам из первой исследуемой группы вводили одну дозу вакцины (6 мкг/доза; 0,5 мл), из второй — двойную дозу (12 мкг/доза; 1,0 мл), а из третьей контрольной группы — двойную дозу плацебо (1,0 мл). Ежедневно проводилось измерение массы тела и общего физического состояния животных; на поздних сроках беременности с помощью теста «открытое поле» оценивалась исследовательская активность и состояние самок. Прибавка в весе у самок проходила нормально; летальных исходов или признаков интоксикации не наблюдалось. Ни в одной из исследуемых групп не было признаков преждевременных или трудных родов. В тесте «открытое поле» на 18-е сутки беременности все самки крыс продемонстрировали преимущественно сбалансированный тип поведения с умеренной двигательной и поисковой активностью без признаков беспокойства.
Половину (N = 10 из каждой группы) животных в каждой группе умерщвляли на 20-й день беременности. Статистически значимых различий между исследуемыми группами по количеству желтых тел в яичниках, местах имплантации в матке, живым и мертвым плодам не было. Плоды сформировались нормально, топография всех исследованных органов была в пределах анатомической нормы, гистологическое строение соответствовало возрасту эмбрионов, развитие костей было нормальным. Патологических изменений органов и тканей обнаружено не было.
Другая половина (N = 10 из каждой группы) животных в каждой из трех групп вакцинированных была использована для выявления возможных нарушений эмбрионального развития, проявляющихся в постнатальном периоде. За потомством наблюдали в течение 60 дней после рождения. Проводилась оценка общего состояния потомства крыс, выживаемость, прибавка в весе, физическое развитие, сформированность сенсомоторных рефлексов, эмоционально-произвольного поведения и способности точно координировать движения. Соотношение самцов и самок в потомстве во всех группах было практически одинаковым (примерно 1: 1). Во всех исследуемых группах за весь период наблюдения (от рождения до двухмесячного возраста) смертность детенышей не превышала 4 % и достоверно не различалась между группами. В группах не было различий в физическом и неврологическом развитии детенышей крыс, а индивидуально обусловленные значения исследуемых показателей находились в пределах физиологической нормы.
Таким образом, вакцина «КовиВак» не оказала отрицательного влияния на общее состояние беременных крыс. Эмбриотоксических, фетотоксических или тератогенных эффектов обнаружено не было. Вакцинация не привела к увеличению смертности потомства и не повлияла на физическое и психологическое развитие детенышей крыс.
Обсуждение результатов
Безопасность
Существует множество тестов для оценки различных параметров безопасности разрабатываемых вакцин на животных моделях. Авторы выбрали классические модельные объекты для исследования безопасности (мыши, морские свинки, крысы и приматы). Для вакцины «КовиВак» проводилась оценка общей острой токсичности у трех видов (мышей, морских свинок и игрунок), хронической токсичности у двух видов (мышей и морских свинок) и гиперчувствительности у морских свинок. По сравнению с группой плацебо никаких изменений выявлено не было. Все показатели были в пределах физиологической нормы.
Существовали предположения о возможной репродуктивной токсичности вакцинных препаратов, содержащих S-белок SARS-CoV-2. Исходя из данных экспериментов авторов на крысах линии Wistar, был сделан вывод о том, что многократная иммунизация вакциной «КовиВак» до или во время беременности не оказывает отрицательного эффекта на внутриутробное или постнатальное развитие потомства.
Таким образом, вакцина «КовиВак» безопасна и может быть использована в клинических испытаниях на людях.
Иммунитет и его стойкость
Краткосрочная иммуногенность вакцины «КовиВак» была оценена на трех животных моделях (двух генетических линиях мышей, сирийских хомячках и обыкновенных игрунках), иммунизированных разными дозами. Вакцина индуцировала синтез НАт у всех изученных видов. Более того, у мышей были обнаружены антитела к двум основным структурным белкам вируса (S и N). В течение первых 2–4 недель не наблюдалось значительных различий между титрами НАт, синтез которых был вызван различными дозами антигена. Различия проявились начиная с пятой недели после первой иммунизации.
Как было отмечено выше, синтез НАт является одним из основных маркеров защиты от SARS-CoV-2 [8]. Следовательно, длительность антительного ответа (НАт) коррелирует с длительностью защиты. После естественного заражения, особенно в случае легкого течения инфекции, ответ в виде НАт довольно слабый и непродолжительный [11].
Сведений об устойчивости иммунитета, вызванного вакциной, очень мало. Хотя в опубликованных доклинических исследованиях показана индукция титров IgG и НАт к SARS-CoV-2 IgG вследствие введения различных вакцин, лишь в немногих работах содержатся данные о продолжительности иммунного ответа. Например, для препарата PiCoVacc (инактивированная вакцина), опубликованы результаты доклинических испытаний, согласно которым титр антител после вакцинации мышей и крыс сохраняется в течение шести недель, а у макак-резусов — до трех недель [25]. В работе, опубликованной Wang с соавт., анализ иммуногенности у животных был ограничен четырьмя неделями [27].
В случае вакцины-кандидата BBV152 измерение иммуногенности при трехдозовом режиме введения проводилось до 25-го дня [29]. Авторы провели оценку долгосрочной иммуногенности у мышей и игрунок в течение одного года. За этот период значительного снижения титров НАт обнаружено не было. Более низкие дозы вводимого антигена приводили к формированию более низкого титра НАт в течение длительного периода наблюдения. Хотя очевидно, что окончательные сведения о длительности иммунитета, обеспечиваемого вакцинами против COVID-19, будут получены в ходе длительных клинических исследований, в данной ситуации животные модели могут служить в качестве удобных суррогатных индикаторов на ранних этапах процесса разработки вакцины. В недавней работе, посвященной клиническому исследованию вакцины на основе мРНК компании Moderna, сообщается о существовании повышенного титра специфических антител в течение как минимум трех месяцев [30]. Согласно экспериментальным данным авторов статьи, вакцина «КовиВак» обеспечивала формирование стабильного длительного иммунитета у мышей и игрунок после двухкомпонентного режима введения препарата.
Профилактическая эффективность
В большинстве недавних исследований в качестве удобной и достоверно нелетальной животной модели профилактической эффективности вакцин против COVID-19 используется золотистый (сирийский) хомячок. У сирийских хомячков инфекция SARS-CoV-2 вызывает значительные патологические изменения в легких и, таким образом, поддерживает развитие стабильного постинфекционного гуморального иммунного ответа в экспериментах с пассивным переносом [35]. Более того, наблюдаемые иммуногистохимические изменения и характер потери массы тела у хомячков сходны с легкой формой инфекции SARS-CoV-2 у человека [36]. В ряде работ продемонстрирована пригодность сирийского хомячка в качестве модели для изучения профилактической эффективности НАт и вакцин против SARS-CoV-2 [37–46], хотя симптомы пневмонии у животного развиваются быстро и протекают тяжело.
Сирийский хомячок в качестве модельного объекта был использован для оценки профилактической эффективности нескольких инактивированных вакцин [47–48], в том числе одобренных для клинического применения [29]. К основным параметрам оценки относят вес животного и присутствие вируса и/или вирусной РНК в мазках из носа, легких и других органов в разные сроки после инфицирования.
В исследовании авторов животные из группы контроля теряли вес до пятого — седьмого дня с момента заражения, тогда как вакцинированные набирали вес с начиная с третьего дня после заражения, что соотносится с данными о BBV152 [29]. Однако потеря веса у контрольных животных в экспериментах авторов была более выраженной — 15 % против 2–10 % в исследовании BBV152. Скорость выведения вирусной РНК из верхних дыхательных путей также была сходной: начиная с седьмого дня после инфицирования в большинстве мазков из носа вирусная РНК не содержалась. Уровень вирусной РНК в легких контрольных животных был одинаковым в обоих исследованиях; по данным авторов, в органах всех контрольных животных содержалась вирусная РНК на четвертые, седьмые и 14-е сутки. Ткани легких вакцинированных животных в основном не содержали вируса: только у одного из пяти хомячков на четвертый и седьмой дни можно было выявить РНК вируса в легких; однако к 14-му дню ткань легких очищалась от вируса. Вирусная РНК была обнаружена в иных тканях (помимо легочной) у животных контрольной группы только на третий день после заражения. Аналогичные результаты были получены для вакцинного препарата BBV152 [29]. Таким образом, представленные результаты демонстрируют профилактическую эффективность вакцины «КовиВак» на модели сирийского хомячка.
Таким образом, для вакцины «КовиВак» не было обнаружено признаков острой/хронической, репродуктивной, эмбрио- и фетотоксичности или тератогенного влияния в антенатальном и постнатальном периодах развития, а также признаков гиперчувствительности у исследованных видов животных. Вакцина способствовала формированию стабильного и устойчивого гуморального иммунного ответа — как в виде специфических IgG к SARS-CoV-2, так и НАт у грызунов и обезьян. Значительного снижения титров НАт в течение одного года не наблюдалось. «КовиВак» продемонстрировала профилактический эффект по отношению к инфекции SARS-CoV-2 у сирийских хомячков. Эти данные стимулируют дальнейшее изучение вакцины «КовиВак» в клинических испытаниях.