Искусственная вентиляция легких (ИВЛ): инвазивная и неинвазивная респираторная поддержка
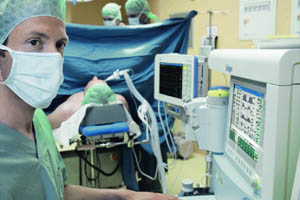
К искусственной вентиляции легких (ИВЛ) прибегают для оказания помощи пациентам с острой или хронической дыхательной недостаточностью, когда больной не может самостоятельно вдыхать необходимый для полноценного функционирования организма объем кислорода и выдыхать углекислый газ. Необходимость в ИВЛ возникает при отсутствии естественного дыхания или при его серьезных нарушениях, а также во время хирургических операций под общим наркозом.
Что такое ИВЛ?
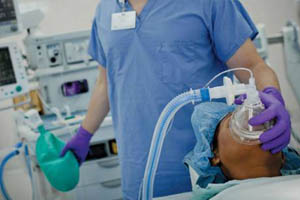
Искусственная вентиляция в общем виде представляет собой вдувание газовой смеси в легкие пациента. Процедуру можно проводить вручную, обеспечивая пассивный вдох и выдох путем ритмичных сжиманий и разжиманий легких или с помощью реанимационного мешка типа Амбу. Более распространенной формой респираторной поддержки является аппаратная ИВЛ, при которой доставка кислорода в легкие осуществляется с помощью специального медицинского оборудования.
Показания к искусственной вентиляции легких
Искусственная вентиляция легких проводится при острой или хронической дыхательной недостаточности, вызванной следующими заболеваниями или состояниями:
Инвазивная вентиляция легких
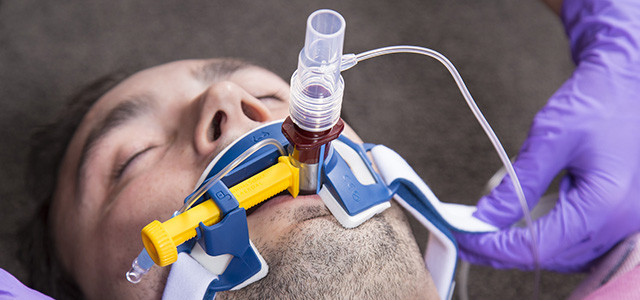
Эндотрахеальная трубка вводится в трахею через рот или через нос и подсоединяется к аппарату ИВЛ
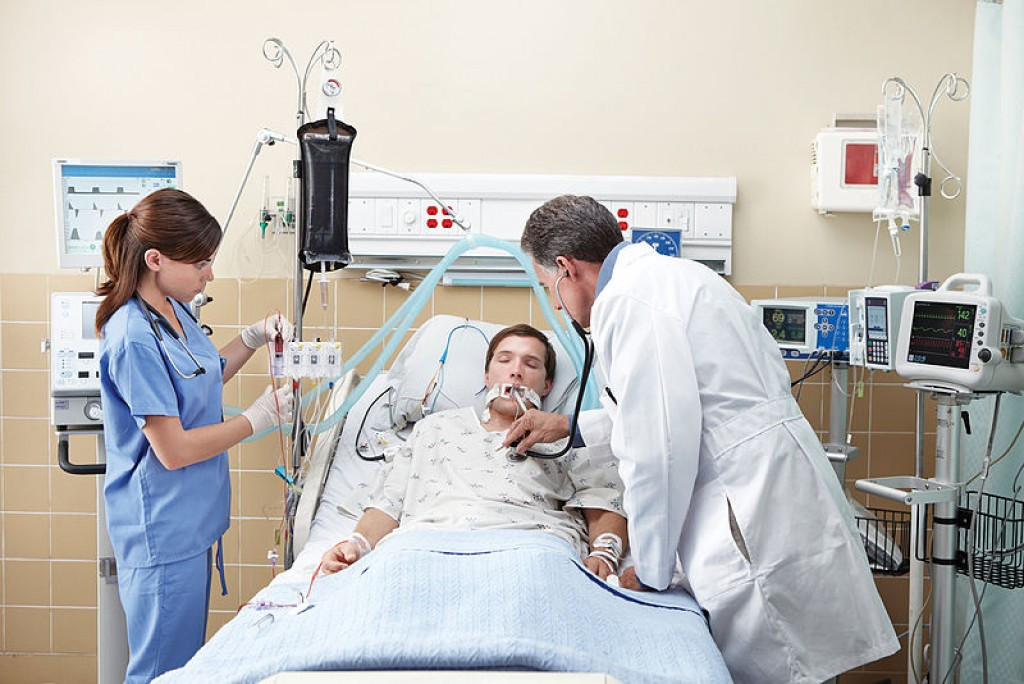
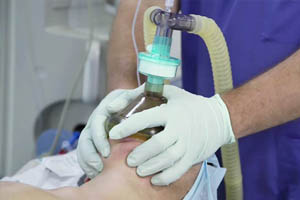
При инвазивной респираторной поддержке аппарат ИВЛ обеспечивает принудительную прокачку легких кислородом и полностью берет на себя функцию дыхания. Газовая смесь подается через эндотрахеальную трубку, помещенную в трахею через рот или нос. В особо критических случаях проводится трахеостомия – хирургическая операция по рассечению передней стенки трахеи для введения трахеостомической трубки непосредственно в ее просвет.
Инвазивная вентиляция обладает высокой эффективностью, но применяется лишь случае невозможности помочь больному более щадящим способом, т.е. без инвазивного вмешательства.
Кому и когда необходима инвазивная ИВЛ?
Подключенный к аппарату ИВЛ человек не может ни говорить, ни принимать пищу. Интубация доставляет не только неудобства, но и болезненные ощущения. Ввиду этого пациента, как правило, вводят в медикаментозную кому. Процедура проводится только в условиях стационара под наблюдением специалистов.
Инвазивная вентиляция легких отличается высокой эффективностью, однако интубация предполагает введение пациента в медикаментозную кому. Кроме того, процедура сопряжена с рисками.
Традиционно инвазивную респираторную поддержку применяют в следующих случаях:
Как работает аппарат инвазивной ИВЛ?
Принцип работы приборов для инвазивной ИВЛ можно описать следующим образом.
Особенности оборудования для инвазивной вентиляции
Оборудование для инвазивной вентиляции легких имеет ряд характерных особенностей.
Неинвазивная вентиляция легких
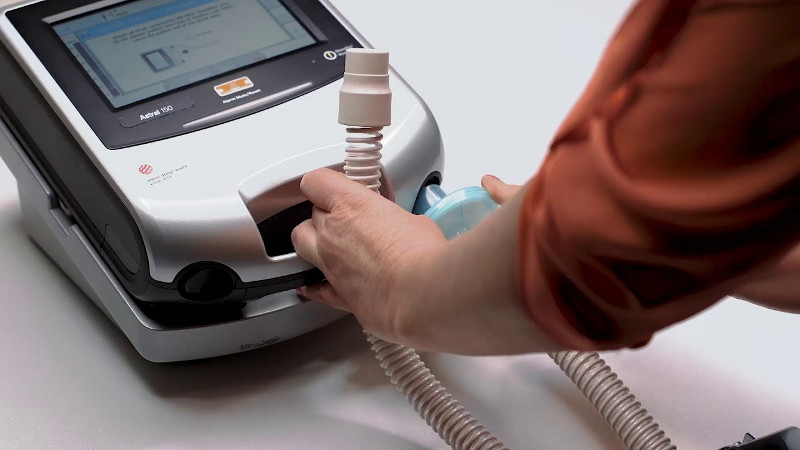
За последние два десятилетия заметно возросло использование оборудования неинвазивной искусственной вентиляции легких. НИВЛ стала общепризнанным и широко распространенным инструментом терапии острой и хронической дыхательной недостаточности как в лечебном учреждении, так и в домашних условиях.
Одним из ведущих производителей медицинских респираторных устройств является австралийская компания ResMed
НИВЛ — что это?
Неинвазивная вентиляция легких относится к искусственной респираторной поддержке без инвазивного доступа (т.е. без эндотрахеальной или трахеостомической трубки) с использованием различных известных вспомогательных режимов вентиляции.
Оборудование подает воздух в интерфейс пациента через дыхательный контур. Для обеспечения НИВЛ используются различные интерфейсы – носовая или рото-носовая маска, шлем, мундштук. В отличие от инвазивного метода, человек продолжает дышать самостоятельно, но получает аппаратную поддержку на вдохе.
Когда применяется неинвазивная вентиляция легких?
Ключом к успешному использованию неинвазивной вентиляции легких является признание ее возможностей и ограничений, а также тщательный отбор пациентов (уточнение диагноза и оценка состояния больного). Показаниями для НИВЛ являются следующие критерии:
Прекращение длительной ИВЛ
Прекращение длительной ИВЛ, извлечение интубационной трубки из просвета гортани и трахеи и переход к самостоятельному дыханию – ответственные шаги после осуществления продолжительной искусственной вентиляции легких. Любой ошибочный шаг на этой стадии лечения способен нивелировать достигнутые терапевтические результаты.
Начало постепенного прекращения вспомогательной вентиляции является таким же важным моментом, как и начало. Специалисты считают, что продолжительное использование данного метода провоцирует развитие зависимости от аппарата у неврологических пациентов. Человек попросту привыкает к аппарату, у него может наблюдаться ослабление мышечного аппарата.
Условия прекращения респираторной поддержки
Ключевым требованием к прекращению ИВЛ является пресечение недостаточности дыхания и восстановление газообмена в легких при самостоятельной дыхательной активности. При самостоятельном дыхании РаО2 должно достигнуть 80 мм.рт.ст, сердечный ритм, дыхательные движения, показатели давления должны пребывать в пределах нормы.
Во время перехода на самостоятельную дыхательную активность и при извлечении интубационной трубки из гортани и трахеи пациент должен самостоятельно делать вдох с показателями разрежения не менее 20 см. вод.ст.
После прекращения продолжительной искусственной вентиляции легких извлечение интубационной трубки должно осуществляться спустя несколько часов после возвращения самостоятельной дыхательной активности у человека. За этот промежуток времени не должно наблюдаться таких признаков:
Временной промежуток, в котором происходит адаптация пациента, зависит от различных факторов – от продолжительности дыхания с помощью аппарата, от характера заболевания. Длительность восстановления колеблется от нескольких часов до нескольких суток, кроме того, могут потребоваться специальные дыхательные упражнения, чтобы восстановить мышечный аппарат и укрепить его. Чтобы провести постепенную адаптацию с самостоятельному дыханию и плавно тренировать дыхательные мышцы, часто прибегают к помощью специального т-образного коннектора. Он подсоединяется к интубационной трубке, аппарат отключается. Через вход этого коннектора человек вдыхает воздух, обогащенный кислородом.
Определение подготовленности пациента к переводу
Ключевыми показателями для извлечения интубационной трубки являются:
Перед изъятием трубки проводится тщательный туалет дыхательных путей. Они должны быть полностью проходимыми. Если на протяжении нескольких суток у пациента не отмечается динамика к самостоятельному дыханию, ИВЛ заменяют интубацией через трахеостому. Важно вовремя обнаружить ошибки при прекращении вентиляции. Иногда, чтобы сохранить функцию диафрагмы, прибегают к электрической стимуляции нервов в ней.
Методики «отлучения» от респиратора
Чтобы прекращение искусственной вентиляции легких было успешным, прибегают к помощи таких средств:
Если у пациента отмечается наличие сопутствующей обструкции дыхательных путей и другие нарушения (левожелудочковая недостаточность, ишемия миокарда), при высоких дыхательных нагрузках среднее внутриплевральное давление может существенно снижаться. Так происходит увеличение постнагрузки, появляется ишемия или застойные явления в сосудах легких. В этих случаях уменьшают потребность в вентиляции теми методами, которые способствуют улучшению механики внешнего дыхания и уменьшают минутную вентиляцию.
Положительный результат приносит применение самостоятельных вдохов и выдохов с постоянно положительным давлением. Либо же применяется неинвазивная респираторная поддержка. Чтобы улучшить функционирование сердца и уменьшить признаки ишемии, используют терапию медикаментозными средствами.
Трахеостомия в практике врача-реаниматолога
На сегодняшний день, одним из эффективных методов в арсенале средств борьбы с нарушениями функции внешнего дыхания является трахеостомия. Указанная методика широко применяется в реаниматологической практике, трахеостомию выполняют приблизительно у 10% пациентов, находящихся на ИВЛ.
Показаниями к выполнению трахеостомии и трахеотомии являются:
1.Стенозирующий ларинготрахеобронхит III и IV степени через 1—2 дня безуспешного лечения при назотрахеальной интубации,
2. Инородные тела трахеи при невозможности их удаления во время прямой ларингоскопии или верхней трахеобронхоскопии.
3. При дренировании дыхательных путей у больных с нарушением акта откашливания.
4. В случаях заведомо длительной (более 5 сут) искусственной вентиляции легких.
5. При рубцовых стенозах и опухолях гортани при невозможности выполнения радикальных операций.
6. При травмах гортани и трахеи с нарушениями внешнего дыхания.
7. При черепно-мозговой травме с необходимостью систематического дренирования трахеобронхиального дерева или длительной искусственной вентиляции легких.
8. Обширные ранения с повреждением лицевого скелета.
Преимущества трахеотомии перед интубацией трахеи:
По данным современных литературных обзоров, среди общеизвестных преимуществ трахеостомии — меньшая потребность в глубокой седации, более быстрое отлучение от респиратора и уменьшение длительности пребывания в ОРИТ и лечебном учреждении. Прежде всего, от ранней трахеостомии выиграют больные с тяжелой сочетанной травмой, особенно с черепно-мозговой травмой и(или) с нарушениями сознания. За исключением нескольких сообщений, не отмечалось различий в уровне смертности между больными с трахеостомой или продленной трансгортанной интубацией. Зачастую, пациенты с трахеостомой могут быть раньше переведены из ОРИТ в профильное отделение, поэтому вопрос раннего наложения трахеостомы должен рассматриваться, как только складываются подходящие условия. У больных с трахеостомой инциденты, связанные с трахеостомической трубкой, могут быть более частыми и с более тяжелыми последствиями, поэтому при решении о переводе больного из ОРИТ прежде всего должна учитываться безопасность пациента.
Безусловно, трахеостомия не лишена и серьезных недостатков, связанных с повышением риска инфекционных осложнений, необходимостью постоянного тщательного ухода за трахеостомой и вероятностью возникновения осложнений во время выполнения этой операции (травма пищевода, кровотечение, острый стеноз трахеи и др.). Поэтому принципиально важным является вопрос уход за трахеостомой, так помимо постоянного удаления трахеобронхиального секрета, необходима активная профилактика гнойного трахеобронхита, мацерации кожи, вторичного инфицирования мягких тканей вокруг послеоперационной раны и т. п.
Это достигается регулярным проведением следующего комплекса мероприятий:
1. Больных с трахеостомой необходимо содержать в помещении с повышенной влажностью воздуха. Для этой цели устанавливается специальный увлажнитель. Повышенная влажность воздуха в летнее время может быть достигнута развешиванием мокрых простыней, а зимой — сушкой их на радиаторах парового или водяного отопления;
2. Помимо регулярного промывания дыхательных путей растворами фурацилина, новокаина, использования протеолитических ферментов, необходимо периодически проводить ингаляции с антибиотиками и щелочно-масляными смесями;
3. Кожу вокруг трахеостомы следует систематически тщательно осушивать и смазывать цинковой мазью либо пастой Лассара;
4. К трахеостоме нужно относиться как к абсолютно стерильной ране — производить манипуляции только тщательно обработанными руками, прокипяченными инструментами, дренажными трубками и растворами. При перевязках пользоваться только стерильным перевязочным материалом и запретить работу без марлевых масок и специальных халатов;
5. В палате, где находится больной с трахеостомой, целесообразно периодически проводить санацию воздуха ультрафиолетовым облучением;
6. С такими больными необходимо регулярно заниматься активной дыхательной гимнастикой и по возможности обеспечивать им двигательный режим.
Следует помнить, что и сама операция и трахеостомическая канюля далеко не безразличны для дыхательных путей. Уже через 2—3 ч после наложения трахеостомы на слизистой оболочке вокруг трахеостомического отверстия появляется пояс рыхлого фибринозного налета. В некоторых случаях этот налет распространяется на слизистую гортани, надгортанник и вниз вплоть до бифуркации трахеи и даже главных бронхов. Непосредственно вокруг канюли очень быстро (через несколько часов) развивается некротическая зона, отек тканей, гиперемия, лейкоцитарная инфильтрация.
В более поздние сроки обнаруживаются эрозии или (значительно реже) глубокие язвы. На 5—7-е сутки наступает метаплазия призматического эпителия в многослойный плоский.
Все это свидетельствует о том, что содержание канюли в просвете трахеи для больного далеко не безразлично. Поэтому возникает вопрос не только о строгих показаниях к трахеостомии, но и о наиболее рациональных сроках удаления канюли (деканулирования).
Существуют следующие правила: если в течение 1—2 суток после операции дыхание пострадавшего остается в пределах нормы, и нет угрозы рецидива дыхательной недостаточности, канюлю следует удалять.
Серьезные изменения в тканях, окружающих трахеостому, свидетельствуют также о том, что в случаях, когда искусственная вентиляция легких предположительно необходима на сравнительно короткий срок (до 24 ч), трахеостомия должна и может быть заменена интубацией.
При ожидаемой длительности ИВЛ больше 14-и дней следует рассмотреть вопрос о наложении трахеостомы. Однако, к сожалению, возможности клиницистов в плане предсказания продолжительности ИВЛ на раннем этапе заболевания ограничены. Однако следует ожидать, что более тяжелое течение болезни в течение продолжительного периода времени — предиктор более длительного нахождения на ИВЛ. В одном из исследовании (Rumbak ) было также отмечено, что больным с большим количеством баллов (>25) по шкале APACHE II требуется более длительная интубация.
Методики трахеостомии постоянно развиваются и совершенствуются. Все больше трахеостомии выполняется в условиях ОРИТ «у постели больного» с применением техники чрескожной дилятационной трахеостомии (ЧДТ).
В нашей клинике операция ЧДТ выполняется выполняются достаточно регулярно. Опыт выполнения чрескожной дилятационной трахеостомии позволил нам убедиться в преимуществах этой методике (в частности трахеостомии по Griggs под эндоскопическим контролем), как наиболее простой, менее затратной экономически, с наименьшим количеством осложнений.
После ивл что подключают
Современные наркозные аппараты предоставляют анестезиологу широкий выбор различных режимов ИВЛ, в отличие от более ранних моделей, где весь спектр режимов был чаще всего представлен одним-единственным – вентиляцией с контролем по объему. Выбор правильного режима для вентиляции пациента во время оперативного вмешательства очень важен, так как помимо удобства для анестезиолога имеет значительное влияние на частоту послеоперационных осложнений. В данной статье мы последовательно разберем все основные режимы вентиляции, представленные в современных наркозных аппаратах и дадим рекомендации по выбору каждого из них.
Проведение общей анестезии начинается, как правило, с преоксигенации пациента. При этом клапан APL открывают и используют поток 100% кислорода, который должен быть больше минутной вентиляции пациента. Например, для преоксигенации пациента с минутной вентиляцией 5,5 л/мин достаточен поток кислорода 7 л/мин. Длительность преоксигенации составляет 3–5 минут и оценивается по показателю концентрации кислорода на выдохе – она должна стать более 70% или стабилизироваться. Далее проводят индукцию, по мере засыпания пациента клапан APL закрывают и переходят на режим ручной ИВЛ при помощи дыхательного мешка и лицевой маски. Не рекомендуется закрывать клапан APL на значения больше 20 см вод. ст. (у взрослых пациентов), так как это может привести к раскрытию пищеводного сфинктера и раздуванию желудка. После интубации пациента или установки ларингеальной маски осуществляют капнографический и аускультативный контроль положения эндотрахеальной трубки (ларингеальной маски) и только затем переходят на автоматическую ИВЛ.
Режим вентиляции с контролем по объему (VCV) является наиболее традиционным для использования. Его плюсы заключаются в том, что пациенту гарантирован установленный минутный объем вентиляции. Минусы этого режима также существенны, так как не гарантировано безопасное значение пикового давления на вдохе. Тем не менее, этот режим очень хорошо знаком большинству анестезиологов, ввиду чего используется наиболее часто у интубированных пациентов. Также этот режим рекомендован в торакальной хирургии, когда грудная клетка пациента открыта и использование режимов с контролем по давлению способно привести к перераздуванию легких.
Режим вентиляции с контролем по давлению (PCV) неоправданно находит значительно меньшее применение, особенно у нас в стране. Вместе с тем, он позволяет более точно контролировать пиковое давление на вдохе, более физиологичен и безопасен. Есть много работ, подтверждающих, что PCV более предпочтителен у пациентов с повышенной массой тела, так как позволяет добиться того же минутного объема вентиляции при значительно меньших цифрах пикового давления на вдохе, по сравнению с вентиляцией с контролем по объему. Режим также хорош тем, что позволяет быстро заметить снижение качества мышечной релаксации, компрессию грудной клетки, обструкцию дыхательных путей и другие неприятности.
Режимы перемежающейся принудительной вентиляции с контролем по давлению или по объему (SIMV и PSIMV) предпочтительны при сохранении у пациента спонтанной вентиляции в той или иной степени, например, при использовании ларингеальной маски. Они позволяют пациенту дышать в промежутках между принудительными вдохами. Поддержку самостоятельных вдохов пациента можно решать подключением опции поддержи давлением (PSV) или поддержки объемом (VSV).
Поддержка самостоятельного дыхания давлением или объемом (PSV и VSV), как отдельные режимы, применяются при сохранении или восстановлении спонтанного дыхания у пациента. Часто применяются при использовании ларингеальной маски, а также на этапе окончания анестезии. Это группа чисто вспомогательных режимов, которые будут работать только в случае сохранения у пациента спонтанного дыхания адекватной частоты. К группе вспомогательных режимов относится и режим SPONT, когда полностью спонтанное дыхание пациента может также поддерживаться давлением.
В заключение следует сказать несколько слов об использовании во время операции функции положительного давления в конце выдоха (PEEP), чем часто необоснованно пренебрегают. Данная опция есть во всех современных наркозных аппаратах, причем в некоторых из них определенное базовое PEEP отключить невозможно. Использование положительного давления в конце выдоха позволяет предупредить развитие послеоперационных ателектазов, а также избежать значительного снижения функциональной остаточной емкости легких при лапароскопических вмешательствах. Базовые значения PEEP у взрослых – 3-5 см вод. ст., а при необходимости данный параметр может достигать 10 см вод. ст. и более.
Что такое ЭКМО?
Уважаемые пациенты и их родственники, теперь Вы можете узнать в статье «ЧТО ТАКОЕ ЭКМО?» ответы на часто задаваемые вопросы относительно технологии ECMO.
Содержание
Введение
Уважаемые родственники и друзья пациентов!
Этот раздел создан Российским обществом специалистов ЭКМО (РосЭКМО) для информирования родственников пациентов, находящихся на ЭКМО. Здесь представлены краткий обзор самой процедуры и ответы на некоторые распространенные вопросы.
Следует иметь в виду, что процедуры, правила и методы лечения могут немного различаться между больницами. В данном разделе мы предоставляем лишь общую информацию, которая является основой для всех центров ЭКМО.
Если вам нужны дополнительные сведения и данные о конкретном пациенте/ситуации, то следует задавать вопросы специалистам непосредственно в вашей больнице.
С уважением,
РосЭКМО
Что такое ЭКМО?
ЭКМО – это специальный метод лечения, при котором используются искусственные сердце и легкое для обеспечения временной поддержки жизни пациента и функционирования его организма, когда собственные сердце и/или легкие человека слишком больны, чтобы выполнять свою нормальную работу. ECMO может поддерживать организм в течение длительного периода времени (от нескольких дней до нескольких недель и даже месяцев), чтобы дать возможность сердцу и/или легким отдохнуть и оправиться от болезни. Хотя сама по себе ЭКМО не вылечит пациента, но она даст ему/ей время, необходимое для лечения и выздоровления. Чаще всего к ECMO прибегают после того, как врачи пробовали применять все другие виды лечения, такие как искусственная вентиляция легких (ИВЛ), лекарства для поддержки работы сердца и легких и так далее, но этого недостаточно для поддержания жизни пациента.
После того, как сердце и/или легкие пациента восстановятся так, чтобы обеспечивать потребности его организма, ЭКМО будет отключена. Если врачи поймут, что ECMO не помогает улучшить ситуацию, или если продолжение её использования может повредить пациенту, процедура также будет прекращена.
Как работает ЭКМО?
Подобно аппарату искусственного кровообращения, используемому при операциях на открытом сердце, для ЭКМО применяются специальный насос, который берет на себя работу сердца по перекачиванию крови, и мембранный оксигенатор (искусственное легкое), который выполняет работу легких по газообмену. Для соединения контура ECMO с организмом пациента одна, две или больше канюль (специальные большие пластиковые устройства, помещаемые в артерии или вены) вводятся в крупные кровеносные сосуды пациента (например, на шее, бедре или напрямую в камеры сердца в грудной клетке). На основании данных о болезни и состоянии пациента команда врачей определит, какой тип ЭКМО использовать, количество необходимых канюль и место их установки. Для установки канюль и начала процедуры в некоторых случаях необходима хирургическая операция, которая обычно проводится сердечнососудистым хирургом. Перед процедурой пациенту получит лекарства от боли и для седации.
Кровь пациента из канюли проходит через оксигенатор (искусственное легкое – устройство со специальной мембраной, через которую происходит газообмен), где кислород добавляется в кровь, а углекислый газ (отработанный газ) удаляется. Затем насыщенную кислородом кровь согревают и возвращают в тело пациента.
С помощью ЭКМО можно поддерживать необходимую организму доставку кислорода, при этом собственные легкие и/или сердце пациента будут находиться в режиме «отдыха». Это даст время и возможность легким и/или сердцу восстановить свою нормальную работу. Таким образом ECMO обеспечивает «мост» к выздоровлению.
На этой картинке показана типичная схема ЭКМО с синей (без кислорода) кровью, которая становится красной (насыщенной кислородом) в оксигенаторе (искусственном легком) вне тела (экстракорпорально). Центрифужный насос (искусственное сердце) обеспечивает перекачивание крови.
Типы ЭКМО
Существует два основных типа ЭКМО (в некоторых редких случаях могут использоваться их модификации). Вено-Артериальная (ВА) ЭКМО применяется для поддержки сердца и/или легких, тогда как Вено-Венозная (ВВ) ЭКМО используется только для поддержки легких. Специалисты на основании болезни и состоянии пациента решат какой тип нужен пациенту.
Вено-Артериальная (ВА) ЭКМО обеспечивает поддержку сердца пациента и легких, позволяя большей части крови пациента перемещаться по контуру в обход сердца пациента. При этом типе подключения кровь забирается из венозного русла и возвращается в артериальное русло, позволяя насыщенной кислородом крови циркулировать по организму, когда собственное сердце пациента не способно прокачивать кровь через организм и обеспечивать его функционирование. Таким образом, аппарат ECMO возьмет на себя насосную функцию сердца, позволяя ему восстанавливаться в режиме «отдыха». В случае ВА ЭКМО используются две канюли – артериальная и венозная, которые могут быть установлены в сосуды на бедре, шее, либо в грудной клетке.
Вено-Венозная (ВВ) ЭКМО осуществляет только поддержку легких, поэтому сердце пациента должно по-прежнему работать достаточно хорошо, чтобы обеспечивать потребности организма. Такой тип подключения применяется для пациентов с тяжёлой дыхательной недостаточностью, когда необходимо только насыщение крови кислородом и удаление углекислого газа, а поддержание насосной функции сердца не требуется. При ВВ ЭКМО насыщение крови кислородом происходит в венозной части системы кровообращения организма. Две канюли помещаются в вены в местах рядом с сердцем или внутри него. Врач может использовать специальный тип канюли с двумя просветами (пути для крови внутри канюли). Это позволяет забирать и возвращать кровь в организм в одном месте. Кровь из контура возвращается перед сердцем пациента, а уже его собственное сердце будет перекачивать насыщенную кислородом кровь по всему телу. При ВВ ЭКМО легкие будут находиться в режиме «покоя» или «щадящем» режиме для обеспечения нормализации/восстановления их функции. Обычно пациенты с повреждением легких нуждаются в искусственной вентиляции легких (ИВЛ), при которой аппарат ИВЛ нагнетает кислород в легкие пациента. Если легкие сильно повреждены, то для поддержания нормального уровня кислорода в крови требуются высокие давление нагнетания и концентрация кислорода. Это, в свою очередь, приводит к последующему травмированию ткани легких, что ведет к необходимости увеличения давления и концентрации кислорода в подаваемой аппаратом ИВЛ газовой смеси. Таким образом, создается порочный круг повреждения больных легких. ECMO «разрывает» этот порочный круг, позволяя легким восстановиться в «щадящем» режиме вентиляции, а организму справиться с основным заболеванием.
Что происходит с пациентом на ЭКМО
Жизнь пациента на ЭКМО поддерживается большой командой профессионалов, включая специалистов ECMO, реаниматологов, хирургов, кардиологов, пульмонологов, физиотерапевтов, реанимационных медсестер и многих других специалистов.
Многие беспокоятся о боли или страданиях, которые испытывает пациент от тяжелого заболевания и большого количества сложных процедур во время ЭКМО. Врачи и медсестры в отделении реанимации и интенсивной терапии будут внимательно следить за любыми признаками того, что пациент чувствует боль, и использовать специальные лекарства для исключения этого. Конечная цель для профессионалов-медиков в отделении реанимации заключается в том, чтобы пациент мог спать и просыпаться с нормальным суточным ритмом и взаимодействовать с окружающим миром (включая родственников), не испытывая боли или тревоги. Зачастую первоначальная процедура подключения требует общей анестезии (наркоза), чтобы пациент спал и не мог почувствовать боль. После этого пациентам дают постепенно просыпаться, а врачи будут обеспечивать седацию (применять успокаивающие препараты), вводить противоболевые лекарства по мере необходимости, чтобы пациенту было комфортно и безопасно. Медсестры в реанимации очень хорошо обучены определять признаки боли и страдания и будут следить за любыми изменениями в состоянии пациента.
Кровь и препараты крови
ЭКМО – это специальный аппарат, который требует значительного количества крови для заполнения, чтобы он мог правильно работать. Во время нахождения на ECMO пациент, скорее всего, получит много донорских продуктов крови для доставки достаточного количества кислорода в органы и ткани, а также для заживления послеоперационных ран, мест, где были размещены канюли, и так далее. Это абсолютно нормальная практика, и переливание крови не обязательно является причиной для тревоги. Если ваша больница разрешит, вы также можете пожертвовать кровь, которая может использоваться для вашего родственника или может быть отдана в общий банк крови, чтобы другие пациенты могли воспользоваться этой спасительной терапией так же, как ваш родственник получал кровь от других доноров.
Лекарственные препараты
Важно понимать, что ЭКМО не является лекарством от какой-либо болезни. Скорее это инструмент, который врачи могут использовать для поддержки жизни пациента, чтобы у него было время получить лекарства и лечение, которые в конечном итоге помогут ему выздороветь. Пациент на ECMO будет получать множество лекарств со многими сложными названиями. Это могут быть антибиотики (чтобы лечить/предотвратить инфекцию), успокоительные лекарства и препараты против боли (чтобы ему было комфортно), диуретики (чтобы помочь почкам выделять мочу), а также и другие виды лекарств, которые будут применяться в зависимости от причины, по которой пациент был подключен к ЭКМО. Со временем, когда пациент начнет выздоравливать, многие из этих лекарств больше не будут требоваться.
Во время ЭКМО пациенту будут проводиться ряд обычных медицинских процедур, которые помогают следить за его состоянием и выздоровлением. Ниже описаны некоторые из этих процедур.
Анализы
Будет требоваться большое количество анализов для контроля функций органов, инфекции и выздоровления. Не беспокойтесь, врачи не будут брать больше крови, чем нужно. Забор крови из системы ECMO или специальных катетеров в пациенте безболезненен и не требует никаких игл или проколов.
Рентген грудной клетки
Необходим для оценки динамики состояния легких. В первые дни ЭКМО рентгенограмма легких может выглядеть как белое пятно. Со временем на снимке начнут появляться участки черного цвета, указывающие на то, что легкие снова наполняются воздухом. Рентген грудной клетки позволяет подобрать параметры искусственной вентиляции легких, контролировать любые побочные эффекты, например пневмоторакс (медицинский термин, обозначающий, что воздух выходит за пределы легких в грудную клетку), когда, возможно, потребуется установить дренаж (трубку для удаления воздуха), чтобы позволить легким расправиться.
Эхокардиография
Эхокардиография – это визуализация сердца пациента с помощью ультразвука. Это неинвазивная и безопасная процедура позволяет оценить размеры и функции сердца: работу камер сердца (желудочков) и клапанов. С помощью эхокардиографии можно точно увидеть расположение канюль и потоки крови из контура, что помогает позиционировать канюли и настроить правильные параметры работы аппарата ECMO. Эхокардиография поможет оценить восстановление собственной функции сердца и точно оценить, насколько сердце готово обеспечивать кровообращение в организме без ЭКМО.
Питание
В течение первых нескольких дней на ЭКМО пациенту не нужно есть, потому что все питание (все витамины, минералы и калории, которые необходимы организму) он/она будут получать через внутривенные катетеры. При тяжелых заболеваниях организм не способен обеспечить достаточное количество кислорода или крови для всех органов и тканей и пытается сохранить то, что он может поддержать, уменьшая приток крови к определенным органам, чтобы гарантировать, что самые жизненно важные органы (сердце и мозг) получат достаточно крови, кислорода и питания. В таких случаях желудок и кишечник могут испытывать снижение кровотока и не смогут полноценно работать. Но как только состояние стабилизируется, и кишечник снова сможет работать, врачи начнут вводить жидкую пищу в желудок или кишечник через специальную трубку, помещенную в нос (назогастральный зонд). В дальнейшем, если врачи посчитают, что пациент достаточно хорошо себя чувствует и сможет безопасно есть самостоятельно, то пациент сможет пить и есть обычным путем.
Физиотерапия
В большинстве случаев пациенту, который находится на ЭКМО, приходится лежать на спине в кровати. Чем дольше пациент прикован к постели, тем больше времени потребуется для возвращения к нормальной жизни после выздоровления. Если мышцы не работают, то они атрофируются (становятся меньше). Пациенты нуждаются в разном времени ЭКМО, и по мере увеличения продолжительности, может возникнуть необходимость в физиотерапии, чтобы помочь поддерживать функцию мышц и подвижность суставов. Этим занимаются специально подготовленные специалисты – физиотерапевты и массажисты. Сначала это могут быть простые упражнения пассивного движения, когда физиотерапевт сам двигает руки и ноги пациента. Со временем пациент начнет включать в процесс свои мышцы, чтобы противодействовать движением физиотерапевта, тренируя их таким образом. Когда медицинская команда считает безопасным и необходимым для пациента, то при определенном типе канюль, пациент может сидеть на кровати, вставать и даже ходить. Это относительно новая методика ранней реабилитации пациентов на ЭКМО, но она помогает пациентам быстрее вернуться к своей нормальной жизни. Если имеются какие-либо опасения по поводу безопасности физиотерапии во время ECMO, она не будет добавлена в лечение до тех пор, пока врачи не посчитают это безопасным и необходимым для пациента.
Как долго пациент будет на ECMO?
Это, вероятно, самый важный вопрос для родственников, и самый сложный для врачей. Каждый пациент индивидуален и требует разного времени пребывания на ЭКМО, в зависимости от причины ECMO. Некоторые пациенты могут быть отключены от аппарата менее чем через 24 часа, а другие должны находиться на нём месяц и даже больше. Чаще всего пациенты находятся на ВА ЭКМО в течение 5-10 дней, на ВВ ЭКМО в течение 10-14 дней, но это только средние значения, которые не отражают состояние и потребность в ECMO конкретного пациента.
Врачи будут прилагать все усилия, чтобы ЭКМО можно было отключить как можно раньше. Несмотря на то, что ECMO предоставляет много преимуществ для спасения жизни пациентов и может быть обеспечена достаточно безопасность этой процедуры в течение разумного срока, но имеются возможные риски и осложнения, и отключение ЭКМО может стать единственным способом полностью избежать этих рисков.
Риски и осложнения
ЭКМО – экстремальная и очень сложная и инвазивная процедура спасения жизни. С одной стороны, ECMO предоставляет большие преимущества для спасения жизни, но с другой эта процедура имеет собственные риски. По возможности врачи обсудят все потенциальные риски и осложнения до установки канюль и начала процедуры (в некоторых случаях ЭКМО это экстренная процедура для спасения жизни, например, при остановке сердца, и в этом случае нет возможности для обсуждения ее рисков/преимуществ с пациентом или родственниками).
Некоторые из наиболее распространенных рисков перечислены ниже. Хотя эти и другие осложнения (проблемы) возможны у любого пациента на ЭКМО, команда врачей сделает все возможное для снижения этих рисков. Хорошо обученная команда будет круглосуточно тщательно контролировать состояние пациента и параметры работы аппаратуры ЭКМО, чтобы минимизировать вероятность осложнений и обеспечить безопасность процедуры. Если возникнут осложнения, специалисты подберут наилучший план лечения для пациента.
Наиболее распространенный риск при ЭКМО – кровотечение. Специальное лекарство – гепарин – должно постоянно добавляться в контур для предотвращения образования тромбов (сгустков крови). Во время ECMO кровь забирается из организма, проходит через сложную систему контура, контактируя с чужеродной для нее пластиковой поверхностью, что активизирует систему свертывания крови и ведет к образованию тромбов (сгустков). Гепарин препятствует их образованию. Чаще всего кровотечение возникает вокруг мест установки канюль либо в местах хирургических операций. Тем не менее, кровотечение может происходить в любом месте и органе, если пациент получает гепарин. Наиболее опасный вид кровотечения – кровоизлияние в мозг, поэтому специалисты постоянно и тщательно контролируют систему свертывания крови для оценки признаков кровотечения. При ЭКМО достаточно часто может потребоваться переливание компонентов крови для восполнения дефицита факторов свертывания и эритроцитов.
Еще одним частым риском во время ЭКМО является тромбоз. Он также связан с активацией системы свертывания крови на чужеродной поверхности контура. Большие тромбы (сгустки) могут блокировать или резко ухудшить работу контура, а мелкие сгустки могут попадать в кровоток пациента и вызывать эмболию (закупорку) сосудов, повреждая органы.
Специалисты ЭКМО постоянно следят за контуром, чтобы вовремя обнаружить возможные осложнения и принять все возможные меры для предотвращения попадания тромбов в кровоток пациента.
Отключение ЭКМО
Специалисты будут оценивать состояние пациента каждый день. Анализы крови и оценка функции сердца и легких – лишь некоторые примеры факторов, которые будут применяться для оценки выздоровления. Когда пациент восстановится до такой степени, что от аппарата ЭКМО будет требоваться лишь очень небольшая поддержка, врачи выполнят пробную остановку ECMO. Это происходит по-разному в зависимости от типа ЭКМО – ВА или ВВ. Такая «пробная остановка» дает специалистам хорошее представление о работе организма пациента без поддержки ECMO. Канюли останутся на месте во время «пробной остановки» и будут удалены только после того, как вся команда будет уверена, что экстракорпоральная поддержка больше не понадобится пациенту.
Но даже с наилучшими усилиями специалистов и соответствующим лечением, есть вероятность, что пациенту может не стать лучше во время ЭКМО. Врачи будут ежедневно информировать родственников о состоянии пациента. Если все возможное для того, чтобы помочь пациенту, было сделано, но пациент не поправляется или даже ухудшается, врачи подробно обсудят возможные варианты с родственниками.
Некоторым пациентам, сердце и/или легкие которых не могут восстановиться, может потребоваться трансплантация этих органов или имплантируемое устройство для длительной механической поддержки сердца (искусственный желудочек сердца – VAD).
Что ожидать после ЭКМО
Когда будет принято решение отключить пациента от ECMO, то канюли удалят. Иногда для этого может потребоваться операция, которая будет выполняться в операционной. В других случаях (обычно для ВВ ЭКМО и реже для ВА ЭКМО) канюли могут быть удалены без операции в отделении реанимации и интенсивной терапии. Для предотвращения кровотечения из мест установки канюль после их удаления наложат швы и повязки.
До тех пор, пока пациент не сможет дышать самостоятельно, он/она останется на аппарате ИВЛ. Постепенно легкие пациента начнут работать лучше, и реаниматологи смогут уменьшить параметры аппарата ИВЛ. После того, как эти параметры станут совсем низкими, и пациент сможет дышать самостоятельно, ИВЛ будет прекращена.
Даже когда пациент будет отключен от ЭКМО и ИВЛ, потребуется еще некоторое время, прежде чем пациент отправится домой. Пациент должен иметь стабильные хорошие функции сердца и легких, быть в состоянии самостоятельно есть. Для возвращения к нормальной повседневной жизни пациентам могут потребоваться несколько дней или недель, так как пребывание в постели в течение длительного времени может сделать их мышцы очень слабыми, и необходимо время для их восстановления.
Роль семьи во время ECMO
Большинство членов семьи чувствуют себя более комфортно, когда они могут «сделать что-нибудь» для своего любимого человека, и есть много простых вещей, которые вы можете сделать, чтобы помочь процессу выздоровления. Пожалуйста, сначала проконсультируйтесь с персоналом, чтобы узнать, как безопасно касаться или разговаривать с пациентом.
Словарь терминов
ACT (Activated Clotting Time (эй-си-ти) – время активированного свертывания (ВАС): тест, который измеряет, сколько секунд требуется для образования сгустка крови.
ECLS: Экстракорпоральная поддержка жизни: другое название для ЭКМО.
Антибиотик: препарат, который убивает бактерии или микробы. Используется для предотвращения или лечения инфекции.
Аорта: большая артерия, которая переносит насыщенную кислородом кровь от сердца ко всему организму.
Аппарат искусственной вентиляции легких (ИВЛ): аппарат для дыхания, который доставляет воздух в легкие пациента через эндотрахеальную или трахеостомическую трубку. Также называется респиратор или вентилятор.
АПТВ: частичное тромбопластиновое время: тест, который измеряет функцию свертывания плазмы крови
Артерия: кровеносного сосуда, который переносят насыщенную кислородом кровь органам и тканям тела.
Бронхоскопия: процедура визуализации и исследования бронхов легких с помощью волоконно-оптической камеры. Образцы ткани и мокроты могут быть отправлены в лабораторию для тестирования.
ВА ЭКМО (ВеноАртериальная ЭКМО, VA ECMO): тип ЭКМО, при котором кровь забирается из вены, насыщается кислородом и возвращается в организм через артерию. Этот тип может использоваться для поддержки сердца и легких.
ВВ ЭКМО: (вено-венозная ЭКМО, VV ECMO): тип ЭКМО, при котором кровь забирается из вены, насыщается кислородом и возвращается в вену. Этот тип используется, когда в поддержке нуждаются только легкие.
Внутричерепное или внутрижелудочковое кровоизлияние: кровотечение в мозг или вокруг него. Это очень опасное потенциальное осложнение ЭКМО. Его можно увидеть на УЗИ или на КТ.
Гемофильтрация и гемодиализ: искусственная почка, которая может быть использована для удаления дополнительной жидкости и шлаков, которые не могут удалить почки пациента. Подключается в контур ЭКМО.
Гепарин: препарат, который предотвращает свертывание крови.
Деканюляция: процесс удаления канюль из кровеносных сосудов. Этот процесс может быть выполнен в отделении реанимации и интенсивной терапии, либо в операционной.
Дренаж грудной клетки: трубка, которая помещается через стенку грудной клетки в пространство между легким и грудной стенкой для удаления воздуха или жидкости. Используется для лечения спавшегося легкого (пневмоторакса) или для удаления жидкости/крови.
Искусственный желудочек сердца ( ventricle assist device (VAD): это устройство, которое помогает левому желудочку сердца, пока пациент ждет трансплантации сердца.
Канюли: пластиковые устройства, которые помещают в кровеносные сосуды для забора крови из тела в контур ЭКМО и возврата обратно.
Канюляция: процесс установки канюль в кровеносные сосуды. Этот процесс может быть выполнен хирургически (через разрез) или пункционно (проведением иглы через кожу в сосуд).
Катетеризация сердца: процедура, при которой маленький катетер помещается в вену или артерию и продвигается до сердца, чтобы посмотреть на функцию сердца под рентгеном.
Команда ЭКМО: в состав команды входят специализированные перфузиологи, реаниматологи, хирурги, медсестры.
КТ – компьютерная томография: сложный рентген, обычно головного мозга или грудной клетки, который позволяет искать кровотечение или другие проблемы.
Мембранный оксигенатор: специальное устройство с мембраной, которая удаляет углекислый газ из крови и заменяет его кислородом. Синоним «искусственное легкое».
МРТ: использование магнитного поля для визуализации мозга или других частей тела.
Острый респираторный дистресс-синдром (ОРДС, Acute Respiratory Distress Syndrome – ARDS): состояние, при котором легкие повреждены и не позволяют кислороду проникать в кровь.
Отключение ЭКМО: процесс, при котором экстракорпоральная поддержка медленно снижается по мере того, как пациенту становится лучше. Этот термин может использоваться для обозначения снижения скорости кровотока аппарата ECMO или подачи кислорода.
Пневмоторакс: утечка воздуха из легких в пространство между легкими и грудной стенкой.
Поток (скорость) ЭКМО: измеряет, сколько крови прокачивается по контуру ECMO для поддержки пациента.
Пробное отключение: период, когда поддержка ЭКМО временно прекращается или снижается до минимума, чтобы оценить функцию сердца и/или легких. Если пациент при этом будет находиться в стабильно хорошем состоянии, то ECMO может быть прекращена.
Рентген грудной клетки: рентгеновский снимок для оценки легких и сердца.
Сонная (каротидная) артерия: большая артерия в области шеи, которая переносит кровь из сердца в мозг.
Терморегулирующее устройство: специальное устройство, которое соединено с мембранным оксигенатором и согревает/охлаждает кровь до того, как она будет возвращена обратно пациенту.
Трахеостома: трубка, которая помещается прямо в трахею через переднюю поверхность шеи и ведет к легким. Эта трубка заменяет эндотрахеальную трубку. Трахеостомическая трубка помогает защитить гортань и снижает риск заражения легких микробами изо рта.
Тромбоциты: мелкие частицы в крови, которые помогают в свертывании крови.
ТЭГ (тромбоэластография): тест, который определяет функционирование свертывающей и противосвертывающей системы крови.
Углекислый газ (CO2): этот газ является одним из отходов организма, который удаляется легкими.
Центрифужный насос: «искусственное сердце» в аппарате ЭКМО – устройство, которое прокачивает кровь через контур, а затем возвращает ее пациенту.
ЭКМО (экстракорпоральная мембранная оксигенация): процедура поддержки жизни, при которой кровь забирается из организма, проходит через оксигенатор (искусственные легкие), где удаляется углекислый газ и добавляется кислород, согревается и возвращается обратно в организм. Эта процедура позволяет поддерживать организм насыщенной кислородом кровью вместо собственного сердца и легких пациента.
Экстракорпоральная сердечно-легочная реанимация (ЭСЛР, extracorporeal cardio- pulmonary resuscitation (E-CPR): чрезвычайная экстренная ЭКМО для пациентов с остановкой сердца.
Эндотрахеальная трубка: трубка, которая помещается в рот/нос и ведет в легкие, чтобы помочь дышать и защищать дыхательные пути пациента.
Эхокардиография: ультразвук, который позволяет видеть и оценивать функцию сердца.
ЭЭГ (электроэнцефалограмма): отслеживание электрической активности головного мозга. Электроды (провода) помещаются на голову в нескольких местах.