Отёк ног (нижних конечностей)
Факторы возникновения отека ног (нижних конечностей)
Отек ног (нижних конечностей) может в равной степени влиять на обе ноги или быть более выраженным на одной нижней конечности. Часто отек ног вызывается несколькими факторами, такими как венозная недостаточность, ожирение или предыдущий забор подкожной вены для шунтирующих операций на сердце.
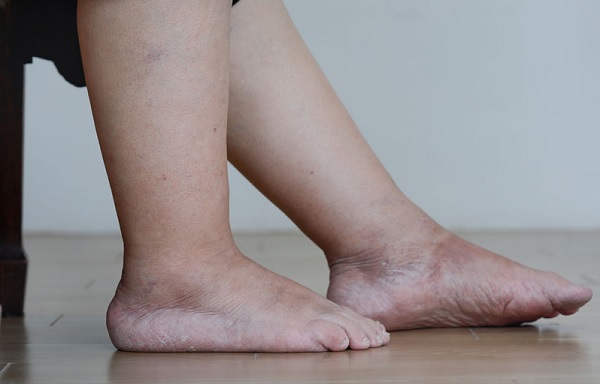
Отёк нижних конечностей
Отеки ног (нижних конечностей) могут возникать из-за повышенного давления в венах, местной травмы, воспалительных изменений, препятствия оттоку лимфатической жидкости, инфекции, низкого уровня белка в крови, ожирения, беременности, состояния задержки жидкости или воздействия лекарств. Высокое давление в венах ног приводит к тому, что жидкость, белки и клетки крови просачиваются через стенки мелких вен в мягкие ткани, особенно возле лодыжек. Это вызывает точечный отек, припухлость, которая оставляет временную вмятину на коже при компрессии обуви, носка или преднамеренном надавливании, например, при нажатии пальцем.
Отёк ног (нижних конечностей) и высокое венозное давление
Причины отёка ног (нижних конечностей) из-за повышенного венозного давления включают:
Варикоз и отечность ног
Другие причины появления отека ног (нижних конечностей)
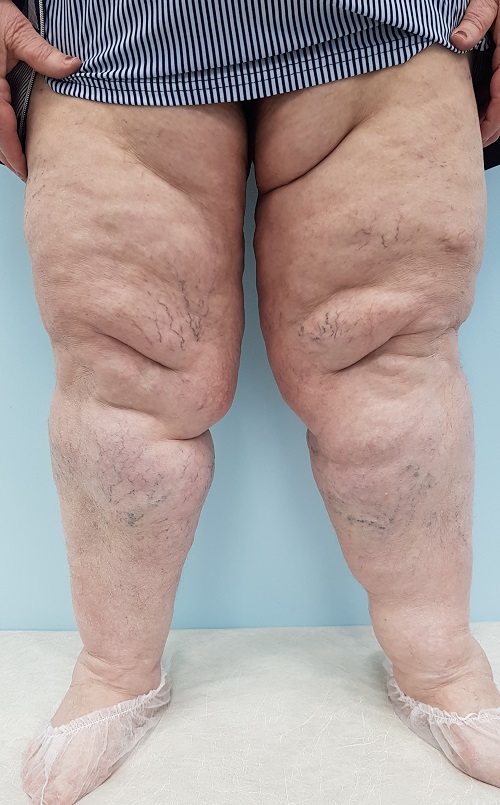
Отечность при липедеме
В зависимости от причин лимфедему разделяют на:
После венозной недостаточности ожирение является следующей по частоте причиной отека ног (нижних конечностей) в США, европейских странах и России. Абдоминальное ожирение частично препятствует венозному и лимфатическому оттоку от ног. Ожирение также ускоряет растяжение вен ног под действием силы тяжести, тем самым способствуя прогрессированию венозной недостаточности.
Вопросы пациентов об отеках на ногах (нижних конечностях)
Как избавиться от отёков ног (нижних конечностей)?
Избавиться от отёков ног в большинстве ситуаций вы сможете только при помощи доктора. Сначала необходимо выяснить причину отёка. Начать диагностику можно с визита к терапевту и флебологу.
Почему возникает отёк ног при варикозе?
Отёк ног при варикозе вен нижних конечностей возникает вследствие нарушения работы клапанного аппарата венозных сосудов. Это приводит к застою жидкости и формированию отёчности.
Как лечить отёк ног (нижних конечностей)?
Отёк ног лечится в зависимости от причины, его вызвавшей. Патология сердца, почек, венозной системы, травмы требуют своего, определённого лечения. Начать лечить отёк ног нужно с обращения к хорошему, внимательному доктору.
К какому врачу пойти, если отекают ноги?
Если отекают ноги, возможно, потребуется обратиться к нескольким специалистам. Начать можно с терапевта или кардиолога.
Отекла одна нога, как лечить?
Если у вас отекла одна нога необходимо срочно обратиться за медицинской помощью. Лучше посетить флеболога и ортопеда. Односторонняя отёчность нижней конечности может быть признаком такого грозного состояния, как тромбоз глубоких вен.
Отеки ног у лежачих больных

Различные классификации отеков как симптомов заболеваний
В норме отечность возникает после длительной нагрузки на ноги; спустя некоторое время, проведенное в неудобной обуви; при изменениях погодных условий (резкое потепление, изменение атмосферного давления). Такие отеки сигнализируют о некоторой дисфункции сердечно-сосудистой системы в период нагрузки. В норме подобные отеки исчезают самостоятельно спустя несколько часов отдыха.
У лежачих больных отечность нижних конечностей без наличия хронических заболеваний обусловлено гиподинамией – низкой физической активностью. Если же в анамнезе у пациента есть болезни сердечно-сосудистой системы (сердечная недостаточность, ишемическая болезнь сердца, артериальная гипертензия, венозная недостаточность), мочеполовой системы (почечная недостаточность, конкременты в почках или мочевыводящих путях), эндокринной системы (сахарный диабет, заболевания щитовидной железы), то отеки неизбежны.
Названные выше заболевания провоцируют появления отека тем, что:
Все эти изменения приводят к накоплению и задержке жидкости в тканях, что и позволяет диагностировать отек. Чаще всего ноги отекают при проблемах с сердцем и сосудами конечностей.
Симптомы отечности ног
Наиболее явный, наглядный симптом отека – это изменение объема и внешнего вида конечности. Наблюдается утолщение отдельных участков, чаще всего голеней, появление синюшных или красных пятен на коже. Из-за сдавливания нервных корешков может появляться постоянная тянущая боль не высокой интенсивности. На ощупь кожные покровы в месте отека прохладные, при пальпации чувствуется некоторая рыхлость, однако на вид кожа натянута тем сильнее, чем ярче выражен отек.
Диагностика включает в себя визуальный осмотр, пальпацию с надавливанием. При этом на коже образуется небольшое углубление, в норме исчезающее через 1 минуту. При подозрении на скрытый, генерализованный отек специалист может назначить УЗИ, анализы крови и мочи.
Лечение и профилактика отеков нижних конечностей
Если отечность ног у лежачего больного связана с каким-либо хроническим заболеванием, то основное лечение направлено на нормализацию работы страдающей системы органов (например, эндокринной). Если же причина отека – это только гиподинамия и длительное лежачее положение пациента, то ему назначают курс массажа, специальную диету, ЛФК и, по необходимости, прием мочегонных препаратов.
Для профилактики отеков у лежачих больных достаточно периодически менять положение пациента; подкладывать под ноги подушки или валики, так чтобы они располагались примерно под углом в 30 гр. относительно тела; следить за чистотой его постельного белья (важно отсутствие складок на нем), регулярно делать пассивную гимнастику. Гимнастика может включать в себя такие упражнения, как сгибание ног в коленях, круговые движения голеностопа, приподнимание ног. Полезно будет ограничить употребление соли и жидкости.
Постинсультный болевой синдром
В статье рассматриваются клинические проявления, особенности диагностики и лечения постинсультной боли. Структура постинсультного болевого синдрома гетерогенна и может включать в себя в разных комбинациях центральную постинсультную боль, спастическую боль
The article covers clinical manifestations, features of diagnostics and treatment of post-stroke pain. The structure of post-stroke pain syndrome is heterogeneous and can include, in different combinations, central post-stroke pain, spastic pain, humeral pain, tension headache and complex regionar pain syndrome. Complicated nature of post-stroke pain requires complex long-term therapy.
В 1906 г. J. J. Dejerine и G. Raussy [1] впервые дали развернутую клиническую характеристику болевому синдрому после перенесенного инсульта. Синдром Дежерина–Русси (центральный или таламический болевой синдром), представлял собой интенсивную непереносимую боль у пациентов с инфарктом таламуса, который включал: острые жгучие боли по гемитипу, снижение всех видов чувствительности, гиперпатию, гемипарез, легкую гемиатаксию, мышечную дистонию. Наряду с двигательными и сенсорными расстройствами такой пациент также испытывает выраженные когнитивные нарушения и депрессию [2]. При этом считается, что тяжесть испытываемой боли коррелирует с тяжестью когнитивных нарушений и депрессии [3]. Постинсультная боль может стать причиной суицидальных попыток. Развитие постинсультной боли отмечается у 12–55% пациентов. Обычно болевой синдром развивается в течение 3–6 месяцев после инсульта [4], однако нередки случаи появления боли и в течение первого месяца. Постинсультный болевой синдром с точки зрения патогенеза является гетерогенным, и в его структуре можно выделить центральную боль, постинсультную боль, боль, связанную со спастичностью, боль в плече, головные боли напряжения, комплексный регионарный болевой синдром.
Долгое время развитие центральной постинсультной боли связывали только с поражением таламуса. Однако внедрение в современную клиническую практику методов нейровизуализации позволило установить, что центральная постинсультная боль развивается как при поражении таламуса, так и вне таламических структур. Центральная постинсультная боль может возникнуть при поражении соматосенсорного анализатора на любом уровне — коры головного мозга, ядер таламуса, структур продолговатого и спинного мозга. По данным эпидемиологических исследований центральная постинсультная боль развивается у 1–12% пациентов. Ряд авторов считает, что ишемический инсульт чаще приводит к развитию центральной боли, чем геморрагический инсульт [5]. Центральная постинсультная боль относится к группе невропатических болевых синдромов и по определению экспертов Международной ассоциации по изучению боли (The International Association for the Study of Pain, IASP) является прямым следствием поражения или заболевания центральных отделов соматосенсорной системы [6].
Наиболее часто цитируемой гипотезой о природе центральной невропатической боли является концепция Хэда и Холмса о нарушении тормозного влияния лемнисковой соматосенсорной системы на восходящую палеоспиноталамическую систему [7]. Более поздние гипотезы о механизмах формирования центральной боли по существу являются детализацией концепции Хэда и Холмса о взаимодействии «специфических» латеральных и «неспецифических» медиальных структур мозга. Например, Л. А. Орбели (1935) [8] придавал важное значение в механизмах развития центральной боли нарушению баланса между лемнисковой и экстралемнисковой системами мозга. K. Winther (1972) [9] существенное место отводит нарушению афферентного взаимодействия между импульсными потоками эпикритической и протопатической боли. Электрофизиологические исследования, проведенные у пациентов с центральными болевыми синдромами, позволили высказать предположение, что гиперактивация нейронов медиального таламуса при повреждении латеральных таламических ядер происходит через ретикулярное таламическое ядро [10, 11]. Согласно гипотезе об ограничении термосенсорного входа [12], центральная боль возникает вследствие снижения холодового тормозного влияния на процессы обработки болевой информации. Предположение автора основывается на том, что при центральных болевых синдромах снижение температурной чувствительности происходит раньше, чем болевой, а в ряде случаев является единственным сенсорным дефицитом. В большинстве случаев пациенты с центральным болевым синдромом испытывают жгучие или леденящие боли в зоне снижения температурной чувствительности, при этом степень боли пропорциональна температурной гипестезии.
Повреждение центральных структур соматосенсорной системы приводит к нарушению механизмов контроля возбудимости ноцицептивных нейронов в центральной нервной системе и изменяет характер взаимодействия в системах, осуществляющих регуляцию болевой чувствительности. Вследствие нарушения тормозных и возбуждающих процессов развивается центральная сенситизация ноцицептивных нейронов с длительной самоподдерживающейся активностью. Повышение возбудимости и реактивности ноцицептивных нейронов при центральном болевой синдроме наблюдается в дорсальном роге спинного мозга, таламических ядрах и соматосенсорной коре большого мозга.
Центральная постинсультная боль может иметь ограниченную зону и локализоваться в какой-либо части тела или распространяться по гемитипу. У пациентов с поражением ствола мозга боль может быть ограничена половиной лица или локализоваться на противоположной стороне туловища или конечностей [2]. Распределение боли по гемитипу характерно для таламического поражения.
Представленность центральной постинсультной боли полностью или частично соответствует локализации чувствительных нарушений и соотносится с областью цереброваскулярного поражения [13]. Примерно 80% центральной постинсульной боли приходится на поражение париетальной коры [14]. Для центральной постинсультной боли характерно сочетание негативных и позитивных сенсорных феноменов в области локализации боли [15]. Расстройства температурной (холодовой) и болевой чувствительности отмечаются более чем у 90% пациентов, в то время как нарушение других видов чувствительности (тактильной, вибрационной) встречается реже [16]. Одновременно в болезненной зоне диагностируется аллодиния, гипералгезия, гиперпатия. У одного больного могут наблюдаться несколько типов болевых ощущений. Постоянная спонтанная боль описывается чаще как жгучая, покалывающая, холодящая и давящая, а периодическая боль носит разрывающий и стреляющий характер [4]. Интенсивность боли может варьировать в течение дня, под воздействием провоцирующих факторов. Основными факторами, приводящими к усилению болевого синдрома, могут быть холод, эмоциональный стресс, физическая нагрузка, усталость, изменение погоды. Тревожно-депрессивная симптоматика усугубляет течение болевого синдрома. Боль может снижаться при отдыхе, отвлечении внимания, исчезает во сне. Многим пациентам приносит облегчение тепло.
Многие пациенты после инсульта также испытывают «спастическую» боль [17]. Проспективное обсервационное исследование продемонстрировало тесную связь между развитием спастичности и боли. У 72% пациентов со спастичностью развивается боль, при этом только 1,5% больных без спастичности испытывают боль [18].
В настоящее время считается, что постинсультная спастичность является отражением сочетанного поражения пирамидных и экстрапирамидных структур головного мозга, приводящего к снижению тормозных влияний преимущественно на α-мотонейроны спинного мозга [19]. Развитие спастичности ухудшает двигательные функции, способствует развитию контрактуры и может сопровождаться болезненными мышечными спазмами [20]. Спастическая дистония и боль приводят к снижению функциональных возможностей больных и их реабилитации. Риск развития спастичности выше у пациентов с выраженным парезом, низкими баллами по шкалам Бартеля, постинсультной центральной болью и сенсорным дефицитом. Ведущую роль в лечении постинсультной спастичности имеет лечебная гимнастика, которая должна начинаться уже с первых дней развития инсульта и быть направлена на тренировку утраченных движений, самостоятельное стояние и ходьбу, а также профилактику прогрессирования спастичности и развития контрактур. В клинической практике для лечения постинсультной спастичности наиболее часто используются миорелаксанты (толперизон, тизанидин, баклофен), применение которых может улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить эффект лечебной физкультуры и предупредить развитие контрактур.
В настоящее время получены прямые доказательства того, что миорелаксирующий эффект толперизона связан не только с торможением активности потенциал-зависимых Na+-каналов, но и снижением выброса возбуждающих нейромедиаторов. В частности, на модели изолированного нерва [21] было установлено, что добавление толперизона в инкубируемую среду в дозе 100 µмоль/л снижает проницаемость ионов натрия на 50%. Сравнительное изучение влияния толперизона и лидокаина на семь типов потенциал-зависимых натриевых каналов показало, что толперизон, также как и лидокаин, оказывает блокирующее действие на активность натриевых каналов, однако степень блокирования у толперизона выражена в меньшей степени. Значительные различия между двумя препаратами в восстановлении активности натриевых каналов были продемонстрированы для трех типов натриевых каналов — Nav1.3, Nav1.5 и Nav1.7, не имеющих отношения к проведению болевой импульсации, в то время как продолжительность инактивации для каналов типа Nav1.8, имеющих отношение к ноцицептивной импульсации, у лидокаина и толперизона была схожей [22].
Исследования, проведенные на клетках ганглиев задних корешков, обнаружили, что толперизон угнетает потенциал-зависимую натриевую проводимость в концентрациях, в которых он ингибировал спинальные рефлексы. Более того, толперизон оказывал значительное воздействие на потенциал-зависимые кальциевые каналы. Эти данные позволили авторам утверждать, что толперизон реализует свое миорелаксирующее действие преимущественно путем ингибирования пресинаптического высвобождения нейромедиаторов из центральных терминалей афферентных волокон путем комбинированного влияния на потенциал-зависимые натриевые и кальциевые каналы [23].
Таким образом, толперизон, блокируя натриевые и кальциевые каналы в ноцицептивных афферентах, способен подавлять секрецию возбуждающих аминокислот из центральных терминалей первичных афферентных волокон, ослаблять частоту потенциалов действия мотонейронов и тем самым тормозить моно- и полисинаптические рефлекторные реакции в ответ на болевые стимулы. Такое действие толперизона обеспечивает эффективный контроль над спастичностью и мышечной болью.
Помимо действия на мышечный тонус, толперизон обладает способностью усиливать периферическое кровообращение. Данный эффект связан с блокадой альфа-адренорецепторов, локализованных в сосудистой стенке. Усиление кровообращения в мышце может быть дополнительным фактором, препятствующим сенситизации мышечных ноцицепторов при мышечной спастичности в условиях болевой импульсации.
Препарат селективно ослабляет патологический спазм мышц, не влияя в терапевтических дозах на нормальные сенсорные и двигательные функции центральной нервной системы (мышечный тонус, произвольные движения, координацию движений) и не вызывая седативного эффекта, мышечной слабости и атаксии. Толперизона гидрохлорид в отличие от других миорелаксантов вызывает мышечное расслабление без симптомов отмены, что было доказано в двойном слепом, плацебо-контролируемом исследовании, проведенном по критериям GCP [24].
В зависимости от доказанной эффективности и степени безопасности препараты были отнесены к той или иной линии терапии (табл.).
Как видно из табл., к препаратам первой линии терапии невропатической боли были отнесены габапентин, прегабалин, дулоксетин, венлафаксин и ТАД.
Авторы рекомендаций отмечают, что выбор того или иного препарата в каждом конкретном случае определяется совокупностью различных факторов, включающих возможные риски нежелательных явлений, наличия коморбидных расстройств (депрессии и нарушений сна), особенности лекарственных взаимодействий, возможность передозировки или лекарственных злоупотреблений.
В качестве терапии первой линии у пациентов с центральной постинсультной болью рекомендуется применение ТАД, прегабалина, габапентина. Селективные ИОЗСН, ламотриджин, опиоиды и их комбинации могут также использоваться при недостаточном эффекте препаратов первой линии.
Важным аспектом при лечении центральной постинсультной боли является четкая постановка реальных целей терапии боли и формирование адекватных ожиданий у пациента и родственников. Учитывая торпидный характер течения центральной постинсультной боли, целью терапии будет не устранение боли, а снижение интенсивности болевого синдрома, расширение функциональных возможностей пациента, улучшение качества жизни. Соблюдение режима дозирования и титрации препаратов, основанного на индивидуальной чувствительности больного, позволит сохранить комплаентное отношение больного к проводимой терапии. Низкие показатели эффективности фармакотерапии невропатической боли по данным ряда исследований, как правило, обусловлены неоптимальным дозированием и преждевременным прекращением приема назначенных лекарственных средств [27, 28]. Использование препаратов с различными механизмами действия при проведении комплексной фармакотерапии может способствовать повышению эффективности лечения. Врач также должен обеспечить постоянное мониторирование терапевтических и побочных эффектов. При мониторинге необходимо оценивать не только интенсивность боли, но и качественные сенсорные характеристики боли (жгучий характер, прострелы, дизестезии, аллодиния, онемение), качество сна, выраженность тревоги и депрессии, функциональные возможности и социальную адаптацию. При неэффективности консервативной медикаментозной и немедикаментозной терапии необходимо направить пациента в альгологические центры для решения вопроса об инвазивных методах лечения.
Литература
М. Л. Кукушкин, доктор медицинских наук, профессор
ФГБНУ НИИОПП, Москва
Дуэль с болезнью. Можно ли восстановиться после инсульта?
Подробнее о методах восстановления мы попросили рассказать врача-реабилитолога, кандидата медицинских наук Елену Васильевну ЛИТВИНОВУ (Нижний Новгород).
— После инсульта последствия неизбежны. Насколько они выражены?
— Заранее точно прогнозировать последствия инсульта практически невозможно. К полноценной жизни возвращаются менее 20% больных.
— От чего зависит степень и время восстановления нарушенных функций?
— Существуют две основные причины нарушения мозгового кровообращения: кровоизлияние в мозг в результате разрыва стенки сосуда (геморрагический инсульт) и закупорка просвета сосуда тромбом или атеросклеротической бляшкой (ишемический инсульт). И в том, и в другом случае гибнет какой-то очаг ткани мозга, лишенный притока свежей крови. А вокруг этого очага находится зона нейронов (нервных клеток), которая балансирует между жизнью и смертью. Так вот эти нейроны можно вернуть к жизни, посылая им поток двигательных импульсов. Когда больной после инсульта приступает к реабилитационным мероприятиям, эти нейроны начинают оживать, подключаются другие отделы мозга, которые берут на себя утраченные функции погибшего участка. После геморрагического инсульта (более тяжелого) качество восстановления может быть даже лучше, чем после ишемического поражения, поскольку зона инактивированных нейронов (готовых к восстановлению) в первом случае гораздо больше.
— При инсульте страдает только одна половина тела или обе?
— Если нарушение кровообращения произошло в правом полушарии мозга, то страдает левая половина тела. При катастрофе в левом полушарии те же явления отмечаются справа. Иногда гибнет та часть мозга, которая отвечает за движения всего тела, но это случается редко.
— Как родственники могут помочь больному в его восстановлении?
— На близких ложится большая ответственность за здоровье больного, от них в это время требуется максимум упорства, внимания, терпения, поскольку родственникам приходится скрупулезно выполнять все рекомендации врача.
Что нужно делать в первое время?
* Необходимо каждые 2 часа поворачивать больного то на один, то на другой бок.
* Несколько раз в день можно проводить легкий массаж спины (поглаживания, растирания), чтобы не было застойных явлений, прежде всего, в легких.
* Утром и вечером следует обмывать больного теплой водой с добавлением шампуня.
* При патологии в венах желательно на несколько часов бинтовать ноги больного, чтобы избежать застоя крови в нижних конечностях.
* Кровать больного лучше расположить так, чтобы пораженная часть тела находилась со стороны источника раздражения (двери, телевизора и т.д.). Это будет стимулировать движения в пораженных конечностях.
* Больным желательно лежать на том и на другом боку и несколько раз в день проводить так называемое ‘лечение положением’.
После инсульта мышцы вначале находятся в расслабленном состоянии, а затем их тонус начинает возрастать. Больная рука как бы ‘укорачивается’: плечо приведено к телу, кисть и пальцы согнуты, а больная нога как бы ‘удлинятся’: голень разогнута в коленном суставе, а стопа находится в положении подошвенного сгибания (‘отвисает’). При ходьбе пациенты обычно отводят ногу в сторону и описывают ей движения по кругу (‘косят’).
Для восстановления правильных движений с первых дней после инсульта и в течение всего реабилитационного периода проводится лечение положением, пассивная и активная гимнастика, дыхательные упражнения и другие способы борьбы с болезнью.
— Помогают ли при спазмах мышцы лекарственные препараты?
— Существует целая группа лекарств-миорелаксантов, которые действуют на спастические (спазмированные) мышцы. Но этими препаратами нельзя злоупотреблять. Дело в том, что полностью снимать спазм в мышцах нежелательно, так как в некоторых случаях при неполном восстановлении движений нормализация тонуса в ноге может привести к снижению её опорной функции. В результате у человека будет затруднен сам акт ходьбы.
Восстановительное лечение включает в себя комплекс различных методов: физиотерапевтическую, физическую реабилитацию, иглорефлексотерапию, занятия в бассейне и многое другое. Большую пользу больные ощущают от выполнения идеомоторных упражнений, которые делаются мысленно. При параличах и глубоких парезах пострадавшему показывают, какие движения возможны в суставах и предлагают, как минимум, 4 раза в день по 15 минут мысленно выполнять упражнения с каждой больной конечностью. Кстати, Валентин Иванович Дикуль начинал свое восстановление именно с упражнений, выполняемых мысленно. Проведенные исследования подтверждают тот факт, что при использовании идеомоторных упражнений реабилитация больного протекает более эффективно.
Нельзя забывать и о здоровых мышцах, которые также нужно тренировать. Чем лучше работает здоровая конечность, и тем быстрее идет восстановление в пострадавшей части тела.
Диагностика
После осмотра пациента и изучения истории болезни проводится магнитно-резонансная или компьютерная томография головного мозга. Такое исследование необходимо, поскольку проявления инсульта могут быть схожи с симптомами менингита, абсцесса головного мозга и многими другими заболеваниями.
После проведенных исследований устанавливается тип инсульта и подбираются наиболее подходящие методы лечения.
Кстати
В домашней аптечке желательно иметь глицин. Многие врачи считают этот препарат нейропротектором, то есть веществом, которое защищает ткань головного мозга.
При появлении неприятных ощущений (прежде всего слабости), впервые появившихся в руке или ноге, расстройстве речи нужно положить под язык 5 таблеток глицина. С помощью такой профилактики возможно в какой-то степени предотвратить мозговое нарушение.
Что такое микроинсульт
Под этим словом понимают временные нарушения мозгового кровообращения, которые сохраняются менее одних суток. Такие маленькие очаги ишемии головного мозга врачи называют лакунарными.
Происхождение микроинсультов связывают с изменением стенок и закупоркой очень мелких артерий, расположенных в глубине головного мозга.
Если лакунарный инсульт поразил зону, где нет важнейших нервных путей, то можно избежать неблагоприятных симптомов. Но, постепенно накапливаясь, микроинсульты ухудшают память, внимание, равновесие при ходьбе.
Если же лакунарный инсульт развился в зоне, где сконцентрированы важные проводящие пути от головного к спинному мозгу, то последствия окажутся очень тяжелыми. В этом случае признаком инсульта может быть мышечная слабость в руке или ноге.
Ставка на здоровье
После инсульта обязательно нужно вести здоровый образ жизни: отказаться от курения и злоупотребления алкоголем, перейти на антисклеротическую диету, подключить посильную физическую нагрузку.
Никотин ухудшает прогноз заболевания и в разы увеличивает вероятность возникновения повторного инсульта.
Питаться нужно продуктами с пониженным количеством холестерина. Это означает, что нельзя есть много животных жиров, которые содержатся в сливочном масле, майонезе, жирных сортах сыра, твороге, жирной свинине, сале, куриных яйцах (их можно употреблять не более двух в неделю).
Рекомендуется увеличить в рационе количество овощей, фруктов и растительных масел. Считается, что растительные масла вместе с овощами снижают уровень холестерина в крови.
Количество соли в рационе нужно уменьшить, так как она задерживает жидкость в организме и повышает артериальное давление.
Занятия физкультурой проводят под контролем артериального давления: при нагрузке верхняя цифра давления не должна быть выше 180-200.


.gif)
