Отёк ног (нижних конечностей)
Факторы возникновения отека ног (нижних конечностей)
Отек ног (нижних конечностей) может в равной степени влиять на обе ноги или быть более выраженным на одной нижней конечности. Часто отек ног вызывается несколькими факторами, такими как венозная недостаточность, ожирение или предыдущий забор подкожной вены для шунтирующих операций на сердце.
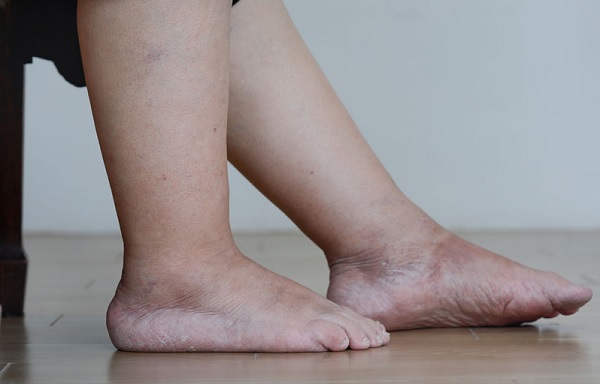
Отёк нижних конечностей
Отеки ног (нижних конечностей) могут возникать из-за повышенного давления в венах, местной травмы, воспалительных изменений, препятствия оттоку лимфатической жидкости, инфекции, низкого уровня белка в крови, ожирения, беременности, состояния задержки жидкости или воздействия лекарств. Высокое давление в венах ног приводит к тому, что жидкость, белки и клетки крови просачиваются через стенки мелких вен в мягкие ткани, особенно возле лодыжек. Это вызывает точечный отек, припухлость, которая оставляет временную вмятину на коже при компрессии обуви, носка или преднамеренном надавливании, например, при нажатии пальцем.
Отёк ног (нижних конечностей) и высокое венозное давление
Причины отёка ног (нижних конечностей) из-за повышенного венозного давления включают:
Варикоз и отечность ног
Другие причины появления отека ног (нижних конечностей)
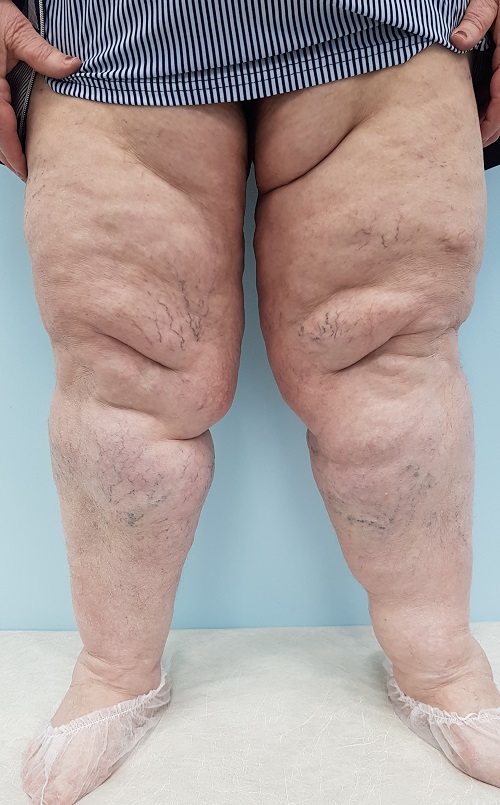
Отечность при липедеме
В зависимости от причин лимфедему разделяют на:
После венозной недостаточности ожирение является следующей по частоте причиной отека ног (нижних конечностей) в США, европейских странах и России. Абдоминальное ожирение частично препятствует венозному и лимфатическому оттоку от ног. Ожирение также ускоряет растяжение вен ног под действием силы тяжести, тем самым способствуя прогрессированию венозной недостаточности.
Вопросы пациентов об отеках на ногах (нижних конечностях)
Как избавиться от отёков ног (нижних конечностей)?
Избавиться от отёков ног в большинстве ситуаций вы сможете только при помощи доктора. Сначала необходимо выяснить причину отёка. Начать диагностику можно с визита к терапевту и флебологу.
Почему возникает отёк ног при варикозе?
Отёк ног при варикозе вен нижних конечностей возникает вследствие нарушения работы клапанного аппарата венозных сосудов. Это приводит к застою жидкости и формированию отёчности.
Как лечить отёк ног (нижних конечностей)?
Отёк ног лечится в зависимости от причины, его вызвавшей. Патология сердца, почек, венозной системы, травмы требуют своего, определённого лечения. Начать лечить отёк ног нужно с обращения к хорошему, внимательному доктору.
К какому врачу пойти, если отекают ноги?
Если отекают ноги, возможно, потребуется обратиться к нескольким специалистам. Начать можно с терапевта или кардиолога.
Отекла одна нога, как лечить?
Если у вас отекла одна нога необходимо срочно обратиться за медицинской помощью. Лучше посетить флеболога и ортопеда. Односторонняя отёчность нижней конечности может быть признаком такого грозного состояния, как тромбоз глубоких вен.
Отеки ног у лежачих больных

Различные классификации отеков как симптомов заболеваний
В норме отечность возникает после длительной нагрузки на ноги; спустя некоторое время, проведенное в неудобной обуви; при изменениях погодных условий (резкое потепление, изменение атмосферного давления). Такие отеки сигнализируют о некоторой дисфункции сердечно-сосудистой системы в период нагрузки. В норме подобные отеки исчезают самостоятельно спустя несколько часов отдыха.
У лежачих больных отечность нижних конечностей без наличия хронических заболеваний обусловлено гиподинамией – низкой физической активностью. Если же в анамнезе у пациента есть болезни сердечно-сосудистой системы (сердечная недостаточность, ишемическая болезнь сердца, артериальная гипертензия, венозная недостаточность), мочеполовой системы (почечная недостаточность, конкременты в почках или мочевыводящих путях), эндокринной системы (сахарный диабет, заболевания щитовидной железы), то отеки неизбежны.
Названные выше заболевания провоцируют появления отека тем, что:
Все эти изменения приводят к накоплению и задержке жидкости в тканях, что и позволяет диагностировать отек. Чаще всего ноги отекают при проблемах с сердцем и сосудами конечностей.
Симптомы отечности ног
Наиболее явный, наглядный симптом отека – это изменение объема и внешнего вида конечности. Наблюдается утолщение отдельных участков, чаще всего голеней, появление синюшных или красных пятен на коже. Из-за сдавливания нервных корешков может появляться постоянная тянущая боль не высокой интенсивности. На ощупь кожные покровы в месте отека прохладные, при пальпации чувствуется некоторая рыхлость, однако на вид кожа натянута тем сильнее, чем ярче выражен отек.
Диагностика включает в себя визуальный осмотр, пальпацию с надавливанием. При этом на коже образуется небольшое углубление, в норме исчезающее через 1 минуту. При подозрении на скрытый, генерализованный отек специалист может назначить УЗИ, анализы крови и мочи.
Лечение и профилактика отеков нижних конечностей
Если отечность ног у лежачего больного связана с каким-либо хроническим заболеванием, то основное лечение направлено на нормализацию работы страдающей системы органов (например, эндокринной). Если же причина отека – это только гиподинамия и длительное лежачее положение пациента, то ему назначают курс массажа, специальную диету, ЛФК и, по необходимости, прием мочегонных препаратов.
Для профилактики отеков у лежачих больных достаточно периодически менять положение пациента; подкладывать под ноги подушки или валики, так чтобы они располагались примерно под углом в 30 гр. относительно тела; следить за чистотой его постельного белья (важно отсутствие складок на нем), регулярно делать пассивную гимнастику. Гимнастика может включать в себя такие упражнения, как сгибание ног в коленях, круговые движения голеностопа, приподнимание ног. Полезно будет ограничить употребление соли и жидкости.
Препараты после инсульта
Ежегодно инсульт случается почти у полумиллиона человек. Более половины из них теряют бытовую независимость. Поэтому правильный подбор препаратов, борьба с последствиями и реабилитация становится важной задачей на многие годы.
Инсульт и реабилитация
Инсульт — острое заболевание, которое связано с нарушением кровообращения и проявляется такими симптомами со стороны нервной системы как:
Выделяют 2 основные формы инсульта:
Реабилитация после инсульта начинается как можно раньше. Комплексный подход в лечении сочетает в себе лекарственную терапию, физиопроцедуры, тренировки по восстановлению утраченных функций. В фармакотерапии выделяют 3 основных направления:
Профилактика повторного инсульта
Причины, приведшие к возникновению инсульта, чаще всего никуда не исчезают и продолжают действовать на человека. От их силы и сочетаний зависит риск повторного инсульта. Профилактика повторного инсульта называется вторичной. Список состояний, на которые обращают внимание в первую очередь:
Соответственно необходима коррекция этих состояний и приведение их в норму для снижения риска повторного инсульта. Лекарственная терапия только часть лечения. Важны диета, физкультура, отказ от вредных привычек.
Антигипертензивные препараты
Артериальное давление рекомендуется снижать, даже если оно повышено совсем незначительно или в пределах нормы: «верхнее» 120-139 мм.рт.ст, «нижнее» 80-89 мм.рт.ст. Так снижение на 5 мм.рт.ст. помогает снизить развитие инсульта на 30%.

Преимущество одних групп антигипертензивных препаратов над другими не доказано. Врачу при назначении приходится учитывать индивидуальные особенности пациента, сочетаемость с другими препаратами, минимизацию побочных эффектов. При этом для пациентов после инсульта важно не только снизить давление, но и максимально его стабилизировать, пусть даже чуть выше целевых значений. Для этого используют:
Препараты препятствующие тромбообразованию
При различных аритмиях повышается риск тромбообразования и возникновение инсультов до 4 раз. Для профилактики этих состояний могут использоваться антикоагулянты и антиагреганты:
Прием этой группы препаратов обычно длительный, можно сказать, что пожизненный.
Статины
Помогают не только бороться с атеросклерозом, высокими цифрами холестерина, но и стабилизируют поверхность уже сформировавшихся бляшек, снижают уровень воспаления в сосудистой стенке, что также уменьшит риск тромбоза:
Борьба с последствиями
Лечение гипертонуса мышц
Спастичность мышц проявляется при попытке пассивного движения в конечности. Цели полностью убрать спазм может и не быть, так как некоторые пациенты используют это мышечное напряжение как элемент стабильности при движении. Проблему это представляет у лежачих пациентов, когда спазмы вызывают боль, мешает реабилитации и уходу.

Для местного устранения спазма внутримышечно могут вводиться препараты нейротоксинов:
Прием начинается с минимальной дозы препарата и постепенно увеличивается до достижения эффекта или до первых побочных явлений. Лечение этих симптомов помогает в лечебной физкультуре и предотвращает развитие контрактур в суставах.
Коррекция мозговых функций
Слабоумие может развиваться у примерно половины перенесших инсульт. В течение первых 6 месяцев риск деменции самый высокий, также он может сохраняться в течение нескольких лет.
Используются ноотропные и нейропротекторные препараты:
Лечение постинсультной депрессии
С постинсультной депрессией разной степени выраженности сталкивается 2/3 пациентов. Требования к антидепрессантам сочетают в себе минимум побочных эффектов, так как обычно есть множество других сопутствующих заболеваний. Также нужен легкий стимулирующий эффект, так как у большинства пациентов развивается астения. Для этой цели могут подойти селективные ингибиторы обратного захвата серотонина:
Эффект обычно наступает через 2 недели. Отменять препараты необходимо постепенно.
Постинсультные боли
Ощущения по типу жжения от ледяной воды возникают после поражения участков мозга, отвечающих за болевую чувствительность. Для лечения используют комбинации перечисленных выше антидепрессантов с антиковульсантами:
В дополнение к лекарствам может использоваться метод транскраниальной электростимуляции.
Патогенетическое лечение
К препаратам, влияющим на механизмы развития неврологических проблем в постинсультном периоде, можно отнести нейропротекторы и антиоксиданты:
Вывод
Список препаратов, которые, как может показаться, могут быть показаны после инсульта огромен. Важны не сами препараты по отдельности, а комплекс мероприятий. Вводить новые препараты или отменять должен доктор, чтобы лечение было эффективным и безопасным. Также желательно узнать прогноз и ставить реалистичные цели по восстановлению, так как объем поражения мозга может накладывать значительные ограничения независимо от интенсивности реабилитации.
Постинсультная спастичность
В России более миллиона больных, перенесших инсульт. Более чем у половины из них остаются после него двигательные нарушения, которые существенно снижают качество жизни и способствуют стойкой инвалидности (инвалидизации) пациентов [1]: чаще всего это гемип
В России более миллиона больных, перенесших инсульт. Более чем у половины из них остаются после него двигательные нарушения, которые существенно снижают качество жизни и способствуют стойкой инвалидности (инвалидизации) пациентов [1]: чаще всего это гемипарез или монопарез конечности с повышением мышечного тонуса по типу спастичности [1, 2, 9, 20].
Патогенез постинсультной спастичности
Спастичность выявляется при исследовании пассивных движений в паретичной конечности как повышенное сопротивление (сокращение) мышцы при ее быстром растяжении. Развитие спастичности при центральном парезе конечности связывается со снижением тормозных влияний на спинальные мотонейроны и интернейроны, что приводит к увеличению числа импульсов, достигающих альфа-мотонейронов в ответ на растяжение мышцы. Снижение тормозных влияний на спинальные мотонейроны и интернейроны объясняется комбинированным поражением пирамидных и экстрапирамидных путей внутри головного мозга вследствие инсульта, при этом важную роль в развитии спастичности отводят повреждению кортико-ретикуло-спинального тракта [2, 16, 20].
В экспериментальных исследованиях показано, что изолированное поражение пирамидного пути не вызывает спастичности, а приводит лишь к парезу в дистальных отделах конечностей, особенно утрате тонких движений руки. В случаях поражения головного мозга при инсульте обычно возникает поражение не только пирамидного пути, но и других двигательных путей, таких как кортико-ретикуло-спинальный тракт, что и сопровождается спастичностью. Поэтому постинсультная спастичность рассматривается как комбинированное поражение пирамидных и экстрапирамидных структур внутри головного мозга [2, 16, 20]. Экстрапирамидная система внутри головного мозга может быть повреждена вследствие поражения самих базальных ганглиев или приходящих либо исходящих от них путей.
В развитии церебральной спастичности при поражении головного мозга большую роль играет ослабление тормозных влияний преимущественно на альфа-мотонейроны, обеспечивающих движение антигравитационных мышц; это объясняет появление характерных проявлений постинсультного спастического гемипареза: приведение плеча, сгибание руки в локтевом и лучезапястном суставах, приведение бедра, разгибание колена и подошвенное сгибание в голеностопном суставе [2, 16, 20].
У больных инсультом спастичность обычно нарастает в паретичных конечностях в течение нескольких недель и месяцев, сравнительно редко (чаще всего при восстановлении двигательных функций) наблюдается спонтанное уменьшение спастичности. Во многих случаях у больных инсультом спастичность ухудшает двигательные функции, способствует развитию контрактуры и деформации конечности, затрудняет уход за обездвиженным больным и иногда сопровождается болезненными мышечными спазмами [2, 5, 9, 11, 20].
Если постинсультный парез сохраняется в течение длительного времени (несколько месяцев и более), то могут возникнуть структурные изменения сегментарного аппарата спинного мозга (укорочение дендритов альфа-мотонейронов и коллатеральный спрутинг афферентных волокон, входящих в состав задних корешков), которые способствуют прогрессированию спастичности [16]. Также развиваются вторичные изменения в паретичных мышцах, сухожилиях и суставах, которые усиливают двигательные расстройства и сопротивление, возникающее в мышце при ее растяжении, что необходимо учитывать при оценке мышечного тонуса в паретичных или парализованных конечностях [16, 20].
Восстановление утраченных двигательных функций максимально в течение двух-трех месяцев с момента инсульта, в дальнейшем темпы восстановления снижаются значительно. Через год после развития инсульта маловероятно уменьшение степени пареза, однако возможно улучшение двигательных функций и уменьшение инвалидности путем тренировки равновесия и ходьбы, использования специальных приспособлений для передвижения и снижения спастичности в паретичных конечностях [1, 2, 9, 11, 20].
Лечение постинсультной спастичности
Лечение постинсультной спастичности направлено на улучшение функциональных возможностей паретичных конечностей, ходьбы, самообслуживания больных. К сожалению, в части случаев возможности лечения спастичности ограничиваются только уменьшением боли и дискомфорта, связанного с высоким мышечным тонусом, облегчением ухода за парализованным пациентом или устранением имеющегося косметического дефекта, вызванного высоким мышечным тонусом [2, 11, 20].
Один из наиболее важных вопросов, который приходится решать при ведении больного с постинсультной спастичностью, сводится к следующему: ухудшает или нет спастичность функциональные возможности больного? В целом, функциональные возможности конечности у больного с постинсультным парезом конечности хуже при наличии выраженной спастичности, чем при ее легкой степени. Вместе с тем у части больных при выраженной степени пареза спастичность в мышцах ноги может облегчать стояние и ходьбу, а ее снижение может привести к ухудшению двигательной функции и даже к падениям [2, 11, 16, 20]. Перед лечением постинсультной спастичности необходимо определить возможности лечения у конкретного больного (улучшение двигательных функций, уменьшение болезненных спазмов, облегчение ухода за пациентом и др.) и обсудить их с пациентом и/или его родственниками. Возможности лечения во многом определяются сроками с момента заболевания и степенью пареза, наличием когнитивных расстройств [2, 11, 16, 20]. Чем меньше сроки с момента развития инсульта, вызвавшего спастический парез, тем более вероятно улучшение от лечения спастичности, потому что оно может привести к существенному улучшению двигательных функций, предотвратив формирование контрактур и повысив эффективность реабилитации в период максимальной пластичности центральной нервной системы. При длительном сроке заболевания менее вероятно существенное улучшение двигательных функций, однако можно значительно облегчить уход за больным и снять дискомфорт, вызванный спастичностью. Чем меньше степень пареза в конечности, тем более вероятно, что лечение спастичности улучшит двигательные функции [16, 20].
Лечебная гимнастика представляет наиболее эффективное направление ведения больного с постинсультным спастическим гемипарезом, она направлена на тренировку движений в паретичных конечностях и предотвращение контрактур [1, 2, 16, 20]. Однако больным, имеющим выраженную спастичность в сгибателях верхних конечностей, не следует рекомендовать интенсивные упражнения, которые могут значительно усилить мышечный тонус (например, сжимание резинового кольца или мяча, использование эспандера для развития сгибательных движений в локтевом суставе).
В качестве методов физиотерапии используются лечение положением, обучение пациентов стоянию, сидению, ходьбе (с помощью дополнительных средств и самостоятельно), бинтование конечности, применение ортопедических аппаратов, тепловые воздействия на спастичные мышцы, а также электрическая стимуляция определенных мышечных групп (например, разгибателей пальцев кисти или передней большеберцовой мышцы [4]).
Массаж мышц паретичных конечностей, имеющих высокий мышечный тонус, возможен только в виде легкого поглаживания. Напротив, в мышцах-антагонистах можно использовать растирание и неглубокое разминание в более быстром темпе.
Иглорефлексотерапия относительно часто используется в нашей стране в комплексной терапии больных, имеющих постинсультный спастический гемипарез, однако контролируемые исследования, проведенные за рубежом, не показывают существенной эффективности этого метода лечения [8].
У больных, перенесших инсульт и имеющих локальную спастичность в паретичных мышцах, можно использовать ботулинический токсин типа А или ботулотоксин (Ботокс, Диспорт). Использование ботулинического токсина показано, если у больного, перенесшего инсульт, имеется мышца с повышенным тонусом без контрактуры, а также отмечаются боль, мышечные спазмы, снижение объема движений и нарушение двигательной функции, связанные со спастичностью этой мышцы [2–4, 17, 20]. Действие ботулинического токсина при внутримышечном введении вызвано блокированием нервно-мышечной передачи, обусловленным подавлением высвобождения нейромедиатора ацетилхолина в синаптическую щель.
Клинический эффект после инъекции ботулинического токсина отмечается спустя несколько дней и сохраняется в течение 2–6 месяцев, после чего может потребоваться повторная инъекция. Лучшие результаты отмечаются при использовании ботулинического токсина в ранние сроки (до года) с момента заболевания и легкой степени пареза конечности. Применение ботулинического токсина может быть особенно эффективно в тех случаях, когда имеется эквино-варусная деформация стопы, вызванная спастичностью задней группы мышц голени, или высокий тонус мышц-сгибателей запястья и пальцев, ухудшающий двигательную функцию паретичной руки [20]. В контролированных исследованиях доказана эффективность Диспорта при лечении постинсультной спастичности в руке [3].
В качестве побочных эффектов от использования ботулотоксина могут быть кожные изменения и боли в месте инъекции. Они обычно самостоятельно регрессируют в течение нескольких дней после инъекции. Возможна значительная слабость мышцы, в которую введен ботулотоксин, а также слабость в мышцах, расположенных близко к месту инъекции, локальная вегетативная дисфункция. Однако мышечная слабость обычно компенсируется деятельностью агонистов и не приводит к ослаблению двигательной функции. Ограничение широкого применения ботулинического токсина в клинической практике во многом вызвано его высокой стоимостью.
Хирургические операции для уменьшения постинсультной спастичности используются редко, они возможны на четырех уровнях — на головном мозге (электрокоагуляция бледного шара, вентролатерального ядра таламуса или мозжечка), спинном мозге (селективная задняя ризотомия), периферических нервах (рассечение периферических нервов) и мышцах или их сухожилиях [2, 16, 20].
С помощью специальной помпы интратекально при постинсультной спастичности может использоваться баклофен [10, 13, 19]. Использование баклофеновой помпы в сочетании с лечебной гимнастикой, физиотерапией улучшает скорость и качество ходьбы больных с постинсультной спастичностью, способных к самостоятельному передвижению [10]. Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств [19]. Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт [13]. Широкое применение этого метода терапии в клинической практике ограничивает его высокая стоимость.
Лечение пероральными антиспастическими средствами
В клинической практике для лечения постинсультной спастичности наиболее часто используются пероральные антиспастические лекарственные средства [5, 11, 12, 16]. Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры и вследствие этого предупредить развитие контрактур. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты [2, 5, 11, 20]. Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта. Антиспастические средства обычно не комбинируют. В нашей стране для лечения постинсультной спастичности наиболее часто используют баклофен (Баклосан), тизанидин (Сирдалуд) и толперизон (Мидокалм).
Баклофен (Баклосан) оказывает антиспастическое действие преимущественно на спинальном уровне. Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК); он связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности. Препарат оказывает также умеренное центральное анальгезирующее действие. Баклофен используется при спинальной (спинальная травма, рассеянный склероз) и церебральной спастичности различного генеза [5, 11, 16]. Начальная доза составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта; препарат принимают во время еды. Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные эффекты чаще проявляются сонливостью, головокружением в начале лечения, хотя в дальнейшем могут ослабевать. Иногда возникают тошнота, запор, диарея, артериальная гипотония; требуется осторожность при лечении больных пожилого возраста, перенесших инсульт.
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Тизанидин (Сирдалуд) обладает также умеренным центральным анальгезирующим действием. Препарат эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах [5, 11, 12, 15, 16, 20]. Начальная доза препарата составляет 2–6 мг/сут в один или три приема, средняя терапевтическая доза — 12–24 мг/сут, максимальная доза — 36 мг/сут. В качестве побочных эффектов могут возникать сонливость, сухость во рту, головокружение и незначительное снижение артериального давления, что ограничивает использование препарата при постинсультной спастичности [15].
Толперизон (Мидокалм) — мышечный релаксант центрального действия, который близок к лидокаину по химической структуре и стабилизирует мембраны нервных клеток. Толперизон снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три приема. Около 40 лет толперизон успешно применялся при лечении спастичности различного генеза, были проведены небольшие исследования, показавшие его эффективность при церебральной спастичности [7, 14].
Недавно было проведено плацебо-контролируемое исследование [18], в котором показана эффективность, безопасность и хорошая переносимость толперизона у больных, перенесших инсульт и имеющих спастичность в паретичных конечностях. В многоцентровое исследование (два центра в Германии и один центр в Болгарии) было включено 120 больных (43 мужчины и 77 женщин) в возрасте от 20 до 78 лет (средний возраст — 63 года) с постинсультной спастичностью. Больные перенесли инсульт в сроки от 3 месяцев до 30 лет (в среднем 3,3 года с момента инсульта) и имели спастичность, выраженность которой достигала 2 баллов и более по шкале Эшуорта в одной или нескольких мышечных группах. У большинства (111 из 120) больных наблюдался гемипарез со спастичностью в верхней и нижней конечности, средняя степень спастичности составила 3 балла по шкале Эшуорта. По основным клиническим характеристикам группа больных, которые принимали толперизон, не отличалась от группы плацебо. В течение четырех недель больные получали толперизон или плацебо, доза которых подбиралась врачом для получения максимального эффекта и могла достигать от 300 до 900 мг толперизона. Далее больные продолжали принимать толперизон или плацебо в течение еще двух месяцев (восьми недель).
Главной целью исследования было изучение влияния толперизона на выраженность спастичности по шкале Эшуорта через 4 недели лечения (в сравнении с плацебо). Дополнительные цели исследования включали изучение влияния толперизона на ежедневную двигательную активность (по пятибалльной шкале), ходьбу в течение двух минут, максимальное расстояние при ходьбе (при спастичности в нижних конечностях), индекс Бартел, общее впечатление врача и больного о лечении.
Результаты проведенного исследования показали, что толперизон достоверно (р
В. А. Парфенов, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва