Влияние заместительной гормональной терапии препаратом Фемостон
Перед назначением ЗГТ всем женщинам проведено УЗИ малого таза, маммография и цитологическое исследование цервикальных мазков. Оценка антропометрических параметров (индекс массы тела — ИМТ, объем талии — ОТ, отношение объема талии к объему бедер — ОТ/ОБ) проводилась исходно и через каждые 3 мес на фоне приема Фемостона. Основные показатели углеводного обмена анализировались исходно, через 6 и 12 мес, по данным 2-часового орального глюкозотолерантного теста с 75 г глюкозы в комбинированной фазе лечения. При этом оценивались базальные уровни глюкозы и инсулина, толерантность к глюкозе, а также суммарная ответная реакция инсулина на глюкозную нагрузку по площади под кривой (ППК) «концентрация время».
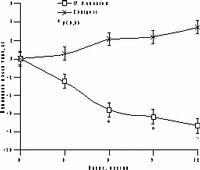
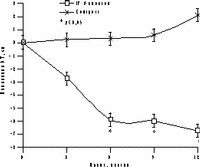
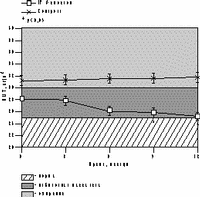
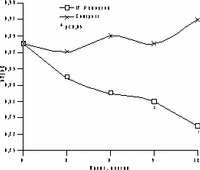
Достоверное снижение массы тела установлено уже через 6 мес терапии в среднем на 4,2±0,9 кг, а через год в среднем на 6,2±0,9 кг (рис. 1). Потеря массы тела происходила за счет уменьшения количества абдоминального жира, о чем свидетельствовали значительные изменения ОТ (на 6,2±0,5 см) и отношения ОТ/ОБ (с 0,88 до 0,78) через год терапии. ИМТ к концу года лечения достиг верхней границы нормы (рис. 1). В контрольной группе антропометрические показатели увеличились. Изменения углеводного обмена на фоне Фемостона заключались в выраженном снижении базальных уровней инсулина и инсулинорезистентности (в среднем на 51,3% и 29,8%, соответственно) при стабильных показателях толерантности к глюкозе (рис. 2). В контрольной группе уровни глюкозы натощак не изменились, а базальные уровни и ППК инсулина возросли.
|
Рис.1. Динамика массы тела и антропометрических параметров на фоне Фемостона у женщин с менопаузальным метаболическим синдромом.
а — масса тела; б — ИМТ; в — ОТ; г — ОТ/ОБ.
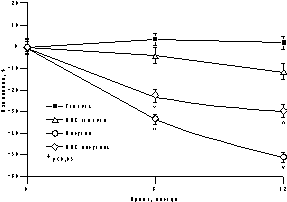 |
Рис. 2.Динамика показателей углеводного обмена на фоне Фемостона.
Полученные на фоне Фемостона результаты об изменении массы тела, существенно отличаются от данных других исследований, в которых сообщается лишь о незначительном уменьшении массы тела [10, 11]. Это объясняется тем, что в нашем исследовании участвовали пациентки со значительной прибавкой массы тела после менопаузы, а в литературе приводятся сведения об изменении массы тела на фоне ЗГТ у женщин с нормальным весом либо со значительным разбросом его значений по группе обследуемых. Падение базальных уровней инсулина и инсулинорезистентности под влиянием Фемостона сочеталось с достоверным снижением массы тела и степени абдоминального ожирения. Поскольку метаболические нарушения могут быть полностью обратимы при нормализации массы тела, не исключено, что улучшение углеводного обмена обусловлено дополнительным (помимо эффекта ЗГТ) влиянием потери массы тела, а также небольшой продолжительностью периода дефицита эстрогенов (и обменных нарушений, соответственно) у женщин в перименопаузе [11].
И.Г. Шестакова
Научный центр акушерства, гинекологии и перинатологии РАМН, Москва
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
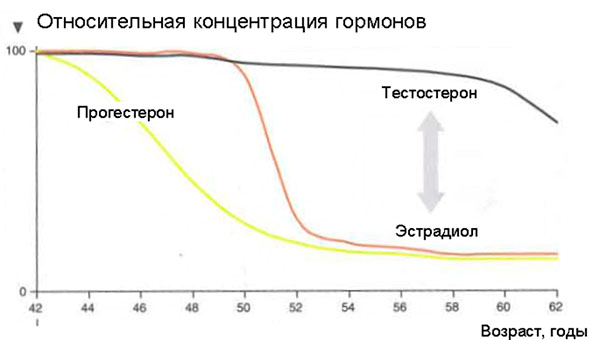
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
Препараты для монофазной терапии – когда месячные отсутствуют
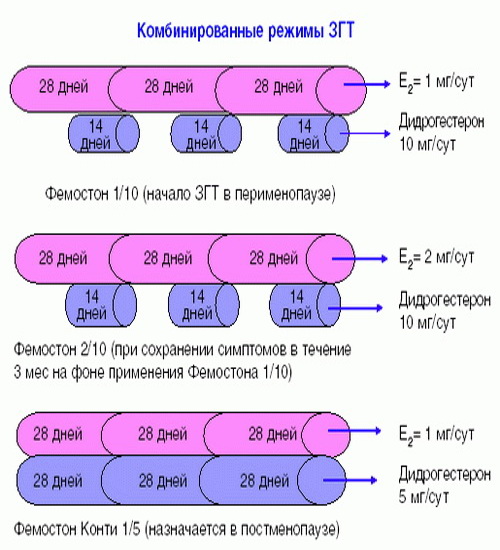
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
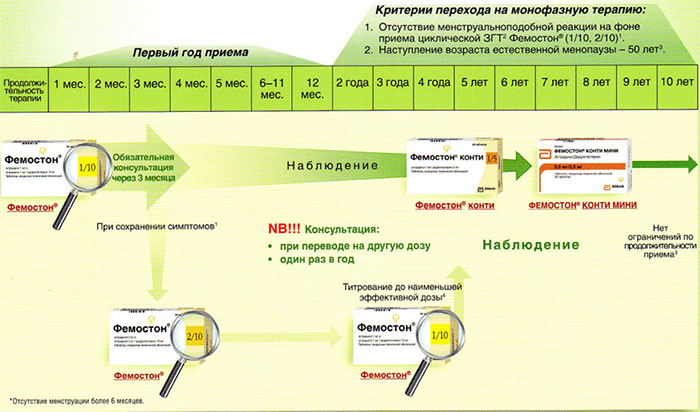
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
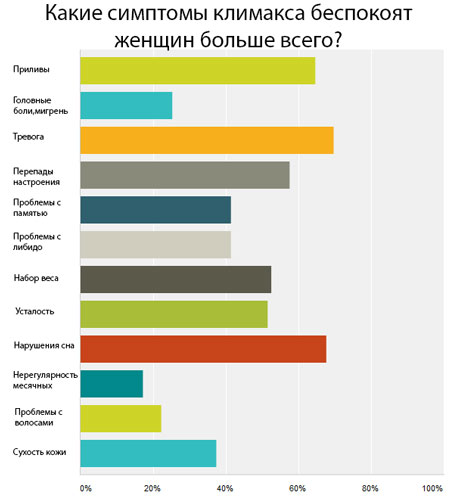
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Заместительная гормонотерапия — как не поправиться
Диетотерапия (с применением специализированных продуктов питания смесей белковых композитных сухих, витаминно-минеральных комплексов) не заменит пациентке, находящейся в климактерическом периоде, лекарственные препараты, назначенные врачом. В первую очередь речь идет о заместительной гормональной терапии, которая в настоящее время считается золотым стандартом поддержки женщины в этот важный период ее жизни. Однако данный вид лечения в настоящее время не вызывает стопроцентного доверия у большинства российских женщин. Страх набрать вес — первое, что останавливает их от принятия гормонотерапии.
Результаты научных исследований последних лет свидетельствуют о том, что заместительная гормональная терапия (ЗГТ) является основным методом лечения и во время перии постменопаузы назначается с целью профилактики и лечения климактерических нарушений.
В этот период жизни женщины значение ЗГТ в коррекции метаболических нарушений, в снижении риска развития сахарного диабета и сердечно-сосудистых заболеваний очень высока. Метаанализ 107 различных исследований влияния ЗГТ на состояние здоровья (1966–2004 гг.) установил снижение частоты висцерального ожирения (на 6,8 %), индекса инсулинорезистентности у женщин без сахарного диабета (на 12,9 %) и с сахарным диабетом (на 35,8 %); уровня глюкозы натощак (на 11,5 %); уровня атерогенных липидов (на 15,7 %); липопротеииа А (на 25 %); фибриногена (на 25 %); ингибитора активации плазминогена (на 25,9 %).
В 28 из 30 исследованиях за последние 20 лет продемонстрировано снижение инвалидизации и смертности от ишемической болезни сердца у женщин, принимающих ЗГТ в постменопаузальный периоде. Метаанализ этих исследований показал, что степень снижения риска инфаркта миокарда, мозгового инсульта и фатальных осложнений ишемической болезни сердца у женщин, получавших ЗГТ, составлял от 35 до 50 %. ЗГТ была одинаково эффективной после наступления как физиологической менопаузы, так и хирургической.
Между тем в современном обществе все еще распространены мифы об огромном количестве побочных эффектов проведения заместительной гормональной терапии.
ЗГТ и увеличение веса
Наиболее распространенной причиной отказа от ЗГТ является боязнь «привыкания» к гормональному лечению и прибавка массы тела.
Известно, что физиологический дефицит эстрогенов характеризуется наряду со снижением периферической чувствительности к инсулину гиперинсулинемией и частым нарушением толерантности к глюкозе. Повышенный уровень инсулина (анаболического гормона) вызывает многие биологические эффекты, среди которых отмечается влияние и на жировую ткань (торможение липолиза, контроль секреции лептина) и повышение аппетита. Поэтому, если женщина в период менопаузы не принимает ЗГТ, контроль за питанием и двигательной активностью в этот период крайне необходим.
Благоприятное влияние ЗГТ включает снижение концентрации инсулина и гликемии, усиление синтеза ГСПГ, вследствие чего снижается концентрация тестостерона и уменьшается андрогенный анаболический вклад в менопаузальный метаболический синдром, улучшаются антропометрические параметры, показатели липидного и углеводного обмена.
В ряде исследований нового тысячелетия не выявлено существенного влияния ЗГТ на изменение массы тела, как считалось ранее. Выполнено достаточно большое количество исследований по изучению влияния ЗГТ на массу тела. Результаты этих исследований едины в подавляющем большинстве случаев: при использовании натуральных эстрогенов ЗГТ не оказывает значимых изменений массы тела. Более того, обзор литературы [1, 2, 3] показывает, что вовремя начатая ЗГТ не только не способствует повышению массы тела, которое возникает в этот период вследствие резкого снижения уровня прогестерона и относительного преобладания андрогенов над эстрогенами, но и препятствует неблагоприятному перераспределению жировой ткани «по мужскому типу», т. е. преимущественно в абдоминально-висцеральной области.
Поправилась на фемостоне что делать
Многие женщины, приближаясь к возрасту менопаузы, отмечают необъяснимую прибавку веса и увеличение объема жировой ткани, особенно в области живота, несмотря на все попытки похудеть. Причем усилия, направленные на снижение веса, которые успешно “работали” ранее, зачастую оказываются неэффективными. В клинической практике увеличение объема жировой ткани в области живота – нередко единственная жалоба женщин в перименопаузе. Большинство из них воспринимает прибавку веса на 5–10 кг как обязательное проявление переходного возраста. Особенно остро увеличение веса ощущают женщины, для которых их физическая форма связана с профессией: спортсменки, балерины, танцовщицы. Как известно, женщины этих профессий годами привыкают соблюдать диету, следить за весом и уровнем физической активности. Именно поэтому их удивляет увеличение веса при неизменном образе жизни, который формировался годами.
Объяснение феномена прибавки веса в климактерии стало возможным в последние 10–15 лет после проведения ряда крупных исследований.
Классификация и клиническое значение увеличения массы тела у женщин
По статистике, у женщин ожирение встречается чаще, чем у мужчин. Причем с возрастом частота ожирения у них прогрессирует, особенно после менопаузы [1, 2].
По определению, ожирение – избыток жировой ткани, а точнее триглицеридов в жировых клетках – адипоцитах. При этом увеличивается их объем, хотя не исключается и формирование новых адипоцитов при стимуляции различными веществами, в частности глюкокортикоидами.
Наличие ожирения определяют по индексу массы тела (ИМТ) – отношению массы тела в килограммах к возведенному в квадрат росту в метрах. Согласно классификации ВОЗ, ИМТ > 25 кг/м 2 свидетельствует об избыточном весе, а ИМТ ≥ 30 кг/м 2 – об ожирении. ИМТ не дает информации о количестве и характере распределения жировой ткани. Для получения полной картины ожирения используются рентгеновская денситометрия и магнитно–резонансная томография. В клинической практике наиболее простой и распространенный способ – вычисление отношения окружности талии (ОТ) к окружности бедер (ОБ) – ОТ/ОБ. При ОТ/ОБ > 0,8 классифицируют андроидное (абдоминальное) ожирение, когда жир накапливается преимущественно в области передней брюшной стенки. Выделяют подкожно–абдоминальное и висцеральное ожирение (избыток жира в висцерально–мезентериальной области). При ОТ/ОБ 30 кг/м 2 частота артериальной гипертензии составляет 32 %, а при ИМТ 2 – 16 %; причем прибавка массы тела на 10 кг приводит к увеличению систолического артериального давления на 3, а диастолического на 2,3 мм рт. ст. [3–5]. При ИМТ от 24 до 24,9 кг/м 2 риск сахарного диабета у женщин выше в 5 раз, а при ИМТ 31 кг/м 2 – в 40 раз по сравнению с пациентками с нормальной массой тела [6].
Заболевания второй категории – следствия ожирения как такового: остеоартрит, обструктивное апноэ (храп) во сне, нарушения психологического плана. Подсчитано, что при увеличении массы тела на один килограмм риск остеоартрита коленного и пястно–запястного суставов возрастает на 9–13 %. Обструктивным апноэ во сне страдают 60–70 % людей с ожирением, особенно абдоминальным. Клинически обструктивное апноэ во сне может ассоциироваться с повышенной сонливостью днем, сердечной аритмией, ишемией миокарда, синдромом гипервентиляции, легочной гипертензией, сердечной недостаточностью и инсультом.
Многие исследователи обращают внимание на широкоизвестный факт, что снижение массы тела значительно снижает риск связанных с ожирением заболеваний. Так, потеря 10 кг веса приводит к снижению риска артериальной гипертензии на 26 %, при потере 20 кг риск сахарного диабета уменьшается на 87 %, а при снижении массы тела на 5 кг за 10 лет шанс развития остеоартрита коленного сустава уменьшается на 50 % [5].
Механизмы увеличения массы тела в менопаузе
Опубликованные сведения об изменении массы тела и распределении жировой ткани после выключения функции яичников немногочисленны. Быстрая прибавка массы тела в перименопаузе происходит примерно у 60 % женщин. По данным Исследования здоровых женщин, в первые три года после менопаузы масса тела в среднем увеличивается на 2,3 кг (у 20 % женщин – на 4,5 кг и более), а через 8 лет – на 5,5 кг [6]. По мнению большинства ученых, увеличение массы тела – последствие менопаузы без учета влияния возрастных изменений.
Причины увеличения массы тела после менопаузы точно не установлены, хотя рассматривается несколько возможных патогенетических механизмов. Показано, что на фоне снижения секреции гормонов яичников увеличивается общее количество жира и происходит его перераспределение в область передней брюшной стенки, а масса мышечной и костной ткани уменьшается. В нескольких исследованиях показано, что изменения составляющих массы тела после менопаузы – снижение плотности костной ткани, уменьшение мышечной массы и увеличение жировой – происходят независимо от изменений общей массы тела. С помощью денситометрии продемонстрировано, что у пациенток в пери– и постменопаузе общее количество жира (особенно на туловище) на 8–9 % больше, а жировая и мышечная масса на бедрах меньше, чем у женщин в пременопаузе [7]. У женщин репродуктивного возраста, которых лечили агонистами гонадотропин релизинг–гормона, отмечены такие же изменения, как и после естественной менопаузы: повышение количества жира на фоне снижения костной и мышечной массы [8]. Увеличение массы тела и формирование абдоминального ожирения на фоне дефицита половых гормонов объясняют изменениями баланса энергии и регуляции жировых клеток, усиленной глюкокортикоидной стимуляцией, относительной гиперандрогенией и другими механизмами.
Прибавка массы тела – это в первую очередь результат нарушения баланса между поступающей с пищей энергией и ежедневным ее расходом на базальный метаболизм, термогенез и физическую активность (см. рисунок). Установлено, что на базальный метаболизм затрачивается 65–70 % ежедневного расхода энергии [9]. Существует строгая взаимосвязь между суммарным ежедневным расходом энергии, долей базального метаболизма и массой мышечной ткани, где в основном он и осуществляется. Установлено, что скорость расхода энергии наследуется, поэтому врожденная низкая интенсивность метаболизма может предопределять возможность развития ожирения.
Термогенез, или термический эффект пищи, – вторая составляющая (около 10 %) суточного расхода энергии. В термогенезе выделяют облигатную функцию, которую невозможно подавить лекарственными препаратами, и факультативную функцию, блокируемую бета–адренергическими веществами. Последнее доказывает важную роль симпатической нервной системы в регуляции баланса энергии.
На физическую активность тратится в среднем около 25 % ежедневного расхода энергии, и эта доля наиболее изменчива: от 10 % у слабых и пожилых до 40–50 % у хорошо тренированных активных женщин. Именно поэтому от физической активности в значительной степени зависит регуляция массы тела у женщин в постменопаузе [10].
Поскольку боўльшая часть ежедневного расхода энергии приходится на базальный метаболизм, даже небольшие его изменения существенно влияют на массу тела. Так, у женщин репродуктивного возраста в лютеиновой фазе менструального цикла на фоне высоких концентраций прогестерона и относительно низких эстрадиола увеличиваются расход энергии, масса тела, общее количество употребляемой пищи и содержание жиров в ней [11].
После менопаузы скорость метаболизма “в покое” замедляется, что подтверждается результатами исследования, в котором при динамическом наблюдении у здоровых женщин в возрасте до 48 лет зарегистрирована постоянная скорость базального метаболизма, а в более старшей возрастной группе отмечено значительное ослабление обменных процессов (на 4–5 % в каждое десятилетие жизни). Установлено, что такая степень снижения скорости базального метаболизма после менопаузы эквивалентна увеличению массы тела на 3–4 кг [12].
При длительном наблюдении за женщинами различного возраста установлено, что в постменопаузе скорость метаболизма в покое снижается примерно на 420 кДж/сут, тогда как в репродуктивном возрасте этот эффект не наблюдается. Из–за метаболических последствий длительного периода нарушенной регуляции баланса энергии не только растет масса жировой ткани, но и сокращается количество мышечной. В частности, с помощью рентгеновской денситометрии установлено, что масса мышечной ткани после менопаузы уменьшается примерно на 3 кг [12].
Механизмы влияния половых гормонов на жировую ткань до сих пор окончательно не установлены. Полагают, что уровень половых стероидов в крови определяет характер распределения жировой ткани, поскольку в ней происходят накопление, интенсивная ароматизация половых гормонов и их секреция. За последние десятилетия установлено, что стероидные гормоны реализуют свое действие через регуляцию экспрессии генов, связываясь в клетках тканей–мишеней со специфическими рецепторами. В настоящее время известны два вида рецепторов к эстрогенам: альфа и b. В жировой ткани экспрессируются бета–рецепторы [13].
Один из основных механизмов влияния половых гормонов на жировую ткань состоит в прямом воздействии на активность липопротеинлипазы – главного фермента регуляции накопления триглицеридов в адипоцитах. У женщин репродуктивного возраста липопротеинлипаза стимулирует эстрогены в жировой ткани бедер и ягодиц, где активность данного фермента выше, чем в подкожном жире абдоминальной области. В результате происходит накопление липидов для обеспечения адекватных запасов энергии в период беременности и лактации. После менопаузы активность липопротеинлипазы снижается, и адипоциты бедренно–ягодичной области уменьшаются в размерах, т. е. происходит относительное перераспределение жира [14].
Прогестерон также участвует в регуляции жировой ткани. Он конкурирует с глюкокортикоидами за их рецепторы в адипоцитах, предотвращая таким образом воздействие глюкокортикоидов на жировую ткань в поздней лютеиновой фазе цикла. Отсутствием такого эффекта прогестерона отчасти объясняется замедление метаболизма после менопаузы. На фоне дефицита половых гормонов липопротеинлипаза не стимулируется и адипоциты жировой ткани бедренно–ягодичной области уже не служат источником запасов энергии в организме [14].
Воздействие половых гормонов на жировую ткань проявляется особенностями распределения жира в различные периоды жизни женщины. Как уже отмечалось выше, для репродуктивного возраста характерны более высокая активность липопротеинлипазы в области бедер и ягодиц, низкая активность липолиза и гиноидное распределение жира. В постменопаузе в этой области активность липопротеинлипазы низкая или отсутствует, а в подкожной абдоминальной и особенно в висцеральной жировой ткани происходит интенсивный липолиз. На фоне заместительной гормональной терапии (ЗГТ) стимулируется активность липопротеинлипазы в адипоцитах бедер и ягодиц, а в абдоминальной жировой ткани активность фермента находится на низком уровне [15].
В клинических исследованиях показано, что у женщин с регулярным менструальным циклом аппетит зависит от уровня эстрадиола в крови. В частности, в периовуляторном периоде общее количество потребляемой пищи резко уменьшается, а в лютеиновой фазе аппетит повышается. Наличие взаимосвязи между уровнями эстрадиола и характером питания у женщин доказывает снижение аппетита через один–два дня после повышения секреции эстрадиола [16].
Специфической области головного мозга, где эстрадиол действует как агент, подавляющий аппетит, не обнаружено. Предполагают, что это осуществляется по механизму обратной связи (как и при взаимодействии с лютеинизирующим гормоном) с одновременным воздействием на несколько областей головного мозга. На основании факта подавления аппетита у животных после имплантации эстрадиола в гипоталамус предложена гипотеза, согласно которой эстрадиол действует на вентромедиальную область гипоталамуса, подавляя тем самым аппетит [16].
Эстрогены могут влиять на жировую ткань, взаимодействуя с лептином – белковым гормоном, секретируемым жировыми клетками. Основная функция лептина – сигнализировать в мозг о достаточности запасов энергии в организме (пороге насыщения). Лептин взаимодействует со специфическими рецепторами, которые имеются в различных органах, и влияет на экспрессию ключевых гипоталамических пептидов в аркуатном ядре, в частности уменьшает содержание нейропептида Y [16].
Установлена строгая взаимосвязь между содержанием лептина в сыворотке крови и количеством жира в организме. При сбалансированности энергии уровень лептина отражает количество триглицеридов в жировой ткани. При несбалансированных поступлении и расходе энергии (голоде, переедании) лептин может выполнять функцию своеобразного индикатора баланса энергии. Установлено, что при потере 10 % массы тела уровень лептина снижается на 53 %, а увеличение массы тела на 10 % приводит к возрастанию содержания лептина на 300 % [16].
Эстрогены регулируют продукцию лептина по механизму положительной обратной связи. Результаты экспериментов на грызунах и исследований тканей человека показали, что в яичниках экспрессируются рецепторы к лептину, а эстрадиол регулирует продукцию лептина адипоцитами. Концентрации лептина увеличиваются в лютеиновой фазе менструального цикла. В нескольких исследованиях у женщин репродуктивного возраста зарегистрированы более высокие концентрации лептина по сравнению с его уровнями у пациенток в постменопаузе [17].
Общеизвестно, что при депрессии, дисфории и хроническом стрессе постоянная стимуляция гипоталамуса приводит к повышению активности системы: кортикотропный релизинг–гормон – адренокортикотропный гормон – надпочечники. Предполагают, что в постменопаузе также усиливается глюкокортикоидная стимуляция, что ведет к увеличению размеров адипоцитов и формированию абдоминального ожирения.
Уровни тестостерона в крови напрямую связаны с количеством абдоминального жира. В постменопаузе снижается содержание глобулина, связывающего половые стероиды, что приводит к повышению концентрации свободного тестостерона, гиперандрогении и вносит дополнительный вклад в формирование абдоминального ожирения.
Влияние заместительной гормональной терапии на массу тела
Сведения о воздействии ЗГТ на массу тела у женщин в постменопаузе противоречивы, а проспективные исследования немногочисленны. Например, Gambacciani M. и соавт. [17] отметили увеличение массы тела на 1,9 кг за год у 12 женщин в группе контроля (без ЗГТ) и стабильную массу тела в группе получавших ЗГТ. В нескольких исследованиях у пациенток, принимавших ЗГТ, отмечено меньшее значение отношения ОТ/ОБ. В Исследовании медицинских сестер, в котором ИМТ учитывали сами участницы, установлено уменьшение этого показателя при использовании эстрогенов. В нескольких работах показано, что монотерапия эстрогенами предотвращает прибавку массы жировой ткани в организме [18].
Таким образом, согласно опубликованным данным, в регуляции массы тела у женщин немаловажную роль играют половые гормоны: они действуют на аппетит, суточный баланс энергии и метаболические процессы в жировой ткани. Большинство ученых считают, что на фоне дефицита половых гормонов независимо от возраста происходит прибавка массы тела за счет увеличения количества жира (с формированием абдоминального ожирения), уменьшения мышечной и костной массы. Результаты нескольких исследований показали, что монотерапия эстрогенами и комбинированная ЗГТ восстанавливают гиноидный, характерный для репродуктивного возраста тип распределения жировой ткани и способствуют снижению массы тела.
С 1997 г. мы обследовали женщин, обратившихся в специализированный центр “Здоровье женщины после 40 лет”. Поскольку, на массу тела у женщин влияет множество факторов, мы тщательно соблюдали одно из условий включения в исследование: отсутствие значительных колебаний массы тела до наступления менопаузы. Таким образом, в наше первое исследование по массе тела в климактерии были включены 55 женщин с прибавкой веса 5 кг и более, совпавшей с менопаузой. Как оказалось, у многих женщин вес начинает расти в период перименопаузы. При первичном обследовании пациенток мы установили, что после менопаузы масса тела в среднем увеличилась на 9,7 кг (5–24 кг) и достоверно коррелировала с продолжительностью постменопаузального периода. Кроме того, оказалось, что у женщин с продолжительностью постменопаузы более пяти лет прибавка в весе была достоверно больше, чем в перименопаузе. Наконец, мы установили, что в постменопаузе масса тела и показатели, характеризующие ожирение и его вид (ИМТ и ОТ), достоверно выше, чем в перименопаузе.
После исходного обследования 45 женщинам назначили ЗГТ. По нашим данным, у подавляющего большинства из них (96,1 %) в течение года наблюдалось прогрессивное снижение массы тела в среднем на 4,5 кг. Степень абдоминального ожирения уменьшилась у 98 % женщин. Более выраженный и быстрый эффект отмечался у пациенток в перименопаузе: масса тела и ОТ достоверно снизились уже к шестому месяцу терапии. Снижение ИМТ практически до верхней границы нормы (25,3 кг/м 2 ) зарегистрировано только в группе женщин в перименопаузе.
Мы также обследовали 46 женщин в постменопаузе (средний возраст – 51,2 года, продолжительность постменопаузы – 3,8 года). К моменту проведения обследования 23 пациентки в течение двух лет принимали циклический комбинированный препарат Фемостон 2/10 (эстрадиол 2 мг ± дидрогестерон 10 мг), остальные 23 женщины никогда ранее не принимали ЗГТ. Всем участницам исследования проведено антропометрическое обследование: измерение роста, массы тела, ОТ и ОБ, вычисление ИМТ и соотношения ОТ/ОБ.