полуконсервативная репликация
Смотреть что такое «полуконсервативная репликация» в других словарях:
полуконсервативная репликация — Метод репликации молекулы ДНК, при которой каждая материнская цепь молекулы ДНК достраивает себе новую дочернюю цепь [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN semiconservative replication … Справочник технического переводчика
Полуконсервативная репликация — * паўкансерватыўная рэплікацыя * semiconservative replication тип репликации ДНК, при котором молекула делится продольно, каждая половина сохраняется и служит матрицей для образующейся новой нити. Термин был введен, когда точный процесс… … Генетика. Энциклопедический словарь
Репликация полуконсервативная — * рэплікацыя паўкансерватыўная * semi conservative replication процесс репликации, при котором дочерние клетки первого поколения получают одну цепь ДНК от родителей, а вторая цепь синтезируется вновь. Такой же процесс повторяется при образовании… … Генетика. Энциклопедический словарь
репликация θ-типа — репликация θ типа θ репликация Двунаправленная полуконсервативная репликация кольцевых молекул ДНК, начинающаяся с образования «вздутия», видимого под электронным микроскопом, расширяющегося в двух направлениях; перед… … Справочник технического переводчика
Семиконсервативная репликация — * семікансерватыўная рэплікацыя * semiconservative replication … Генетика. Энциклопедический словарь
генетический код — Долгое время наследственные механизмы были предметом внимания генетиков, но природа молекул, переносящих информацию от одного индивида к другому, оставалась неведомой. Была известна роль макромолекул протеина и нуклеиновых кислот в этом… … Западная философия от истоков до наших дней
История науки — История науки это исследование феномена науки в его истории. Наука, в частности, представляет собой совокупность эмпирических, теоретических и практических знаний о Мире, полученных научным сообществом. Поскольку с одной стороны наука… … Википедия
semiconservative replication — semiconservative replication. См. полуконсервативная репликация. (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
Полуконсервативный способ репликации



РЕПЛИКАЦИЯ ДНК
Репликация ДНК – синтез ДНК – происходит по полуконсервативному механизму. Согласно гипотезе Уотсона-Крика, каждая из цепей двойной спирали ДНК служит матрицей для репликации комплементарных дочерних цепей. При этом образуются две дочерние двухцепочечные молекулы ДНК, идентичные родительской ДНК. Каждая из этих молекул содержит одну неизмененную цепь родительской ДНК и одну вновь синтезированную цепь дочерней ДНК.
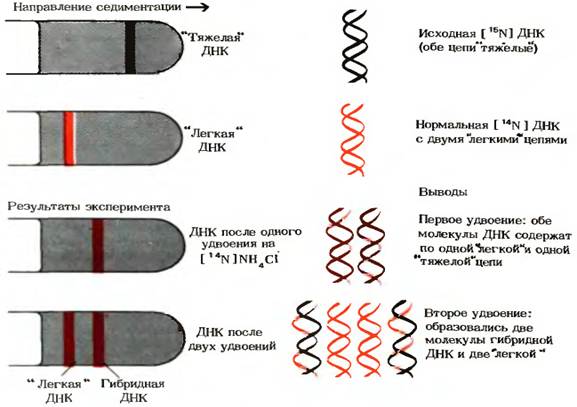
Гипотеза Уотсона-Крика была проверена с помощью опытов, выполненных М.Мезельсоном и Ф.Сталем в 1957 г. Клетки E.coli выращивали в течение ряда поколений в среде, содержащей в качестве источника азота хлористый аммоний NH4Cl, в котором обычный изотоп [ 14 N] был заменен на «тяжелый» изотоп [ 15 N]. Вследствие этого все соединения клеток, имеющие в своем составе азот, в том числе и азотистые основания ДНК, оказались обогащенными изотопом [ 15 N]. Плотность ДНК, выделенной из этих клеток, была выше плотности нормальной [ 14 N] ДНК. Смесь «тяжелой» [ 15 N] и «легкой» [ 14 N] ДНК удалось разделить методом центрифугирования в концентрированном растворе хлористого цезия. Поскольку [ 15 N] ДНК чуть тяжелее, чем [ 14 N] ДНК, полоса, в которой она достигает равновесия в градиенте СsCl, расположена ближе ко дну пробирки, чем полоса с [ 14 N] ДНК (рис.7)
Рис. 7 Результаты эксперимента Мезельсона-Сталя
Мезельсон и Сталь перенесли клетки E.coli, росшие на среде с изотопом [ 15 N] и содержащие «тяжелые» цепи ДНК, на свежую среду с обычным изотопом [ 14 N]. На этой среде клетки E.coli выращивали в течение времени, необходимого для удвоения клеток. Затем из этих клеток выделяли ДНК и анализировали ее плотность с помощью описанного выше метода седиментации (осаждения ДНК в растворе СsCl). В градиенте СsCl была обнаружена лишь одна полоса ДНК, плотность которой оказалась средней между плотностью нормальной «легкой» [ 14 N] ДНК и плотностью «тяжелой» [ 15 N] ДНК (рис. ). Это подтвердило, что двухцепочечная ДНК дочерних клеток содержит одну старую 15 N – цепь от родительской ДНК и одну новую 14 N – цепь.
Если выделить ДНК из клеток, которые прошли два цикла удвоения на среде с [ 14 N], то она разделится на две полосы: одна с плотностью, соответствующей плотности нормальной «легкой» ДНК, а другая с плотностью «гибридной» ДНК, наблюдавшейся после первого удвоения клеток. На основании этих данных Мезельсон и Сталь пришли к выводу, что в строгом соответствии с гипотезой Уотсона-Крика каждый дочерний дуплекс ДНК после двух циклов удвоения клеток содержал одну родительскую и одну новообразованную цепь ДНК. Такой механизм репликации назвали полуконсервативным. Полученные результаты полностью исключили консервативный способ репликации, при котором одна дочерняя ДНК должна была бы содержать обе исходные цепи, а другая состояла бы из двух новосинтезированных цепей. Опыт Мезельсон и Сталя позволил также отвергнуть дисперсивный механизм репликации, при котором каждая дочерняя цепь ДНК состоит из коротких участков как родительской, так и новообразованнй ДНК, соединенных между собой случайным образом.
Полуконсервативный способ репликации ДНК. Биологическое значение.
Полуконсервативный механизм репликации ДНК. Перед каждым делением клетки в ней должно удвоиться содержание ДНК, чтобы каждая дочерняя клетка получила полный набор хромосом. Основу каждой хромосомы образует одна двухцепочечная молекула ДНК. Предложенная Дж. Уотсоном и Ф. Криком модель строения ДНК форме регулярной двойной спирали сразу же позволила понять принцип копирования ДНК. Ее репликация происходит полуконсервативным способом: две исходные цепи материнской ДНК расходятся, и каждая из них становится матрицей для синтеза новой комплементарной цепи. Таким образом, каждая новая двойная спираль ДНК содержит одну старую и одну новую цепь. Такой механизм репликации ДНК, при котором от одного поколения к другому передается одна из двух материнский цепей ДНК, получил название полуконсервативного и был экспериментально доказан в 1958 году М. Мезельсон и Ф. Сталь.
Легко представить, что удвоение ДНК происходит вследствие того, что цепи расходятся и каждая цепь служит матрицей для синтеза новой комплементарной цепи ДНК. Каждая дочерняя молекула состоит из одной старой материнской и одной новой синтезированной цепи ДНК.
Общие принципы репликации ДНК.
В основе процесса репликации лежит принцип копирования материнской цепи ДНК с образованием двух идентичных молекул ДНК. В основе синтеза новой цепи ДНК лежит принцип комплементарности азотистых оснований, т.е. последовательность нуклеотидов материнской цепи определяет последовательность нуклеотидов в синтезируемой цепи ДНК
Синтез новых цепей ДНК идет в направлении 5’ → 3’.
Кольцевая хромосома прокариот имеет одну точку начала репликации, которая
называется OriC. В этой точке цепи расходятся и образуются две репликативные вилки, которые движутся в противоположном направлении. Скорость синтеза ДНК в клетках прокариот составляет 500 нукл./сек. Две вилки встречаются на противоположной стороне кольца. В клетках прокариот существует специальный фермент гираза (топоизомераза II), который разделяет две образующиеся кольцевые молекулы ДНК. Антибиотик налидиксовая кислота угнетает размножение бактерий, путем инактивации гиразы.
В клетках эукариот этот фермент отсутствует, поэтому налидиксовую кислоту используют в клинической практике для лечения бактериальных инфекций.
ЧАСТЬ III. ПУТИ ПЕРЕДАЧИ ИНФОРМАЦИИ
Скучных ферментов не бывает.
— Артур Корнберг, «С любовью к ферментам», 1975
25. МЕТАБОЛИЗМ ДНК
В качестве хранилища генетической информации ДНК занимает центральное место среди биологических макромолекул. Нуклеотидная последовательность ДНК кодирует первичную структуру всех молекул клеточной РНК и белков и через ферменты опосредованно влияет на синтез всех других клеточных компонентов. Переход информации от ДНК к РНК и белку определяет размер, форму и жизнедеятельность всех живых существ.
ДНК прекрасно обеспечивает стабильное хранение генетической информации. Однако понятие «стабильное хранение» означает статичную неизменную картину. Оно не отражает сложности процессов, с помощью которых генетическая информация сохраняется и передается от одного поколения клеток к следующему. Метаболизм ДНК включает как процессы точного копирования молекул (репликация), так и процессы, которые влияют на саму структуру, несущую информацию (репарация и рекомбинация). Именно эти процессы мы и рассмотрим в данной главе.
Метаболизм ДНК должен происходить идеально точно. Химические реакции присоединения одного нуклеотида к другому при репликации ДНК элегантны и на удивление просты. Сложности, как мы увидим далее, в ферментативном аппарате, обеспечивающем точность передачи генетической информации. Ошибки, возникающие при синтезе ДНК, могут привести к серьезным последствиям, причем не только потому, что они изменяют или нарушают функцию определенного гена, но и потому, что такое изменение передается по наследству.
Ферменты, участвующие в синтезе ДНК. копируют молекулы ДНК, содержащие миллионы оснований. Они проделывают это с необыкновенной точностью и скоростью, несмотря на то что ДНК очень компактно упакована и связана с другими белками. Образование фосфодиэфирных связей между нуклеотидами в растущей цепи ДНК — только часть сложного процесса, в котором задействовано множество белков и ферментов.
Задача сохранения генетической информации лежит в основе процесса репарации ДНК. В гл. 8 (т. 1) подробно описана чувствительность ДНК ко многим разрушительным воздействиям. Такие воздействия происходят нечасто, но они играют очень важную роль, поскольку устойчивость организмов к изменениям последовательности ДНК очень низкая. ДНК — единственная макромолекула, для которой предусмотрена система репарации; количество, разнообразие и сложность механизмов репарации отражает многообразие пагубных для ДНК воздействий.
Клетки могут перестраивать хранящуюся в них генетическую информацию в процессах под общим названием «рекомбинация». Казалось бы, процесс рекомбинации подрывает принцип первостепенного значения стабильности и целостности генетической информации. Однако на самом деле большинство перестроек ДНК играет конструктивную роль в поддержании целостности генома, специфическим образом влияя на репликацию и репарацию ДНК и расхождение хромосом.
В этой главе особое внимание уделяется ферментам метаболизма ДНК. Они заслуживают внимательного изучения не только ввиду их большого биологического значения и чисто научного интереса, но и в связи с их возрастающей ролью в качестве лекарственных препаратов в медицине и в качестве инструментов в широком круге современных биохимических технологий. Многие ценные открытия в области метаболизма ДНК были сделаны на клетках Escherichia coli, поэтому для объяснения основ метаболизма обычно в качестве примера служат хорошо известные ферменты этой бактерии. Беглый взгляд на некоторые важные гены на генетической карте Е. coli (рис. 25-1) позволяет представить себе сложность ферментных систем, участвующих в метаболизме ДНК.
Рис. 25-1. Хромосомная карта Escherichia coli. Показано расположение генов, кодирующих многие важные для метаболизма ДНК белки. Количество известных генов, участвующих в метаболизме ДНК, свидетельствует о сложности этих процессов. Числа от 0 до 100 внутри кольцевой хромосомы соответствуют генетическим единицам измерения, называемым минутами. Каждая минута соответствует отрезку молекулы ДНК длиной примерно 40 000 п. н. Трехбуквеные названия генов обычно отражают некоторые аспекты их функции, к примеру, mut — мутагенез; dna — репликация ДНК; pol — ДНК-полимераза; rро — РНК-полимераза; uvr — устойчивость к УФ; rес — рекомбинация; dam — метилирование аденина; lig — ДНК-лигаза; Теr — терминация репликации; ori — точка начала репликации (у Е. coli это oriC, как на рисунке).
Прежде чем перейти к детальному изучению процесса репликации, сделаем короткое отступление и поговорим о принятых сокращениях названий бактериальных генов и белков, поскольку со многими из них нам предстоит встретиться в этой и последующих главах. Аналогичные договоренности используются и в обозначениях эукариотических генов, хотя конкретное сокращение может зависеть от вида организма, и единого правила для всех эукариотических систем не существует.
Бактериальные гены обычно обозначают тремя строчными буквами курсивом, и, как правило, название отражает функцию этих генов. Например, dna, uvr и rес гены означают репликацию ДНК, устойчивость к поражающему действию УФ-облучения и рекомбинацию соответственно. Если несколько генов отвечают за одну и ту же функцию, они дополнительно обозначаются буквами А, В, С и т. д., например, dnaA, dnaB, dnaQ, что обычно указывает на порядок их открытия, а не порядок участия в цепи реакций. ■
Использование сокращений в названиях белков менее очевидно. В ходе генетических исследований обычно выделяют и характеризуют белковые продукты каждого гена. Многие бактериальные гены были идентифицированы и названы до того, как выяснилось значение их белковых продуктов. Иногда оказывается, что продукт гена — это уже известный белок, и его приходится переименовывать. Однако часто бывает, что продукт гена еще неизвестен и обладает активностью, которую нельзя описать обычным названием фермента.
Бактериальные белки часто сохраняют названия соответствующих генов. Названия белков Е. coli пишутся прямым шрифтом с заглавной буквы, например, белковые продукты генов dnaA и rесА называются DnaA и RecA соответственно. ■
25.1. Репликация ДНК
Задолго до установления структуры ДНК ученых удивляла способность организмов воссоздавать самих себя и способность клеток образовывать много идентичных копий крупных и сложных макромолекул. Рассуждения на эту тему концентрировались вокруг концепции матрицы — структуры, которая позволяет молекулам соединяться в определенном порядке и образовывать макромолекулу с уникальной последовательностью и функцией. В 1940-е гг. уже сложилось представление о том, что носителем генетической информации является ДНК, но только когда Джеймс Уотсон и Фрэнсис Крик установили ее структуру, стало понятно, каким образом ДНК играет роль матрицы для репликации и передает генетическую информацию: дело в том, что одна ее цепь комплементарна другой. Основания образуют пары по определенным правилам, и каждая цепь является матрицей для новой цепи с предсказуемой комплементарной последовательностью (см. рис. 8-14, 8-15 в т. 1).
Было доказано, что основные свойства процесса репликации ДНК и каталитические механизмы этого процесса в значительной степени идентичны у всех видов организмов. Именно это единство механизмов мы постараемся подчеркнуть в нашем обсуждении, продвигаясь от общих основ процесса репликации к ферментам репликации Е. coli и, наконец, к репликации эукариот.
Основные принципы репликации ДНК
В ранних исследованиях репликации бактериальной ДНК и ее ферментов было установлено несколько базовых принципов, на которых основан синтез ДНК у всех живых существ.
Репликация ДНК полуконсервативна.
Каждая цепь ДНК служит матрицей для синтеза новой цепи, при этом образуются две новые двухцепочечные молекулы ДНК, каждая из которых состоит из одной новой и одной старой цепей. Поэтому процесс называется полуконсервативной репликацией.
Уотсон и Крик выдвинули гипотезу полуконсервативной репликации вскоре после публикации своей статьи о структуре ДНК с 1953 г.; в 1957 г. эта гипотеза была подтверждена Мэтью Мезельсоном и Франклином Сталем, которые искусно провели следующие эксперименты. Мезельсон и Сталь культивировали клетки Е. coli на протяжении многих генераций в среде, в которой единственный источник азота (NH4Cl) содержал тяжелый изотоп азота 15 N вместо наиболее распространенного легкого изотопа 14 N. Плотность выделенной из этих клеток ДНК примерно на 1% больше, чем у обычной [ 14 N] ДНК (рис. 25-2, а). Несмотря на столь небольшое различие, смесь тяжелой [ 15 N] ДНК и легкой [ 14 N] ДНК можно разделить центрифугированием в градиенте плотности хлорида цезия.
Рис. 25-2, а — несколько поколений клеток выращивали в среде, содержащей только тяжелый азот 15 N, поэтому в ДНК этих клеток содержался исключительно азот 15 N, что показано в виде одной (синей) полосы, образующейся при центрифугировании в градиенте плотности CsCl. б — клетки переносили на среду, содержащую только легкий азот 14 N, и после первого деления клеток выделяли ДНК, которая в градиенте хлорида цезия образовывала более высокую (фиолетовую) полосу, в — после второго цикла репликации ДНК разделялась на две полосы: гибридную (фиолетовую) и еще более легкую (красную), содержащую только ДНК с 14 N, что подтверждало полу- консервативный характер репликации.
Клетки Е. coli, выращенные на среде с 15 N, переносили на свежую питательную среду, содержащую только изотоп 14 N, где клетки продолжали расти до тех пор, пока численность популяции не удваивалась. ДНК, выделенную из этой первой генерации клеток, центрифугировали в градиенте CsCl и наблюдали единственную полосу, положение которой свидетельствовало о том, что двухспиральная ДНК дочерних клеток представляет собой гибрид, содержащий одну новую цепь с 14 N и одну родительскую цепь с 15 N (рис. 25-2, б).
Репликация начинается в точке начала репликации и обычно идет в двух направлениях.
После доказательства полуконсервативного механизма репликации возникло множество вопросов. Полностью ли раскручивается родительская ДНК до начала репликации каждой цепи? Начинается ли репликация в случайной или в какой-то особой точке? После инициации в какой-то точке репликация происходит в одном направлении или в двух?
В ранних исследованиях Джона Кэрнса, проведенным с помощью метода авторадиографии, удалось доказать, что репликация — высококоординированный процесс, в котором родительские цепи одновременно расплетаются и реплицируются. Кэрнс получил радиоактивную ДНК Е. coli, для чего культивировал эту бактерию на среде с меченным тритием ( 3 Н) тимидином. ДНК была аккуратно выделена, покрыта слоем фотографической эмульсии и оставлена так на несколько недель; за это время радиоактивный тимидин оставил в фотоэмульсии «следы» — зерна серебра, создав фотоотпечаток молекулы ДНК. По этим отпечаткам видно, что интактная хромосома Е. coli представляет собой единую гигантскую кольцевую структуру длиной 1,7 мм. В радиоактивной ДНК, выделенной из клеток во время репликации, кроме того, была обнаружена дополнительная петля (рис. 25-3, а). Кэрнс сделал вывод, что, петля образуется в результате формирования двух радиоактивных дочерних цепей, каждая из которых комплементарна родительской пени. На одном или на обоих концах петли движется репликативная вилка, в которой родительская ДНК раскручивается, позволяя реплицироваться разделившимся цепям. Согласно полученным Кэрнсом данным, обе цепи ДНК реплицируются одновременно, а различные варианты его эксперимента (рис. 25-3, б) показали, что репликация бактериальных хромосом двунаправленная: на обоих концах петли расположены активные репликативные вилки.
Рис. 25-3. Выявление двунаправленного характера репликации ДНК. а — во время репликации кольцевой хромосомы образуется структура, напоминающая греческую букву тета (θ), так как обе нити реплицируются одновременно (новая нить показана красным цветом). б — репликация может происходить в одном или в обоих направлениях, что можно установить с помощью авторадиографии: при внесении 3 Н на короткий период непосредственно перед прекращением реакции метка (отмечена красным) обнаруживается в одной или в двух репликативных вилках соответственно. Так была продемонстрирована двунаправленность репликации у Е. coli, Bacillus subtilis и других бактерий. На авторадиограмме показан репликационный «глазок» в ДНК В. subtilis. Самая большая плотность зерен серебра (стрелки) наблюдается именно в тех двух местах, где происходит репликация. Не подвергшаяся репликации часть хромосомы, находящаяся вне глазка, не содержит метки и поэтому невидима.
Чтобы выяснить, образуются ли репликативные вилки в каком-то определенном участке ДНК, необходимо было установить по всей длине молекулы некие реперные точки. Это было сделано с помощью метода денатурирующего картирования, разработанного Россом Инманом с коллегами. С помощью хромосомы бактериофага λ длиной 48 502 п. и. было показано, что можно вызвать избирательную денатурирацию ДНК в последовательностях с необычно высоким содержанием пар А = Т, получая воспроизводимую картину одноцепочечных глазков (см. рис. 8-28 в т. 1). Таким же образом можно частично денатурировать выделенную ДНК, содержащую репликативные петли. Это позволяет измерить и картировать положение и движение репликативных вилок, используя денатурированные области в качестве реперных точек. С помощью данного метода было показано, что в этой системе репликативные петли всегда возникают в особых точках, которые были названы точками начала репликации (ориджинами). Получил подтверждение и выявленный ранее двунаправленный характер репликации. У кольцевых молекул ДНК две репликативные вилки встречаются в точке, расположенной напротив точки начала репликации. Специфические точки начала репликации с тех пор были идентифицированы и охарактеризованы у бактерий и низших эукариот.
Синтез ДНК наполовину прерывистый и проходит в направлении 5’—> 3′.
Новая цепь ДНК всегда синтезируется в направлении 5′ —> 3′, т. е. приращение ДНК происходит со стороны свободной ОН-группы на 3′-конце (строение 5′- и 3′-концов цепи ДНК см. на рис. 8-7 в т. 1). Поскольку две цепи ДНК антипараллельны, цепь, служащая в качестве матрицы, считывается с 3’-конца в направлении к 5′-концу.
Но если синтез ДНК всегда происходит в направлении 5′ —> 3′, как могут обе цепи синтезироваться одновременно? Если обе цепи синтезируются непрерывно, пока движется репликативная вилка, одна цепь должна синтезироваться в направлении 3′ —> 5′. Эту проблему в 1960-х гг. разрешил Рейджи Оказаки с коллегами. Они обнаружили, что одна из новых цепей ДНК синтезируется в виде коротких отрезков, которые теперь называются фрагментами Оказаки. В результате их исследований стало ясно, что одна цепь синтезируется непрерывно, а вторая — прерывисто (рис. 25-4). Направление синтеза непрерывной, или лидирующей, цепи совпадает с направлением движения репликативной вилки. Направление синтеза прерывистой, или отстающей, цепи противоположно направлению движения вилки. Фрагменты Оказаки различаются по длине от нескольких сотен до нескольких тысяч нуклеотидов в зависимости от типа клеток. Ниже мы увидим, что синтез лидирующей и отстающей цепей четко координируется.
Рис. 25-4. Различия цепей ДНК на репликативной вилке. Новая цепь ДНК (красная) всегда синтезируется в направлении 5′ —> 3′. Матрица считывается в противоположном направлении. 3′ —> 5′. Лидирующая цепь непрерывно синтезируется по направлению движения репликативной вилки. Другая цепь, отстающая, синтезируется прерывисто в виде коротких отрезков (фрагментов Оказаки) в направлении, противоположном тому, в котором движется репликативная вилка. Фрагменты Оказаки сшиваются ДНК-лигазой. У бактерий длина фрагментов Оказаки составляет примерно от 1000 до 2000 нуклеотидов. В клетках эукариот они короче: от 150 до 200 нуклеотидов.
ДНК разрушается нуклеазами
Чтобы объяснить энзимологию процесса репликации ДНК, сначала рассмотрим ферменты, которые разрушают, а не синтезируют ДНК. Эти ферменты называют нуклеазами или ДНКазами, если они обладают большей специфичностью к ДНК, чем к РНК. Каждая клетка содержит несколько разных нуклеаз, принадлежащих к двум большим классам: экзонуклеазы и эндонуклеазы. Экзонуклеазы расщепляют нуклеиновые кислоты с одного конца молекулы. Многие из них работают только в направлении 5′ —> 3′ или только в направлении 3′ —> 5′, удаляя нуклеотиды либо с 5′-конца, либо с 3′-конца одной цепи двухцепочечной молекулы нуклеиновой кислоты или одноцепочечной ДНК. Эндонуклеазы начинают расщепление нуклеиновой кислоты со специфических внутренних сайтов, расщепляя цепь на более мелкие фрагменты. Некоторые экзонуклеазы и эндонуклеазы расщепляют только одноцепочечные ДНК. Существует несколько важных классов эндонуклеаз, которые разрушают только определенные нуклеотидные последовательности (например, эндонуклеазы рестрикции, которые имеют очень большое значение в биотехнологии; см. гл. 9, рис. 9-2 вт. 1). В этой и в последующих главах мы встретим много типов нуклеаз.
ДНК синтезируется ДНК-полимеразами
Поиск фермента, который может синтезировать ДНК, начался в 1955 г. Артуру Корнбергу с коллегами удалось очистить и охарактеризовать ДНК-полимеразу из клеток Е. coli. Этот фермент, состоящий из одного полипептида, теперь называют ДНК-полимеразой I (Мr = 103 000; кодируется геном роlА). Гораздо позже исследователи обнаружили, что Е. coli содержит еще как минимум четыре другие ДНК-полимеразы, описанные ниже.
При детальном изучении ДНК-полимеразы 1 были установлены общие для всех ДНК-полимераз характеристики процесса синтеза ДНК. В основной реакции происходит перенос фосфорильных групп. При этом 3′-гидроксильная группа нуклеотида на 3′-конце растущей цепи выступает в роли нуклеофила, атакующего α-фосфор присоединяющегося дезоксинуклеозид-5′-трифосфата (рис. 25-5). В результате высвобождается неорганический пирофосфат. Основная реакция выглядит следующим образом:
Еще в ранних исследованиях ДНК-полимеразы I удалось определить два основных условия, необходимых для полимеризации ДНК. Во-первых, все ДНК-полимеразы нуждаются в матрице. Реакция полимеризации происходит на матрице ДНК согласно правилам комплементарности оснований, установленным Уотсоном и Криком: если в матрице присутствует гуанин, к новой цепи присоединяется дезоксинуклеотид цитозина и т. д. Это открытие имеет очень важное значение не только потому, что оно объясняет химическую основу точной полуконсервативной репликации ДНК, но и потому, что это был первый пример использования матрицы для проведения реакции биосинтеза.
Во-вторых, полимеразы нуждаются в праймере. Праймер — это участок цепи (комплементарный матрице) со свободной З’-гидроксильной группой, к которой может присоединиться нуклеотид. Иначе говоря, перед началом синтеза часть новой цепи уже должна существовать: все ДНК-полимеразы могут присоединять нуклеотиды только к уже существующей цепи. Многие праймеры представляют собой олигонуклеотиды РНК, а не ДНК; специальные ферменты синтезируют праймеры там и тогда, где и когда они требуются.
После присоединения нуклеотида к растущей цепи ДНК ДНК-полимераза либо диссоциирует, либо продвигается вдоль матрицы и присоединяет следующий нуклеотид. Диссоциация и обратное присоединение полимеразы может ограничивать среднюю скорость полимеризации — процесс обычно протекает быстрее, если полимераза присоединяет нуклеотиды, не покидая матрицы. Среднее число нуклеотидов, присоединенных до диссоциации полимеразы, определяет ее процессивность. ДНК-полимеразы существенно различаются по процессивности; некоторые присоединяют всего несколько нуклеотидов до диссоциации, другие присоединяют многие тысячи.
Репликация — очень точный процесс
Рис. 25-6. Значение геометрии пар оснований для точности репликации ДНК. а — стандартные пары оснований А = Т и G = C очень схожи по геометрии, и, если активный центр фермента может вместить одну пару (синяя рамка), то обычно он вмещает и другую, б — геометрия аномальных пар отличается, и они не помещаются в активном центре ДНК-полимеразы I.
Рис. 25-7. Пример исправления ошибки благодаря 3′ —> 5′-экзонуклеазной активности ДНК-полимеразы I. При изучении структуры фермента было установлено, что при ориентации фермента по ходу движения ДНК- центр его экзонуклеазной активности локализован впереди центра полимеразной активности. Ошибочное спаривание (здесь ошибка С-А) препятствует транслокации ДНК-полимеразы I в следующее положение. Фермент скользит назад, исправляет ошибку благодаря своей 3′ —> 5′-экзонуклеазной активности, а затем возобновляет полимеразную активность в направлении 5′ —> 3′.
У Е. coli не менее пяти ДНК-полимераз
Более 90% ДНК-полимеразной активности в экстрактах Е. coli связано с функцией ДНК-полимеразы I. Однако вскоре после выделения этого фермента в 1955 г. стали накапливаться сведения о том, что он не может осуществлять репликацию крупной хромосомы Е. coli. Во-первых, скорость, с которой фермент присоединяет нуклеотиды (600 нуклеотидов/мин), не соответствует скорости движения репликативной вилки в бактериальной клетке (скорость движения репликативной вилки, как минимум, в 100 раз выше). Во- вторых, ДНК-полимераза I обладает относительно низкой процессивностью. В-третьих, генетические исследования показали, что в репликации участвуют многие гены и, следовательно, многие белки: очевидно, что ДНК-полимераза I действует не в одиночку. В-четвертых, и это особенно важно, в 1969 г. Джон Кэрнс выделил бактериальный штамм с поврежденным геном ДНК-полимеразы I, с которого синтезировался неактивный фермент. Хотя этот штамм был чрезвычайно чувствителен к повреждениям ДНК, тем не менее он был жизнеспособен!
Поиск других ДНК-полимераз привел к открытию в начале 1970-х гг. ДНК-полимеразы II и ДНК-полимеразы III у Е. coli. ДНК-полимераза II участвует в одном из механизмов репарации ДНК (разд. 25.3). ДНК-полимераза III — главный фермент репликации у Е. coli. Свойства трех ДНК-полимераз Е. coli сравниваются в табл. 25-1. ДНК-полимеразы IV и V, идентифицированные в 1999 г., принимают участие в необычном варианте репарации ДНК (разд. 25.2).
Таблица 25-1. Сопоставление ДНК-полимераз Е. coli