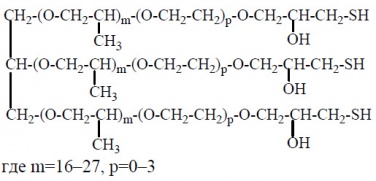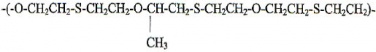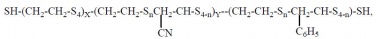Содержание
Структура
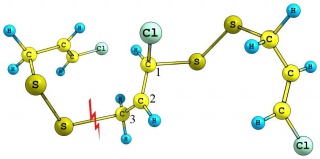
Полисульфидные анионы образуют цепочки с расстоянием между связями S-S около 2 Å. Цепи принимают перекошенные формы. В твердом состоянии эти соли представляют собой плотные твердые вещества с сильной ассоциацией катионов натрия с анионными концами цепей. [2]
Производство и возникновение
Полисульфид натрия можно получить путем растворения серы в растворе сульфид натрия. [3] В качестве альтернативы они производятся окислительно-восстановительной реакцией водного едкий натр с серой при повышенных температурах. [4] Наконец, они возникают при восстановлении элементарной серы натрием, реакция часто проводится в безводном аммиаке.
Эти соли используются в производстве полисульфидные полимеры, как химическое фунгицид, как средство для почернения медь украшения, как компонент в батарея полисульфида бромида, как тонер в фотохимическом растворе, и в дубление промышленность по удалению волос с шкур.
Реакции
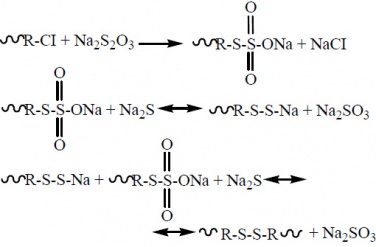
Как эксплуатируется в натриево-серная батарея, полисульфиды абсорбируют и высвобождают восстанавливающие эквиваленты, разрывая и образуя связи S-S соответственно. Показана идеализированная реакция тетрасульфида натрия:
Алкилирование дает органические полисульфиды согласно следующему идеализированному уравнению:
Алкилирование органическим дигалогенидом дает полимеры, называемые тиоколы.
Протонирование этих солей дает сероводород и элементарную серу, что иллюстрируется реакцией пентасульфида натрия:
Способ получения полисульфидов натрия Советский патент 1984 года по МПК C01B17/22
Описание патента на изобретение SU1129186A1
Изобретение относится к неорганическому синтезу сульфидных материалов, предназначенных для использования в качестве катодных материалов во вторичных источниках тока, в частности к способу получения полисульфидов натрия.
Известен способ получения полисульфидов натрия путем сплавления сульфида натрия с серой 1.
Недостатки способа т- низкая скорость взаимодействия компонентов и недостаточно высокая чистота получаемых соединений.
Наиболее близким к изобретению по технической сущности и достигаемому эффекту является способ получения полисульфи.дов натрия, включающий прямое взаимодействие элементарных натрия и серы при повышенных температурах. Согласно известному способу натрий расплавляют в органическом растворителе (бензол, толуол), нагреванием последнего до кипения. После чего расплавленный металл с помощью мешалки диспергируют на мелкие капли и добавляют к нему небольшими порциями серу. Полученный продукт освобождают от растворителя отгонкой под вакуумом, фильтруют в расплавленном состоянии через стеклянный фильтр и снова переплавляют. Весь процесс занимает 20-30 ч 2.
Недостатками способа являются длительность процесса и сложность его за счет большого числа операций, использование токсичных и взрывоопасных растворителей.
Поставленная цель достигается тем, что согласно способу получения полисульфидов натрия путем взаимодействия предварительно диспергироЕванного расплавленного натрия с элементарной серой при повышенной температуре, расплав натрия с температурой 120-200°С вводят со скоростью 0,01-0,03 мл/с в pacii.uia серы с температурой 250-350°С.
Серу предварительно нагревают в среде инертного газа.
5 Взаимодействие натрия с серой при 250350°С позволяет получать полисульфид натрия в расплавленном состоянии, что позволяет избежать блокировки капель натрия твердым продуктом и значительно увеличить скорость реакции взаимодействия, а значит и интенсивность всего процесса. Введение расплавленного натрия через делительное устройство позволяет очищать его от примесей окислов и гидроокисей, которые всегда имеются на его поверхности,
г а следовательно, получать полисульфид более высокой степени чистоты. Этому способствует и отсутствие в предлагаемом способе органическогд растворителя, поскольку полисульфид натрия получается свободнымот продуктов взаимодействия натрия с раство0 рителем, в частности углерода; карбидов натрия и др. Кроме того, уменьшаются загрязнение окружающей среды токсичными органическими растворителями и взрывоопасность производства.
5Предлагаемый способ осуществляется
Похожие патенты SU1129186A1
Реферат патента 1984 года Способ получения полисульфидов натрия
1. СПОСОБ ПОЛУЧЕНИЯ ПОЛИСУЛЬФИДОВ НАТРИЯ путем взаимодействия предварительно диспергированного расплавленного натрия с элементарной серой при повышенной температуре, отличающийся тем, что, с целью интенсификации и упрощения процесса, расплав натрия с температурой 120-200°С вводят со скоростью 0,01-0,03 мл/с в расплав серы с температурой 250-3500°С. 2. Способ по п. 1, отличающийся тем, что серу предварительно нагревают в среде инертного газа.
Полисульфиды
Из Википедии — свободной энциклопедии
Полисульфиды щелочных металлов образуются при взаимодействии элементарной серы с соответствующим сульфидом (при сплавлении или в концентрированном растворе):
N a 2 S 2 + S n S → S n S 2 + N a 2 S <\displaystyle <\mathsf 
2 — окислитель); ( N H 4 ) 2 S 2 + S n S → ( N H 4 ) 2 S n S 3 <\displaystyle <\mathsf <(NH_<4>)_<2>S_<2>+SnS\rightarrow (NH_<4>)_<2>SnS_<3>>>> 

2 — восстановитель).
При взаимодействии с кислотами разлагаются с образованием сульфанов, серы и H2S. Также как и пероксиды, персульфиды способны диспропорционировать:
N a 2 S 2 → N a 2 S + S <\displaystyle <\mathsf 
2 — окислитель, восстановитель); 2 F e S 2 → 2 F e S + 2 S <\displaystyle <\mathsf <2FeS_<2>\rightarrow 2FeS+2S>>> 
Присоединение серы к солям синильной кислоты лучше всего протекает при действии на них легко отдающего S полисульфида аммония по схеме (для двусернистого аммония):
K C N + ( N H 4 ) 2 S 2 → K N C S + ( N H 4 ) 2 S <\displaystyle <\mathsf
База кодов ТН ВЭД
С учетом исключений, указанных во вступлении (в общих положениях пояснений) к данной подгруппе, в эту товарную позицию включены сульфиды металлов (соли сероводорода (H2S) товарной позиции 2811). Старое название «кислые соли сероводородной кислоты» («sulphydrates») (гидросульфиды) иногда применяется к кислым сульфидам. Сульфиды неметаллов из данной товарной позиции исключаются (товарная позиция 2813).
а) Сульфид натрия (Na2S). Получается восстановлением сульфата натрия с помощью угля. Безводный продукт в виде беловатой массы пластинок (концентрированный или расплавленный сульфид), растворимый в воде и сульфатирующийся на воздухе; может существовать в виде гидратированных кристаллов (с 9 молекулами воды) бесцветных или зеленоватых в зависимости от степени чистоты. Умеренный восстановитель, используемый при получении органических соединений. При флотационных процессах способствует абсорбции масла на поверхности руд за счет осернения. Используется также для удаления щетины при дублении, в косметических препаратах и как средство против паразитов.
б) Кислый сульфид натрия (гидросульфид) (NaHS). Получается действием сероводорода на нейтральный сульфид. Бесцветные кристаллы, растворимые в воде. Используется для удаления шерстного покрова при дублировании, при крашении, как поглотитель меди при очистке никеля, как восстановитель в органическом синтезе, и т.д.
(2) Сульфид цинка (ZnS). Искусственный сульфид цинка получается в гидратированной форме осаждением тетрагидроксоцинката (II) щелочного металла сульфидом натрия. Белая паста или порошок, часто содержащая оксид цинка и другие примеси. Используется или в чистом виде, или в смеси с оксидом магния как пигмент в резиновой промышленности. Соосажденный с сульфатом бария образует литопон (товарная позиция 3206). Активированный серебром, медью и т.д., образует люминофор товарной позиции 3206. Следует отметить, однако, что сульфид цинка входит в данную товарную позицию только в несмешанном и неактивированном виде.
Из данной товарной позиции исключаются цинковая обманка (природный сульфид цинка) (товарная позиция 2608) и вюрцит (также природный сульфид цинка) (товарная позиция 2530).
(3) Сульфид кадмия (CdS). Искусственный сульфид получают осаждением из раствора кадмиевой соли (например, сульфата) сероводородом или сульфидом щелочного металла. Желтый пигмент (кадмиевый желтый) используется в живописи и при производстве матового стекла; соосажденный с сульфитом бария, образует ярко-желтое красящее вещество, применяемое при изготовлении красок или керамики (товарная позиция 3206).
Из данной товарной позиции исключается природный сульфид кадмия (гринокит) (товарная позиция 2530).
(4) Кислый сульфид аммония (гидросульфид аммония) (NH4.HS). Кристаллические хлопья или иголки; очень летучий. Используется в фотографии и в органическом синтезе.
(5) Сульфид кальция (CaS). Получается кальцинированием смеси сульфата кальция и углерода. Сероватая или желтоватая масса, иногда люминесцирующая, почти не растворимая в воде. Часто содержит сульфат и другие примеси. Используется в чистом виде или обработанный оксидом мышьяка III, или известью для удаления шерстного покрова при обработке шкур. Применяется также для удаления волос в косметике, как микробицид в медицине, в металлургии и при изготовлении люминесцентных красок.
(6) Сульфиды железа. Наиболее важным искусственным сульфидом железа является сульфид железа (II) (FeS), получаемый плавлением смеси серы и железных опилок. Имеет форму пластинок, палочек или кусочков черноватого цвета с металлическим блеском. Применяется при получении сероводорода и в керамической промышленности.
(7) Сульфид стронция (SrS). Сероватый продукт, при контакте с воздухом становится желтым. Используется для удаления щетины в дубильном производстве, в косметике и при изготовлении люминесцентных красок.
(8) Сульфиды олова. Искусственный сульфид олова (IV) (дисульфид олова) (SnS2) получается нагреванием серы с хлоридом аммония и оксидом олова или амальгамой. Золотисто-желтые хлопья или порошок, не растворимый в воде и сублимирующийся при нагревании. Используется для бронзирования древесины, гипса и т.д.
а) Искусственный трисульфид (Sb2S3). Получают действием кислоты на природный сульфид, растворенный в гидроксиде натрия в виде красного или оранжевого порошка (осажденный трисульфид). Используется или в чистом виде, или в смеси с пентасульфидом, или другими продуктами в качестве пигмента в резиновой промышленности (сурьмяная киноварь, красная сернистая сурьма). Плавленный природный сульфид образует черный трисульфид, применяемый в пиротехнике, для изготовления спичечных головок, взрывающихся пистонов и капсюлей (с хлоратом калия), порошка для фотовспышек (с хроматом калия) и т.д. Горячая обработка карбонатом натрия дает «минерал кермес» («kermes mineral»), состоящий, в основном, из трисульфида сурьмы и диоксостибата (III) натрия (sodium pyro-antimonate), использующийся в медицине (товарная позиция 3824).
(б) Пентасульфид (golden antimony sulphide) (пятисернистая сурьма, Sb2S5). Получают окислением раствора тиодиоксостибата (V) натрия (соль Шлиппе). Оранжевый порошок, постепенно разлагающийся даже в темноте. Используется для получения грунтовок, для вулканизации и окрашивания резины, в лекарственных препаратах для людей (отхаркивающее) или для ветеринарных целей.
Природный сульфид сурьмы (стибнит) и оксосульфид сурьмы (кермезит) из данной товарной позиции исключаются (товарная позиция 2617).
10) Сульфид бария (BaS). Получается восстановлением природного сульфата (баритов, товарная позиция 2511) с помощью угля. В чистом виде представляет собой белое порошкообразное или комковатое вещество; загрязненный продукт имеет сероватый или желтоватый цвет. Токсичный. Используется аналогично сульфиду стронция.
11) Прочие сульфиды. К ним относятся:
а) Сульфиды калия (нейтральные и кислые). Гидросульфид калия используется для получения меркаптанов.
(б) Сульфиды меди, используемые для изготовления электродов и красок, устойчивых к действию морской воды. Природный сульфид меди (ковеллит, халькоцит) из данной товарной позиции исключают (товарная позиция 2603).
в) Сульфид свинца, используемый в керамической промышленности; природный сульфид свинца (галенит) из данной товарной позиции исключают (товарная позиция 2607).
12) Полисульфиды, классифицируемые в данной товарной позиции, являются смесями сульфидов тех же металлов.
а) Полисульфид натрия получают нагреванием серы с карбонатом натрия или нейтральным сульфидом натрия. Содержит, в основном, дисульфид натрия (Na2S2), трисульфид и тетрасульфид и примеси (сульфат, сульфит и т.п.). Продукт представляет собой зеленоватые пластины, растворимые в воде, окисляющиеся на воздухе и очень гигроскопичные. Содержится в плотно закрытых контейнерах. Используется, главным образом, как восстановитель в органическом синтезе (приготовление сернистых красителей), во флотационных процессах, при получении полисульфидов этилена, искусственного сульфида ртути, серных ванн или смесей для лечения чесоточных заболеваний.
б) Полисульфид калия («серная печень») используется в тех же целях, что и полисульфид натрия и, в частности, для серных ванн.
Из этой товарной позиции исключаются следующие природные сульфиды:
а) Сульфид никеля (миллерит) (товарная позиция 2530),
б) Сульфид молибдена (молибденит) (товарная позиция 2613),
в) Сульфид ванадия (патронит) (товарная позиция 2615),
г) Сульфид висмута (висмутинит) (товарная позиция 2617).
Полисульфидные олигомеры. Синтез. Структура. Свойства.
Содержание
Свойства полисульфидных олигомеров
Герметики на основе полисульфидных олигомеров (ПСО), в первую очередь, на основе жидких тиоколов, нашли широкое применение в авиационной промышленности, машиностроении и в строительстве, благодаря уникальному комплексу свойств – выдающейся маслобензостойкости, газонепроницаемости, атмосферостойкости и возможности долговременной эксплуатации в широком температурном интервале.
Синтез полисульфидных олигомеров
В промышленности синтез жидких тиоколов осуществляется путем поликонденсации водных растворов полисульфида натрия с органическими галогенидами с получением дисперсии высокомолекулярного каучука последующим расщеплением ее по дисульфидным связям и получением жидкого тиокола с концевыми SH-группами.
В качестве исходных мономеров для получения полисульфидных олигомеров (ПСО) широко используются органические ди- и тригалоидопроизводные и полисульфиды натрия различного состава. Однако, при синтезе серосодержащих олигомеров характерна недостаточная селективность реакции поликонденсации и расщепления, что приводит к разнозвенности полимеров и разбросу в свойствах вулканизатов.
Кроме того, в процессе получения тиоколов образуется значительное количество сточных вод. Указанные недостатки промышленного синтеза олиготиолов определили поиск альтернативных способов получения. В настоящее время существует множество новых методов синтеза тиоколовых олигомеров и их модифицированных аналогов, информация по которым «разбросана» по различным периодическим изданиям.
Методы синтеза
Данный метод привлекает возможностью проведения процессов синтеза и выделения жидкого тиокола практически в одном реакторе с получением жидких тиоколов высокой степени чистоты и со строго заданными свойствами.
Получение жидкого тиокола через соли Бунте происходит следующим путем:
Этот метод синтеза полисульфидных олигомеров позволяет получать тиоколы с заданными молекулярными параметрами, с выходом 98–99 %, практически по безотходному замкнутому циклу.
промежуточный метастабильный комплекс
Например, при использовании в качестве дигалогена би-3-хлор-3-окипропилового эфира синтезированы олигомеры, имеющие в основной цепи ОН-группы. Вулканизаты этих олигомеров имеют большую, в сравнении с традиционными ПСО, адгезию к субстратам. ВНИИСК (г. Ленинград), разработан способ синтеза ТПМ–полимера, представляющего собой политиолполиолполиэфир структуры:
В качестве исходного полиэфира использовался полиоксипропиленоксиэтиленполиол марки «Лапрол» с молекулярной массой 1000–6000. Получение ТПМ-полимера осуществляется через получение хлорсодержащего лапрола с функциональностью по хлору 2,1–3,0.
Полученный олиготиол представляет собой низковязкую жидкость (1,0–3,0 Па*с при20 °С), способную вулканизоваться всеми отвердителями, характерными для жидкого тиокола. Его вулканизаты обладают хорошим комплексом свойств, однако более значительно, чем герметики на основе жидкого тиокола, набухают в воде.
Полисульфид-полиэфир содержит 7 % серы и 5,7 % SH-групп. Получение таких олигомеров осуществляется по такой же схеме, которая в свое время была предложена в работах. Герметики на их основе обладают высокими физико-механическими свойствами, водостойкостью и удовлетворительной стойкостью к действию растворителей.
Соответствующие вещества на стадии поликонденсации включаются в полимерную цепь и пространственную сетку. В некоторых случаях вещества играют роль диспергирующихся усиливающих наполнителей.
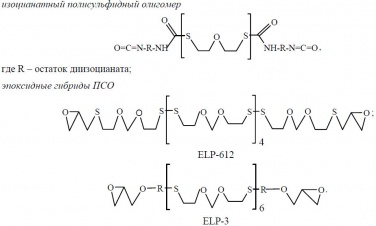
Такие варианты модификации ПСО на стадии синтеза позволяют получать материалы с иной структурой основной цепи. Синтезированные продукты могут иметь как концевые тиольные группы, так и, например, эпоксидные, изоцианатные и другие группы.
Последнее способствует увеличению скорости отверждения однокомпонентных герметиков на его основе влагой воздуха.
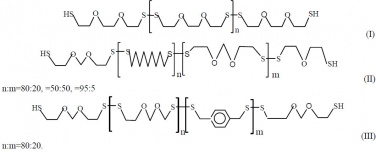
Благодаря введению большого углеводородного фрагмента и наличию ароматического углеводорода, олигомеры (II) и (III) напротив характеризуются невысокой скоростью прохождения водяного пара.
Полимер (III) обладает повышенной термостабильностью. По сравнению с «обычными» жидкими тиоколами олигомер (III) не растворим в эпоксидных смолах на основе дифенилолпропана (бисфенол А). Это обстоятельство позволяет использовать его не только в качестве эластификатора, но и для повышения ударной вязкости эпоксидных смол благодаря образованию эластичных микродоменов.
Пермапол
В США синтезирован новый класс полисульфидных жидких каучуков – «Пермаполов» – с концевыми SH-группами, обладающих существенными преимуществами в сравнении с традиционными жидкими тиоколами.
Вулканизаты на основе пермаполов, благодаря высокимфизико-механическим свойствам, адгезионными технологическим показателям, нашли применение в авиации для антикоррозионной защиты резервуаров с топливом и др.
Фирмой Products research and Chemicals Corporation (PRC) налажено производство олигомеров пермапол Р-2 и Р-3. Пермапол Р-2 рекомендуется для герметизации стеклопакетов:
Отсутствие «слабых» формалиевых структур и дисульфидных связей в политиоэфирах пермапол Р-3 придает им некоторые преимущества. Структура Р-3 обусловливает их большую, в сравнении с традиционными ПСО, агрессивостойкость:
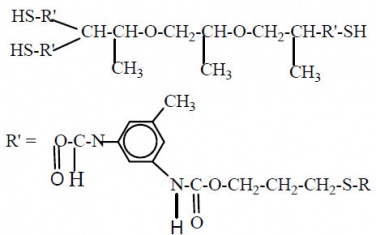
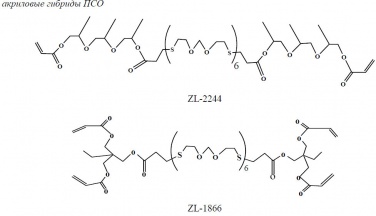
При этом функциональные группы олиготиола могут иметь различную природу. В работе исследовался способ синтеза ПСО с концевыми гидроксильными группами на основе дитиодиэтиленгликоля. Это позволило получать олигомеры, обладающие комплексом свойств, присущих тиоколовым и уретановым материалам, при меньшем количестве побочных отходов. Модификация концевых групп на стадии синтеза олиготиола может осуществляться за счет постреакций меркаптогрупп с реакционноспособными соединениями. Ниже приведены варианты синтезированных продуктов имеющих различные концевые группы:
При проведении поликонденсации возможно использование непредельных сомономеров,например, стирола, метилметакрилата, изопрена, винилацетата. В результате использования технологии, аналогичной промышленному синтезу ПСО, получается однородная водная дисперсия, сохраняющая свою стабильность долгое время. Она хорошо смешивается с синтетическими латексами любых типов и ввиду высокого содержания серы может использоваться в качестве вулканизующего агента для латексов и каучуков эмульсионной полимеризации.
При использовании в качестве сомономеров смеси стирола и нитрила акриловой кислоты с дихлорэтаном в равном соотношении получается сополимер со статическим распределением звеньев:
где х=0–30, у=3–5, n=1 или 3.
Молекулярная масса продукта 1000–4500.
Сополимер отверждается при 20 °С. Продукты отверждения проявляют свойства эластомера, имеют хорошую адгезию, применяются для герметизации швов в строительстве и в качестве заливочных компаундов в электронике.
Таким образом, рассмотренные методы синтеза позволяют получать ПСО с регулируемыми молекулярной массой, распределением по типу функциональности, степенью разветвленности и содержанием функциональных групп.
При модификации на стадии синтеза тиоколов реакционноспособными соединениями возможно изменение природы основной цепи и функциональных групп ПСО. Введение в состав молекулы тиокола фрагментов реакциионноспособных соединений приводит к существенному увеличению адгезионного взаимодействия с субстратами, а также к повышению прочностных характеристик и химической стойкости отвержденных материалов.
Это позволяет значительно расширить области практического применения модифицированных олиготиолов.
Источник:
журнал «Известия Волгоградского государственного технического университета» (Выпуск № 1 / 2006), авторы: Минкин В. С., Нистратов А. В., Ваниев М. А.