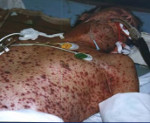
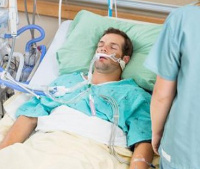
Полиорганная недостаточность
Полиорганная недостаточность (Синдром полиорганной недостаточности, СПОН, ПОН) — тяжёлая неспецифическая стресс-реакция организма, совокупность недостаточности нескольких функциональных систем, развивающаяся как терминальная стадия большинства острых заболеваний и травм. Главной особенностью полиорганной недостаточности является неудержимость развития повреждения органа или системы до такой глубины, что он не способен поддерживать жизнеобеспечение организма. На долю синдрома приходится до 80 % общей летальности палат реанимации и интенсивной терапии хирургических стационаров.
Следует отличать синдром полиорганной недостаточности от терминальной поливисцеропатии, когда в результате хронического патологического процесса или старости последовательно и необратимо утрачивают функции все структурно-функциональные системы организма.
Содержание
История
Термин «полиорганная недостаточность» впервые появился в работе N.Тylney и сотр. «Последовательная системная недостаточность после разрыва аневризмы брюшной аорты. Нерешенная проблема послеоперационного лечения» (1973). В дальнейшем другими учёными — А.Baue (1975), B.Eisman (1977) и D.Fry (1980-1982), были окончательно выделены особенности этого состояния и его дефиниции.
Этиопатогенез
Полиорганная недостаточность развивается как исход тяжёлой сочетанной травмы, эклампсии, сепсиса, инфекционно-токсического и геморрагического шока, асистолии, комы, вызванной диабетом, менингоэнцефалитом, отравлениями.
В основе развития синдрома лежит острое снижение обмена веществ и энергообразования в результате расстройств метаболизма и микроциркуляции в тканях, что приводит к нарушению функций и структуры органов. Этиологические факторы (тяжёлая травма, токсические агенты и др.), повреждая клеточные и сосудистые мембраны, приводят полиморфноядерные нуклеары (гранулоциты) и эндотелиоциты в состояние «кислородного взрыва», что провоцирует выброс огромного количества медиаторов полиорганной недостаточности, обладающих разнонаправленными эффектами. Всего известно более двухсот медиаторов, в том числе:
Развивается комплекс патологических изменений как в очаге поражения, так и на уровне формирования механизмов адаптации (гипофиз, гипоталамус, кора надпочечников).
Выделяют 3 фазы патологического процесса:
Клиника
Клиника синдрома состоит из проявлений недостаточности каждой из затронутых систем организма. Кроме того, медиаторы повреждения формируют синдром системного воспалительного ответа (ССВО) — генерализованную системную воспалительную реакцию. ССВО характеризуется следующими проявлениями:
Прогноз
При развитии недостаточности 3 и более органов и систем прогноз неблагоприятный. Летальность по разным авторам колеблется от 35% до 70%.
Полиорганная недостаточность
Полиорганная недостаточность – это тяжелое общее патологическое состояние, которое характеризуется нарушением или отсутствием функционирования двух и более систем организма ребенка, подростка или взрослого человека.
Она была выделена в отдельный синдром в конце прошлого века. Исследователь В. А. Гологорский считает, что при возникновении полиорганной недостаточности изменения в организме (нарушения) однотипные, независимо от причин, которые привели к такому состоянию организма.
Что провоцирует / Причины Полиорганной недостаточности:
Причиной может быть травма, инфекция, гипоперфузия тканей, воспаление, гиперметаболизм. Эти факторы не обязательно становятся причиной полиорганной недостаточности. Но любой из них может привести к развитию мультифокальных патофизиологических процессов. В клеточных повреждениях важную роль играют медиаторы. Количество их при выбросе зависит от тяжести повреждающего фактора.
Патогенез (что происходит?) во время Полиорганной недостаточности:
В патогенезе полиорганной недостаточности у человека важное место занимаются серьезные метаболические нарушения. В терминальной стадии заболевания выражен катаболизм протеинов мышц. Он возникает из-за углеводов и жиров, если пациент находится в очень тяжелом состоянии, и если формируется невосполнимый энергетический дефицит. Развивается протеинозависимый энергетический обмен, в основе которого лежат активация протеолиза и распад структурных белков жизненно важных органов, мышечной ткани.
Активированные вирусные и микробные токсины, а также мастоциты и макрофаги выделяют вещества, которые, в свою очередь, могут провоцировать тканевые и клеточные повреждения. В патогенез имеет месте свободнорадикальное окисление. Оно повреждает клетки.
В развитии полиорганной недостаточности играет роль нарушение иммунитета, а также септические процессы. Наиболее частыми причинами сепсиса становятся грамотрицательные бактерии, которые попадают из желудочно-кишечного тракта взрослого или ребенка в кровоток и органы. Потому исследователи предполагают, что ЖКТ – своеобразный генератор полиорганной недостаточности.
В патогенезе важная роль отводится:
В организме происходят явления гипоксии и реперфузии, в результате чего происходит агрегация и адгезия нейтрофилов, а эндотелий активируется. Медиаторы нейтрофилов разрушают клеточную мембрану в органах и тканях, из-за чего тканевая гипоксия становится еще хуже. В начале шока активируется система комплемента, фибринолиза, коагуляции. Тканевая травма активирует комплемент по альтернативному пути, а бактерии – по классическому и альтернативному.
Увеличиваются темпы выработки провоспалительных цитокинов. Нарастают тканевые повреждения, что усугубляет тяжесть полиорганной недостаточности. В начальной стадии тяжелой травмы активируется большое количество клеток, которые синтезируют медиаторы, токсически действующие на ткани. Возникает системная воспалительная реакция. Часто системное воспаление вызывает гипоксию и повреждение функции органов.
В самом начале развития процессов система коагуляции участвует в патогенезе полиорганной недостаточности. Активация системы коагуляции и угнетение фибринолиза вызывают тяжелую органную гипоперфузию.
Симптомы Полиорганной недостаточности:
Проявляющиеся при полиорганной недостаточности симптомы и их прогресс вызваны, в большинстве случаев, сочетанием нарушений в дыхательной и сердечнососудистой системе, а также нарушениями в печени и почках человека. Исследователями выделено 4 стадии заболевания:
Вовремя диагностировать полиорганную недостаточность затруднительно. Специальное исследование или ретроспективный анализ показывают, что еще в начале нарушений и человека была латентная недостаточность нескольких или многих органов. Современные методы диагностики этой болезни несовершенны.
Синдром полиорганной недостаточности проявляется у детей с инфекционными болезнями при тяжелой их форме. При легкой форме болезни поражения органов выявить не удается. Но лабораторные и инструментальные методы позволяют выявить компенсированную или субкомпенсированную полиорганную недостаточность, которая говорит о том, что состояние может усугубиться, функционирование этих органов станет в будущем еще хуже.
Нарастание токсического синдрома приводит к прогрессированию нарушений кровотовка в почках, коже, печени, в крайних случаях развивается ишемия и циркуляторная блокада, которые типичны для терминальной стадии заболевания. Также в крови человека происходит накопление метаболитов, которые оказывают токсическое действие на организм, что проявляется в нарушении выделительной функции почек, печени и желудочно-кишечного тракта.
Нарушение биохимических процессов детоксикации в печени доказывается накоплением аммиака в крови детей и взрослых с токсикозами. В крови собирается свободный фенол, в печени происходит его связывание с глюкуроновой или серной кислотой, он должен выделяться с мочой. О почечной недостаточности говорит скопление пептидов средней массы в крови.
К развитию эндотоксемии приводит реакция централизации системного кровообращения, которая вызывает и циркуляторную гипоксию органов и тканей организма. Что касается легких, возникает респираторный дистресс-синдром. Нарушается дыхание, отекают легкие, в организм не поступает достаточное количество кислорода. У человека учащается пульс и появляется одышка. Врачи могут обнаружить признаки цианоза: бледность или посинение кожи, пятная на коже. Конечности становятся прохладными.
Что касается почек, при полиорганной недостаточности высокий риск появления олигурии. В организме задерживается моча. Если человек взрослый, он может заметить это сам. Если ребенок мало «ходит в туалет по-маленькому», это могут заметить родители или его воспитатели. Этот симптом проявляется не только при полиорганной недостаточности, потому исключительно по нему делать выводы о диагнозе нельзя.
Если работа почек нарушена, в моче находят содержание белка, лейкоцитов и эпителия выше нормы, также могут быть найдены эритроциты. Когда олигурия прогрессирует, развивается анурия.
Что касается печени, при полиорганной недостаточности возникает холестатическая желтуха. Проявления такие:
При полиорганной недостаточности часто возникает ДВС-синдром, при котором фиксируют рассеянное свертывание крови. Блокируется микроциркуляция, что приводит к изменениям дистрофического характера. ДВС-синдром может проявляться геморрагическим синдромом, в основном это появление подкожных гематом и кровоподтеков в подкожно-жировой клетчатке.
Одно из проявлений полиорганной недостаточности у детей и взрослых – нарастающая острая сердечная недостаточность. ОСН считается одним из самых тяжелых нарушений кровообращения. Мышца сердца теряет свое свойство сокращения, потому перекачивание перетекающей по нему крови в разы усложняется, что приводит неминуемо к застою крови. Следствием развивающейся ОСН может стать астма или отек легких, все эти состояния крайне опасны для жизни человека.
При правожелудочковой недостаточности как проявлении полиорганной недостаточности может увеличиться печень; все органы и ткани очень плохо снабжаются кислородом, появляются отеки. Человеку становится всё сложнее дышать.
Одно из проявлений полиорганной недостаточности – язвы желудка и 12-перстной кишки. В верхней части живота появляются боли, которые в большинстве случаев постепенно усиливаются. Язвенную болезнь неминуемо сопровождает изжога. Дети маленького возраста не могут сказать о своих ощущениях, потому у них нельзя заподозрить язву по выше перечисленным симптомам.
Со стороны ЦНС полиорганная недостаточность проявляется заторможенностью, острым психозом, а крайнее состояние – коматозное.
Лечение Полиорганной недостаточности:
Полиорганная недостаточность во многих случаях оканчивается смертью. Чтобы предотвратить летальный исход, важно своевременное и правильное лечение. В комплекс лечения срочно должны быть включены методы функциональной поддержки органов жизнеобеспечения:
Терапия включает методы экстракорпоральной элиминации токсичных веществ:
Эти методы следует применять, пока не восстановятся функции органов человека, и организм не будет в состоянии сам поддерживать собственный гомеостаз.
Профилактика Полиорганной недостаточности:
Специфические методы профилактики не разработаны.
Полиорганная недостаточность ( Синдром полиорганной недостаточности )
Полиорганная недостаточность – одновременное или последовательное поражение нескольких систем с первоначальным преобладанием симптомов отказа одной из них. Определяющими признаками являются цианоз, одышка, отеки, анурия, гипотония, шоковое состояние. Диагноз устанавливается на основании клинической картины, данных лабораторного и аппаратного обследования. Специфическое лечение: поддержка дыхания и сердечной деятельности, стабилизация гемодинамики, устранение патогенетического фактора (борьба с инфекцией, коррекция метаболических нарушений, восстановление ОЦК, нормализация гемостаза), искусственная и естественная детоксикация.
МКБ-10
Общие сведения
Полиорганная недостаточность (ПОН) – патология, возникающая преимущественно у пациентов реанимационных отделений. Как самостоятельная нозологическая единица впервые была описана в 1973 году, до этого считалась сочетанием двух и более не связанных между собой нарушений. Частота встречаемости составляет около 5-10% от общего количества больных. Смертность в этой группе приближается 60%. Чаще погибают пациенты, имеющие сбои в работе трех органов. Состояние развивается на 3-5 сутки после успешного восстановления сердечной деятельности, при тяжелых сочетанных травмах, отравлениях, эндотоксикозах. В основе развития лежит синдром системного воспалительного ответа.
Причины полиорганной недостаточности
ПОН возникает в результате патологических изменений, происходящих в организме после остановки и последующего восстановления работы сердца. Кроме того, она может формироваться на фоне тяжелой политравмы, инфекционно-токсического шока, сепсиса, перитонита. Чаще развивается, если один из органов, вовлеченных в процесс, ранее был поражен хронической патологией или изменен в результате воздействия первичного фактора (контузия легкого при ДТП, снижение сократительной способности миокарда при остром коронарном синдроме). В число этиофакторов включают:
Патогенез
Полиорганная деструкция имеет несколько механизмов развития, основным из которых является ишемическое повреждение органов. Часть клеток отмирает, остальные переходят в анаэробный режим гликолиза. Основные повреждения возникают при восстановлении кровотока. В этот период образуется большое количество свободных радикалов, вызывающих перикисное окисление тканей. Вторым патогенетическим механизмом является интенсивное тромбообразование на начальной стадии ДВС-синдрома. Образующиеся микроэмболы нарушают проходимость капиллярной сети, что усиливает ишемию.
Отеки в результате повышенной проницаемости сосудов приводят к накоплению жидкости в брюшной полости, усилению внутриабдоминальной компрессии. Происходит механическое сжатие органов живота, подъем диафрагмы с ограничением подвижности легких. Отмечается рост внутригрудного давления, уменьшение рабочего пространства сердца. Нарушается отток крови от мозга. В процесс вовлекается центральная нервная система, развивается церебральный отек с появлением неврологической симптоматики.
Классификация
Деление ПОН на группы производится по результатам оценки деятельности органов и систем, общего состояния пациента. Для этого может быть использована шкала Apache II или Д. Маршалла, созданная в 1995 году специально для работы с больными, страдающими полиорганной недостаточностью. На практике более актуальным является метод А. Л. Левита, представленный в 2000 году. Согласно ему, каждая из систем может находиться в компенсированном, субкомпенсированном или декомпенсированном состоянии. Полиорганная недостаточность определяется как тяжелая при декомпенсации двух систем, как крайне тяжелая – при значительных изменениях в трех органах. Оценка проводится отдельно по каждому органу.
Симптомы полиорганной недостаточности
Клиническая картина зависит от наличия поражения тех или иных структур. Обычно на первый план выходят признаки изменений со стороны дыхательной системы. Отмечается одышка, диффузный цианоз, включение вспомогательной мускулатуры в процесс вдоха, потливость, психомоторное возбуждение. Пациенты, способные самостоятельно передвигаться, занимают вынужденное положение сидя с упором руками в кровать. Позднее активность сменяется заторможенностью, угнетением сознания.
Полиорганная недостаточность с поражением сердца проявляется загрудинными болями, нестабильностью гемодинамики, накоплением жидкости в мягких тканях за счет усиления пролиферации плазмы сквозь сосудистую стенку. Может возникать отек легких, сопровождающийся появлением розоватой пены изо рта. Выявляется компенсаторная тахикардия до 180 уд./мин, позднее сменяющаяся брадикардией с урежением ЧСС до 40 и ниже. На терминальной стадии происходит снижение чувствительности к инотропным средствам и альфа-адреномиметикам.
При почечно-печеночной разновидности болезни объем диуреза заметно снижается. Затем возникает анурия, требующая проведения гемодиализа. Обнаруживается гипогликемия, влекущая за собой нарушения сознания. У пациента развивается асцит, диспепсия, белковые отеки. Кожа и слизистые оболочки желтеют, возможна геморрагическая сыпь. Через несколько часов или дней обнаруживаются признаки печеночной энцефалопатии: больной не отдает себе отчет в своих действиях, не понимает, где находится, что с ним происходит.
Поражения ЖКТ характеризуются признаками обструкции, обусловленной механическим сдавлением кишечника. Определяется боль, вздутие, асимметрия передней брюшной стенки, задержка стула и газов, рвота. Отсутствует толерантность к кормлению. Возможно развитие стрессовой язвы и кишечной геморрагии, которая проявляется снижением уровня Hb, бледностью пациента, падением АД, возникновением или усилением ДВС синдрома при массивной кровопотере.
Осложнения
При успешном купировании полиорганное поражение может завершаться развитием отсроченных заболеваний. У 5% пациентов, повторно обратившихся за помощью в ЛПУ, диагностируют хроническую почечную недостаточность, примерно 2% больных испытывают симптомы ишемической болезни сердца или имеют признаки ХСН. Легочные изменения отмечаются в 3% случаев. В остром периоде осложнением является фибрилляция желудочков на фоне токсического поражения миокарда и тахикардии с ЧСС выше 160-180/мин. Возможно повреждение проводящей системы сердца с формированием СА или АВ блокады. Ишемия мозга нередко приводит к снижению умственных способностей, энцефалопатии, парезам, параличам.
Диагностика
Диагностика осуществляется по результатам клинического, лабораторного и инструментального обследования. Курировать пациентов должен анестезиолог-реаниматолог, однако провести первичный осмотр и установить предварительный диагноз для направления больного в профильное отделение может врач любой специальности, в том числе сотрудник бригады СМП. Дифференциальную диагностику проводят с сочетанной патологией нескольких систем организма, этиологически не связанной с механизмами развития рассматриваемого заболевания. Полная программа обследования включает:
Лечение полиорганной недостаточности
Терапия направлена на восстановление ОЦК, нормализацию реологических свойств крови, поддержку витальных функций, предотвращение последствий отсроченного характера. Полиорганная недостаточность должна быть купирована на стадии компенсации, это увеличивает вероятность полного восстановления. Применяются следующие лечебные воздействия на больного:
Прогноз и профилактика
Полиорганная недостаточность имеет благоприятный исход при раннем начале лечения. По мере прогрессирования процесса в организме накапливаются необратимые изменения, повышающие риск возникновения осложнений. Декомпенсированная форма болезни имеет неблагоприятный прогноз, в 60% случаев приводит к гибели пациента. Профилактика заключается в предотвращении ПОН. Следует купировать очаги инфекции, при объемных травмах начинать массивную инфузию еще на догоспитальном этапе, своевременно устранять имеющиеся нарушения гемодинамики и сердечного ритма. Важным моментом является контроль диуреза пациента, находящегося на лечении в ОРИТ. Разница между употребленной и выделенной жидкостью не должна составлять более 100-200 мл в сутки.
О лечении полиорганной недостаточности при COVID-19 рассказали в Сеченовском Университете

Согласно патогенезу, «цитокиновый шторм» является опосредованным последствием влияния коронавируса на иммунную систему человека. Шанс его возникновения может повыситься в случае тяжёлого течения заболевания и заражения побочными бактериальными инфекциями. А также другими факторами – средне-тяжёлым или тяжёлым течением заболевания, склонностью к тромбообразованию и быстрое прогрессирование болезни. Впоследствии он может привести к многочисленным осложнениям даже при успешном его погашении – для лёгких, сердца, сосудов и других органов.
«Краеугольным камнем в лечении коронавирусной инфекции является поддержание гипокоагуляции. Посредством прямого или опосредованного действия вируса выявляется склонность к тромбообразованию. Здесь в каждом учреждении необходимо использовать индивидуальный подход, руководствуясь рекомендациями, которые мы имеем на данный момент», – объяснил Борислав Силаев.
Он также напомнил, что необходимо проводить компьютерную томографию хотя бы раз в 7 суток, чтобы отследить динамику заболевания и потенциальные риски.
При лечении бактериального воспаления при коронавирусной инфекции важно знать о риске возникновения цитокинового шторма и своевременно проводить скрининг двух белков – прокольцитонина и C-реактивного белка. Диагностическими критериями возникновения цитокинового шторма являются нормальный или сниженный уровень прокальцитонина, фебрильная лихорадка, прогрессирующая полиорганная недостаточность, а также специфические показатели анализа крови.
Цитокиновый шторм – опасное явление, которое можно лечить как медикаментозно, так и экстрапорально. Но предпочтительнее не допускать его возникновения, и принимать меры для его предотвращения, подчеркнул эксперт.
Код вставки на сайт
О лечении полиорганной недостаточности при COVID-19 рассказали в Сеченовском Университете

Согласно патогенезу, «цитокиновый шторм» является опосредованным последствием влияния коронавируса на иммунную систему человека. Шанс его возникновения может повыситься в случае тяжёлого течения заболевания и заражения побочными бактериальными инфекциями. А также другими факторами – средне-тяжёлым или тяжёлым течением заболевания, склонностью к тромбообразованию и быстрое прогрессирование болезни. Впоследствии он может привести к многочисленным осложнениям даже при успешном его погашении – для лёгких, сердца, сосудов и других органов.
«Краеугольным камнем в лечении коронавирусной инфекции является поддержание гипокоагуляции. Посредством прямого или опосредованного действия вируса выявляется склонность к тромбообразованию. Здесь в каждом учреждении необходимо использовать индивидуальный подход, руководствуясь рекомендациями, которые мы имеем на данный момент», – объяснил Борислав Силаев.
Он также напомнил, что необходимо проводить компьютерную томографию хотя бы раз в 7 суток, чтобы отследить динамику заболевания и потенциальные риски.
При лечении бактериального воспаления при коронавирусной инфекции важно знать о риске возникновения цитокинового шторма и своевременно проводить скрининг двух белков – прокольцитонина и C-реактивного белка. Диагностическими критериями возникновения цитокинового шторма являются нормальный или сниженный уровень прокальцитонина, фебрильная лихорадка, прогрессирующая полиорганная недостаточность, а также специфические показатели анализа крови.
Цитокиновый шторм – опасное явление, которое можно лечить как медикаментозно, так и экстрапорально. Но предпочтительнее не допускать его возникновения, и принимать меры для его предотвращения, подчеркнул эксперт.
Неудачи интенсивного лечения полиорганной недостаточности: патофизиология и потребность в персонификации (обзор литературы)
1 ФГБНУ «Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний», Кемерово
2 ФГБОУ ВО «Кемеровский государственный медицинский университет», Кемерово
3 ФГБУ «Национальный медицинский исследовательский центр хирургии им. А.В. Вишневского», Москва
Для корреспонденции: Григорьев Евгений Валерьевич, д-р мед. наук, профессор, заведующий кафедрой анестезиологии и реаниматологии, Кемерово; e-mail: grigorievev@hotmail.com
Для цитирования: Григорьев Е.В., Шукевич Д.Л., Плотников Г.П., Кудрявцев А.Н., Радивилко А.С. Неудачи интенсивного лечения полиорганной недостаточности: патофизиология и потребность в персонификации (обзор литературы). Вестник интенсивной терапии имени А.И. Салтанова. 2019;2:48-57. DOI: 10.21320/1818-474X-2019-2-48-57
Реферат
Полиорганная недостаточность (ПОН) — наиболее тяжелый исход критического состояния любого генеза (сепсис, травма, ишемия и реперфузия), планка летальности при данном синдроме не имеет тенденции к снижению. Обзорная статья предлагает прежде всего знакомство с ключевыми научными направлениями, по которым на данный момент развивается теория ПОН (исследование значимости аларминов, митохондриальная дисфункция, барьерная недостаточность, иммунологическое и неврологическое сопряжение, формы программированной гибели клеток, индуцированная иммуносупрессия, разрешение воспаления). Исследования доказывают целесообразность введения персонифицированного подхода к диагностике ПОН путем обоснования эндофенотипа критического состояния на основании комплекса иммунологических, геномных и клинических показателей.
Ключевые слова: системный воспалительный ответ, полиорганная недостаточность, алармины, митохондрии, иммунная супрессия, барьерная недостаточность, эндофенотип
Поступила: 22.02.2019
Принята к печати: 26.03.2019
Полиорганная недостаточность (ПОН) — множественная прогрессирующая и/или последовательная недостаточность функции органов («классическое» определение Baue et al.) — остается бременем для всей системы оказания медицинской помощи вообще и для служб реанимации в частности в силу высокой затратности лечения и поддерживающих мероприятий, низкой вероятности благоприятного развития сценариев ПОН, значимым влиянием ПОН на отдаленные исходы критических состояний (длительный когнитивный дефицит у выживших, низкое качество жизни, высокая частота физических ограничений даже в молодом возрасте пациентов) [1, 2]. В 1977 г. термин «полиорганная недостаточность» был впервые предложен группой Ben Eiseman, в статье которых было впервые описано наличие множественной органной недостаточности у 42 пациентов с тяжелой сочетанной травмой [3]. Существующие теории ПОН с момента описания данного синдрома предполагали наличие бимодального характера ПОН [4], однако суть бимодального феномена со временем изменилась: если в первой половине 90-х гг. ПОН зачастую носила характер «ятрогенного» повреждения вследствие отсутствия стандартных операционных процедур, данных широкомасштабных рандомизированных и основанных на доказательности исследованиях оценки влияния стратегических мер по лечению критических пациентов, то на данный момент подобные проблемы в основном решены (например, обоснование использования «концепции малых дыхательных объемов» при остром респираторном дистресс-синдроме (ОРДС) позволило нивелировать неблагоприятные клинические исходы, связанные не столько с собственно ОРДС, сколько с развитием вентилятор-индуцированного повреждения легких) [5, 6]. Тем не менее за «первым ударом» (first hit) следует второй пик формирования ПОН («хроническая» госпитальная инфекция мультирезистентными штаммами, реактивация вирусов, мальнутриция и кахексия, саркопения, иммуносупрессия, персистирующая зависимость от поддерживающей терапии), что, собственно, и обусловливает сложность лечения, ведет к формированию персистенции ПОН и делает практически неснижаемой планку госпитальной летальности и неблагоприятных исходов критических состояний — это, в свою очередь, обосновывает целесообразность изменения подходов как к диагностике, так и терапии ПОН путем внедрения эффекта персонификации и создания клинического, иммунологического и генетического портрета критического пациента [7].
Теория danger — принципиальный прорыв в патогенезе, в том числе и критических состояний, — объединила врожденный и приобретенный иммунитет и доказала схожесть и универсальность формирования так называемого ответа хозяина (host response) как при сепсисе, так и при воздействии на пациента неинфекционного характера повреждения (травма, ишемия/ре- перфузия) [8].
Клетки в условиях стерильной неинфекционной или инфекционной системной воспалительной реакции (СВР) обладают возможностью выброса так называемых аларминов или дистресс-ассоциированных паттернов (danger-associated molecular patterns — DAMP), теоретическое обоснование термина произошло от аналогичных молекулярных паттернов инфекционного (связанного с возбудителями — бактериями, вирусами, грибами) генеза — патоген-ассоциированных молекулярных паттернов (pathogen-associated molecular patterns — PAMP). Толл-подобные рецепторы (toll-like receptors — TLR), RAGE-рецепторы, нуклеотид-связывающие домены олигомеризации (NOD) и NOD-со- держащие богатые лейцином последовательности объединяются термином «паттерн-распознающие рецепторы» (PRR) и обладают универсальностью активации клеток макроорганизма в ответ на внешнюю стимуляцию. Внутриклеточные DAMP представлены молекулами, которые в физиологических условиях включены в нормальный цикл работы клетки, в таких условиях они не распознаются иммунной системой, что отличает их от воспалительных цитокинов. DAMP активируют PRR с дальнейшей активацией иммунного ответа, внеклеточные DAMP способны связываться с PRR после деструкции тканей и клеток в виде растворимой формы DAMP.
Локальный воспалительный ответ является важнейшим в отношении координации раннего тканевого ремоделирования, неоваскуляризации, активности ростовых факторов и реализации репарации как «исхода» и сбалансированности воспаления.
Выраженная деструкция тканей, значительная нагрузка микроорганизмами или инвазия высоковирулентных возбудителей вызывают дисрегуляцию системного воспалительного ответа. Локальный выброс цитокинов и активация воспаления могут быть избыточными в ответ на инфекционный или неинфекционный стимул. Цитокины активируют эндотелиоциты и вызывают фиксацию на поверхности эндотелиальной выстилки комплемента, в дополнение к этому неспецифические иммунные клетки (нейтрофилы и макрофаги) путем выброса свободных радикалов (СР) кислорода и токсических гранул могут вызвать локальный тканевой некроз. Все перечисленное ведет к дополнительному выбросу DAMP и потенцированию круга активности иммунного ответа [14].
Некроптоз и пироптоз являются вариантами несвязанной с апоптозом программированной клеточной гибели при дисрегуляции воспаления. С учетом альтернативного пути активации клеточной гибели подобный механизм ведет к выбросу дополнительных DAMP. Выброс ДНК из нейтрофилов и макрофагов формирует так называемые нейтрофильные внеклеточные ловушки (neutrophil extracellular trap — NET), которые выключают участок кровотока из системного кровообращения и способны уничтожать бактерии и клетки собственного организма путем нетоза (от аббревиатуры NET). Особенностью является и тот факт, что гибель клеток ведет к выбросу цитокинов вне локального очага повреждения, тем самым реализуя дистантный эффект потенцирования СВР и ПОН [15].
Митохондриальная ДНК (митДНК) уже в течение нескольких лет рассматривается как один из многообещающих кандидатных аларминов. Когда из поврежденных митохондрий вследствие разрыва мембран клеток выбрасывается содержимое, специфические компоненты митохондрий распознаются организмом PRR-системы первичного иммунитета как РАМР из-за схожести с N-формильными компонентами стенки клеток бактерий с последующей реализацией системного воспалительного ответа [16]. Особенностью является тот факт, что мит- ДНК способна индуцировать СВР вне наличия первичной бактериальной нагрузки. Более того, выброс мит- ДНК, который превышает возможности внутриклеточной аутофагии в отношении снижения уровня мит- ДНК, ведет к TLR-9 опосредованному системному воспалительному ответу в эндотелиоцитах, что может быть компонентом формирования системной барьерной недостаточности [17].
Барьерная недостаточность
Эндотелий — избирательная мембрана, регулирующая движение воды, электролитов, микро- и макромолекул и клеток между тканями и кровью. Известно, что эндотелий обладает свойствами активной регуляции подобных перемещений, и ряд авторов доказали важнейшую роль, которую играет эндотелий в реализации СВР и ПОН как при сепсисе, так и при неинфекционной СВР. Так, Deutschman et al. в своем обзоре показали, что основой для расстройства гомеостаза при ПОН может являться так называемая барьерная недостаточность. По сути, есть два компонента взаимосвязи ПОН и барьерной недостаточности: активация сигнальных молекул и вовлеченность эндотелиальной выстилки в генерализацию воспалительного ответа и формирование капиллярной утечки с активацией молекул, участвующих в системе гемостаза и развитии микротромбозов [18].
Ранее было изучено, что следствием экспрессии воспалительных рецепторов является инфильтрация лейкоцитами и гиперпродукция воспалительных медиаторов. По аналогии с лейкоцитами эпителиальные клетки ряда органов экспрессируют воспалительные рецепторы на своей поверхности и могут также участвовать в выбросе медиаторов (цитокины, хемокины, оксид азота) [19]. Таким образом, эндотелиоциты и эпителиоциты становятся ответственными за воспалительный ответ, эти клетки способны распознавать такие лиганды, как DAMP и PAMP, в тканях и продуцировать такие биологические активные молекулы, как хемокины и провоспалительные и противовоспалительные медиаторы, а также факторы свертывания. Механизмы подобного амплифицирования системного воспаления посредством ряда транскрипционных факторов (например, NF-κB) формируют специфические условия, которые рядом исследователей были объединены под названиями «СВР-индуцированный васкулит» (SIRS-induced vasculitis — SIVA, по Matsuda) или «шок-индуцированная эндотелиопатия» (shock-induced endotheliopathy — SHINE, по Johansson) [20, 21].
Сопряжение «эндотелий–гемостаз»
Могут быть выделены разные пути активации системы гемостаза на уровне микроциркуляции при системном воспалительном ответе. Важнейшим является формирование тромбина, обусловленное выбросом тканевого фактора. В условиях СВР основными источниками тканевого фактора являются моноциты, макрофаги, кроме того, усиливается роль в выбросе тканевого фактора активированного эндотелия [22, 23].
Активированные цитокинами эндотелиальные клетки экспрессируют тканевой фактор, который в свою очередь, через связь с факторами VII и X вызывает синтез тромбина и фибрина. Кроме того, есть мнение авторов о том, что тканевой фактор может вызывать «слущивание» (или шеддинг) микрочастиц с поверхности эндотелия, что также активирует СВР [24, 25].
Поверхность эндотелия вне системного воспаления «защищена» системой антикоагулянтов (система протеина C + S, антитромбин, ингибитор тканевого фактора), эндотелиальная дисфункция вызывает выключение всех трех компонентов защиты. При СВР наблюдаются угнетение синтеза антитромбина, усиление процесса разрушения путем воздействия активированных нейтрофилов и активное потребление. Функция ингибитора тканевого фактора повреждается за счет снижения синтеза гликозаминогликанов на поверхности эндотелия. Система протеина С+S повреждается за счет нарушения синтеза, наблюдается нарушение активности системы за счет нарушения экспрессии тромбомодулина на поверхности эндотелиоцитов [26].
Нейтрофильные внеклеточные ловушки
СВР и свертывание на уровне микроциркуляции могут взаимно усиливаться за счет формирования системы NET[27]. В ходе активации любыми лигандами PAMP и DAMP нейтрофилы формируют во внеклеточном пространстве так называемые сетевые структуры, имея в своем составе ДНК нейтрофила как основного структурного компонента ловушки, гистоны, биологически активные молекулы (эластаза нейтрофилов, лактоферрин, миелопероксидаза, катепсин G). Целью формирования ловушки является локализация и нейтрализация бактерий и грибов [28]. Факт образования ловушек был назван «нетоз», что отличает подобный вариант гибели нейтрофилов от некроза и апоптоза. Нити ДНК в составе ловушек способны контактно активировать калликреинкининовую систему и факторы системы свертывания крови, вызывать адгезию изменeнных тромбоцитов, блокировать микроциркуляцию за счет повреждения эндотелия путем воздействия медиаторов из состава ловушек, что может поддерживать СВР и ПОН в случае избыточного образования NET [29].
Гликокаликс
Апикальная поверхность эндотелиальных клеток, расположенных в кровеносных, лимфатических сосудах и сердце, покрыта гликокаликсом, слоем глубиной от 1 до 3 мкм. Компонентами гликокаликса являются заякоренные к клеткам протеогликаны, боковые цепи глюкозаминогликанов и сиалопротеины [30, 31]. В состав протеогликанов входит белковое ядро, в которому фиксированы глюкозаминогликаны; в состав белкового ядра входят синдикан, глипикан и перлекан. Данная сеть обволакивает поверхность эндотелия со стороны просвета кровеносного сосуда с проникновением в межклеточную расщелину вплоть до соприкосновения с внеклеточным матриксом базальной мембраны. Все растворимые компоненты (альбумин, тромбомодулин) и ряд сывороточных белков (антитромбин III, молекулы клеточной адгезии) связаны с внутрипросветной фазой гликокаликса.
Визуализация гликокаликса затруднена по причине нестабильности и хрупкости трехмерного слоя.
Классический метод — трансмиссионная электронная микроскопия — ограничена в использовании по причине технических особенностей методики и прежде всего невыполнимости метода in vivo. Другим методом является оценка флюоресценции гликокаликса с использованием флюоресцентных меток и конфокальной микроскопии. Прижизненная микроскопия и/ или использование полупроницаемых меток и оценка внутрисосудистого распределения являются одними из вариантов прижизненной оценки повреждения гликокаликса in vivo. Кроме того, методом иммуноферментного анализа могут быть определены сывороточные концентрации компонентов гликокаликса (синдикан) с оценкой ангиопоэтинов и уровня микроальбуминурии [32].
Гликокаликс играет ключевую роль в физиологии микроциркуляции и проницаемости эндотелиального барьера, поддерживая онкотический градиент, регулируя адгезию/миграцию лейкоцитов и ингибируя микроциркуляторный тромбоз [33].
Гликокаликс выполняет роль механотрансдуктора, который передает силы сдвига на эндотелиоциты посредством белковых комплексов. Конформация гликокаликса ведет к выбросу оксида азота, что вызывает изменение регуляции сосудистого тонуса и перераспределение кровотока и потока кислорода к тканям, что делает гликокаликс ответственным за микроциркуляторный дистресс-синдром в условиях шока, ишемии и реперфузии и состояния «нефизиологического кровообращения» (например, экстракорпоральная перфузия), для восстановления метаболического сопряжения органной функции и локальной гемодинамики [34].
Гликокаликс формирует так называемую модель «парацеллюлярной проницаемости», в которой он регулирует проницаемость жидкости и растворенных веществ и макромолекул в интерстициальное пространство из просвета сосуда, прежде всего данный фактор является ведущим в отношении проницаемости слоя «гликокаликс/внутрисосудистая жидкость» для альбумина, что, по сути, формирует так называемый синдром повышенной проницаемости капилляров [35].
В ходе системного воспаления структура и функция гликокаликса нарушаются с активным участием нарушенной функции в реализации эндотелиального повреждения и барьерной недостаточности. Наиболее значительным является разрушение нормальной парацеллюлярной проницаемости и перераспределения альбумина в интерстициальное пространство, далее по значимости идет нарушение сосудистого тонуса с депонированием крови в микроциркуляции, повреждение гепаран-сульфата с формированием прокоагулянтного локального внутрисосудистого гомеостаза и микротромбозами, экспрессия молекул межклеточной адгезии и усиление трафика лейкоцитов по эндотелиальной поверхности, оксидативное повреждение эндотелия [36, 37].
Неврологические и иммунологические сопряжения
Реализация иммунологического ответа на PAMP и DAMP вовлекает в процесс критические для гомеостаза регуляторные нейроэндокринные механизмы. Замкнутая цепь регуляции нейроэндокринного ответа, объединяющая нейроэндокринную, нервную и иммунную системы, состоит из двух компонентов — сенсорного афферентного и регуляторного эфферентного. Афферентная импульсация модулируется цитокинами и гормонами, которые проникают через гематоэнцефалический барьер в портальную систему гипофиза. Эфферентная часть нервной регуляции характеризуется наличием «воспалительного рефлекса» [38].
Липополисахариды, бактериальные токсины, провоспалительные цитокины и другие медиаторы системного воспалительного ответа взаимодействуют напрямую с сенсорными нейронами вегетативной нервной системы с реализацией афферентного потенциала действия, который «двигается» по сенсорным компонентам блуждающего нерва до ядра одиночного тракта в стволе мозга. Данные сигналы необходимы для формирования гипертермии и иных неврологических симптомов воспалительного ответа. «Воспалительный рефлекс» является ведущим в отношении выброса фактора некроза опухоли (ФНО) в ответ на ЛПС и иные медиаторы системного воспаления. Эфферентные сигналы из ствола мозга идут к ганглиям чревного сплетения, в которых находятся адренергические клетки селезеночных нервов. В окончаниях селезеночных нервов норэпинефрин, выбрасываемый аксонами, взаимодействует с подвидами Т-клеток, которые экспрессируют холинацетилтрансферазу, фермент, лимитирующий биосинтез ацетилхолина [39, 40]. Ацетилхолин, продуцируемый данными клетками, взаимодействует с никотин-ацетилхолиновыми рецепторами, которые экспрессируются в пульпе селезенки и макрофагах краевой зоны. Передача сигнала посредством ацетилхолиновых рецепторов подавляет внеядерную транслокацию NF- κB, стабилизирует митохондриальные мембраны и ингибирует активность инфламмасом, что в дальнейшем уменьшает выброс ФНО, ИЛ-1 и HMGB-1 (high mobility group box protein-1) [41].
Нервные импульсы также способны распространяться по симпатическим нервам из ствола головного мозга, что в окончательном итоге выражается в выбросе адренергических нейротрансмиттеров в тканях, взаимодействующих с клетками врожденного иммунитета и экспрессирующих α-и β-адренергические рецепторы, что вызывает модуляцию выброса цитокинов [42]. Еще одним эфферентным путем, который модулирует ответ цитокинов при СВР, является передача нервных импульсов по блуждающему нерву с регуляцией выброса допамина. Взаимодействия лигандов с допаминовыми рецепторами D1, экспрессирующихся на моноцитах и макрофагах, ослабляют воздействие ЛПС на выброс ФНО [43].
Следовательно, СВР инфекционного и неинфекционного генеза и тяжесть ответа (и, соответственно, тяжесть тканевого повреждения) зависят от исходного статуса вегетативной нервной системы, принимающей участие в регуляции врожденного иммунного ответа.
Митохондриальная дисфункция
Все компоненты патофизиологии критических состояний (нарушение доставки и потребления кислорода, ишемия и реперфузия, сепсис) вызывают клеточный стресс и нарушают физиологию митохондрий. Ингибирование окислительного фосфорилирования и синтеза аденозинтрифосфорной кислоты (АТФ) нарушает электролитный (прежде всего кальциевый) гомеостаз, что в итоге вызывает увеличение продукции СР. Кроме того, отмечается нарушение структуры митохондрий — деструкция и фрагментация [44]. Считается, что продукция СР является важнейшим фактором митохондриальной дисфункции. Активность митохондрии регулируется наличием субстратов и доступностью АДФ и иными формами посттрансляционной модификации [45]. Считается, что предотвращение продукции СР митохондриями снижает выброс провоспалительных цитокинов, что может быть основой для коррекции интенсивной терапии ПОН путем целенаправленного воздействия на дисфункцию митохондрий. Последствиями митохондриальной дисфункции являются истощение запасов АТФ, выброс цитохрома С и апоптоз-индуцирующего фактора, выброс СР и оксида азота, нарушение аутофагии [46, 47].
Критическое состояние (ишемия, гипоксия) ведет к нарушению сопряжения окислительного фосфорилирования и протонного градиента за счет открытия во внутренней мембране митохондрии митохондриальных пор проницаемости, снижению концентрации АТФ, к потере митохондриального матрикса и разрушению митохондрий, формированию микровезикул в эндоплазматическом ретикулуме и цитоплазме, выбросу лизосомальных ферментов, что ведет, в свою очередь,к гибели клеток [48].
Нарушение функции митохондрий сопровождается выбросом проапоптотических факторов (цитохром С) из межмембранного пространства с активацией каспаз. Считается, что ведущими в этом процессе являются активность СР и липопероксидация мембран. Вторым значимым для активации апоптоза белком считается апоптоз-индуцирующий фактор. Проапоптотическая активность потенцируется ишемией и реперфузией за счет увеличения содержания внутриклеточного кальция, что вызывает, в свою очередь, деполяризацию мембраны митохондрии [49–51].
Аутофагия — один из механизмов эндогенной цитопротекции, который позволяет клеткам «избавляться» от поврежденных органелл или молекул. Имеются формы неспецифической и целенаправленной аутофагии, которые реализуются путем формирования секвестрации содержимого цитозоля за счет образования фагофор с двойной мембраной, которые далее созревают в аутофагосомы с лизисом содержимого, при наличии рецепторного белка на поверхности того или иного клеточного компонента может реализовываться целенаправленная аутофагия [52].
Митохондриальная дисфункция и нарушение биогенеза митохондрий и аутофагии считаются одними из важнейших компонентов ПОН, включая острое повреждение почек, ОРДС и нарушение функции сердечно-сосудистой системы. Морфологические нарушения при ПОН характеризуются снижением массы митохондрий, фрагментацией митохондрий и потерей структуры крист [53].
В качестве вариантов патофизиологии вовлечения митохондрий в генез ПОН исследователи называют опосредованное СР нарушение структуры и функции клеток, выброс мит- ДНК в качестве DAMP и дисфункцию биогенеза и аутофагии, энергетическую недостаточность клетки [54].
Иммунная супрессия
Первичный иммунный ответ в виде контролируемой или неконтролируемой СВР вызывает выброс медиаторов, который, в свою очередь, объясняет клеточный и гуморальный ответы организма. Ответ включает активность нейтрофилов, фагоцитарную активность, повреждение эндотелиального барьера и синтез острофазовых реактантов, хемотаксис нейтрофилов в очаг воспаления и/или тканевого повреждения, активность системы свертывания. Первичный провоспалительный ответ в зависимости от выраженности базовой активности медиаторов СВР сменяется компенсаторным противовоспалительным ответом, однако абсолютной ясности в последовательности этих фаз до сих пор нет, т. к. анализ больших баз данных генетического материала показал одновременную ап- и даун-регуляцию транскрипции генов, отвечающих за ответ. Известно, что вторая фаза — фаза противовоспаления — инициирует индуцированную иммуносупрессию. Фазность СВР зависит от многих факторов: коморбидность, факторы собственно возбудителя при сепсисе или выраженности тканевого поражения при стерильной СВР и, конечно, генетики. Ряд авторов считает, что собственно фаза индуцированной иммуносупрессии является адаптивным ответом, что, вероятно, расширяет возможности в терапии путем ее целенаправленной индукции [55, 56].
Одним из компонентов индуцированной иммуносупрессии является апоптоз иммунных клеток. Первичными агентами апоптоза служат каспазы митохондриального происхождения, наряду с ядерными факторами транскрипции они активируют программу апоптоза клеток. Апоптоз активируется параллельно с провоспалительным пиком медиаторов СВР. Т-клетки адаптивного иммунитета CD-4 и CD-8 особенно подвержены апоптозу, что доказывается экспериментами in vitro, когда сыворотка пациентов с сепсисом, будучи добавлена к культуре лимфоцитов, вызывала апоптотическую гибель клеток [57].
ИЛ-10, как ведущий цитокин с противовоспалительными свойствами, обнаруживается у пациентов в большинстве представленных исследований с ПОН. ИЛ-10 продуцируется регуляторными Т-лимфоцитами (Treg) и Т2-лимфоцитами, подавляя ответ CD-8 Т-клеток, что, в свою очередь, снижает активность по выбросу и синтезу моноцитами медиаторов воспаления. Данный феномен подавления провоспалительной активности моноцитов и называется собственно иммунным параличом, характеризуется апоптозом лимфоцитов (лимфопения), увеличением числа Treg и снижением экспрессии молекул основного комплекса гистосовместимости (MHC [major histocompatibility complex] класса II — HLA-DR [human leukocyte antigens]).
Клеточное истощение — характерный иммунологический симптом иммуносупрессии, характеризуется экспрессией Т-лимфоцитами ингибиторных рецепторов (PD-1, CD-69, CD-25), что не позволяет клеткам продуцировать цитокины. Одним из объяснений может быть чрезмерная нагрузка внешними антигенами (вирусы, бактерии) [59].
Воспалительный метаболический комплекс
Нарушения метаболизма являются специфичными для ПОН и СВР. Имеются данные, что СВР вызывает метаболическую дисфункцию, специфичную для воспалительного ответа. Известно, что метаболиты сами по себе являются не только субстратами для метаболических процессов, но и субстратами для модификации иммунных клеток, служат медиаторами для передачи сигналов внутри и между клетками, регуляторами экспрессии генов, ингибиторами или активаторами ферментов [60]. Септическая кахексия — один из наиболее явных признаков проявления воспалительного метаболического комплекса. Кахексия — комплексный метаболический синдром, характеризирующийся потерей скелетной мышечной массы, что ассоциируется обычно с воспалением (вероятно персистирующим), инсулинорезистентностью и катаболизмом белков. Мышечная слабость как проявление индуцированной СВР кахексии считается ведущим условием персистирующей ПОН наряду с полинейропатией и полимиопатией критических состояний [61]. Системное воспаление посредством активации факторов транскрипции усиливает экспрессию генов убиквитина, атрогина-1, тем самым ускоряя разрушение белков [62]. Сопряжение воспаления и кахексии включает механизм выброса и активации супрессорных клеток миелоидного происхождения, клеток, которые одинаково активируются при септической и раковой кахексиях [63].
Нарушение функции желудочно – кишечного тракта и микробиом
В здоровом организме эпителий тонкой кишки имеет поверхность в 40 м2, полностью обновляется каждые 5 дней, обладает эффектом барьера между иммунными клетками кишки и 40 трлн микроорганизмов, постоянно живущих в просвете кишки. Впервые мнение о ЖКТ как «моторе» ПОН было высказано почти 40 лет назад. Данная теория обосновала компонент внутрибрюшной гипертензии, абдоминального компартмент-синдрома и роль в развитии нозокомиальных инфекционных осложнений [64]. Первично апробированная теория транслокации микрофлоры из просвета кишки за счет интестинальной гиперпроницаемости, что приводило бы к транслокации интактных бактерий в кровоток, на данный момент не является абсолютно подтвержденной [65]. Считается, что лимфа, оттекающая от ЖКТ, содержит всего лишь незначительное число бактерий, обычно минимальную концентрацию ЛПС и цитокинов, однако липидные фактор лимфы и микросомальный белок-переносчик триглицеридов способны активировать TLR в легких, тем самым потенцируя СВР и ПОН [66]. Интестинальная гиперпроницаемость является основой вклада ЖКТ в патогенез ПОН. С подобными процессами ассоциируется апоптоз эпителиоцитов ЖКТ, разрывы плотных контактов за счет разрушения окклюдинов и клаудинов, нарушение функции киназы легких цепей белка миозина, нарушение реологии слоя слизи и уменьшение его гидрофобности [67]. Микробиом — комплексная экологическая система, которую следует учесть в ходе рассмотрения патофизиологии ПОН.
Разрешение воспаления
Исторически сложилось, что воспалительный процесс является пассивным, предполагает устранение стимула воспаления, снижение вплоть до остановки продукции хемоаттрактантов, разведение градиентов хемокинов и предотвращение последующего рекрутмента лейкоцитов. Однако за последние десятилетия рядом авторов было показано, что разрешение (резолюция) воспаления — процесс активный, связанный с синтезом биологически активных медиаторов, которые являются ведущими в отношении возвращения воспалительного гомеостаза. Исследователями доказано, что разрешение воспаления (подавления воспалительной реакции) характеризуется прекращением хемотаксиса, снижением синтеза провоспалительных и вновь образуемых медиаторов, снижением активности макрофагов, нейтрофилов и лимфоцитов. Важную роль в разрешении воспаления играют так называемые медиаторы восстановления (proresolving mediators) [68].
Эндофенотип полиорганной недостаточности
Эндофенотип — вновь введeнный подкласс, соединяющий генетическую детерминацию и собственно симптомы заболевания. Исходно понятие было введено в психиатрии, однако с учетом того, что данная классификация была предложена для разделения многофакторной патологии (чем являются и критические состояния) на более простые и, что важно, измеряемые проявления, данная концепция может быть использована в ходе оценки патофизиологии и выбора терапии ПОН. Поскольку стерильное системное воспаление, ПОН предполагают довольно сложное взаимоотношение между эндотелиальными клетками, тромбоцитами, лейкоцитами, системы свертывания, воспалительными медиаторами, вариабельность подобных отношений клеток и систем поддержания гомеостаза на фоне исходного генотипа пациента, состояния микробиома, возраста, коморбидной патологии требует персонификации диагностики и — самое важное — персонификации терапии. Это может быть объяснено тем, что в ходе исследований и разработок теории «опасности» (danger theory) была установлена способность клеточных поверхностных паттерн-распознающих рецепторов отвечать на DAMP и PAMP одновременно, что делает СВР и ПОН синтезом ответа организма как на инфекционный, так и неинфекционный стимулы. Вероятно, что каждому пациенту будет соответствовать определенный эндофенотип критического состояния, пути активации сигнальных рецепторов, состояния макроорганизма (генетика, воз- раст, характер питания и т. д.).
Примером подобного могут служить три воспалительных фенотипа, связанных с педиатрическим сепсисом, что обусловлено взаимоотношениями между воспалением и свертыванием и объясняет определенный ответ на терапию: 1) ПОН, ассоциированная с иммунным параличом; 2) ПОН, ассоциированная с тромбоцитопенией; 3) последовательная ПОН [69]. Для каждого фенотипа были характерны иммунносупрессорные или гипериммунные проявления определенной выраженности (изменение ответа клеток ex vivo на эндотоксин или цитокины, нарушение экспрессии HLA-DR и/или лимфопения, изменение системного содержания цитокинов), которые характеризовались клиническими критериями (время с момента начала критического состояния, выраженность гемостазиологических расстройств) [69].
Проект MARS, инициированный авторским коллективом Scicluna et al., поставил перед собой цель определить биологические релевантные молекулы с позиции молекулярного эндофенотипа. Проспективное обсервационное исследование в нескольких центрах в Нидерландах и Великобритании пациентов с сепсисом включало полногеномный профиль экспрессии с последующей кластеризацией и машинным обучением. Первичной задачей служило выявление генетического эндотипа пациента, вторичной — сопоставление эндотипа и клинических исходов и особенностей пациентов. Были выделены 4 эндотипа (исследователи назвали их MARS 1–4, гены сигналинг-цитокинов, паттерн-распознающих рецепторов, клеточной пролиферации, клеточной мобильности, сигнальных путей лимфоцитов, клеточной смерти, метаболических путей, катаболизма белков и трансляционной модификации), каждый из которых ассоциировался с определенными особенностями течения клиники сепсиса и исходом, что позволило авторам предложить вариант «генетической» подписи, состоящей из профиля экспрессии 140 генов [70].
Заключение
СВР, ее дисрегуляция и формирование сложного ансамбля взаимоотношений аларминов, активности паттерн-распознающих рецепторов, включения в механизм системного эндотелиального повреждения, повреждения гликокаликса, митохондриального дистресс-синдрома, индуцированной иммуносупрессии, комплекса сопряжения метаболизма и воспаления и финального аккорда — активного процесса разрешения воспаления — делают практически сложной курацию пациентов с ПОН, объясняя как отсутствие понимания диагностических биохимических критериев органной недостаточности, так и провалы множества модулирующих стратегий, направленных на удаление/ ингибирование медиаторов СВР. Персонификация диагностических поисков и формирование эндофенотипа критического пациента как портрета со специфическими иммунологическими, генетическими и клиническими чертами — вероятный путь улучшения клинических исходов у пациентов с ПОН.
Источники финансирования. Работа выполнена в рамках гранта Президента РФ для государственной поддержки ведущей научной школы РФ НШ-2696.2018.7 за счет средств федерального бюджета «Прогнозирование и превентивная интенсивная терапия персистирующей полиорганной недостаточности».
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов. Е.В. Григорьев, Д.Л. Шукевич, Г.П. Плотников — концепция статьи, анализ литературных источников; А.Н. Кудрявцев, А.С. Радивилко — сбор источников литературы.
ORCID авторов