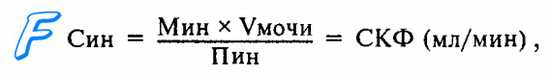Почечный клиренс что это
Основной количественной характеристикой процесса фильтрации является скорость клубочковой фильтрации (СКФ). СКФ —это объем ультрафильтрата или первичной мочи, образующийся в почках за единицу времени. Эта величина зависит от нескольких факторов: 1) от объема крови, точнее плазмы, проходящей через корковое вещество почек в единицу времени, т. е. почечного плазмотока, составляющего в среднем у здорового человека массой 70 кг около 600 мл/мин; 2) фильтрационного давления, обеспечивающего сам процесс фильтрации; 3) фильтрационной поверхности, которая равна примерно 2—3 % от общей поверхности капилляров клубочка (1,6 м2) и может изменяться при сокращении подоцитов и мезан-гиальных клеток; 4) массы действующих нефронов, т. е. числа клубочков, осуществляющих процесс фильтрации в определенный промежуток времени.
В физиологических условиях СКФ поддерживается на довольно постоянном уровне (несмотря на изменения системного артериального давления) за счет механизмов ауторегуляции.
К их числу относятся:
1) миогенная ауторегуляция тонуса приносящих артериол по принципу феномена Остроумова— Бейлиса;
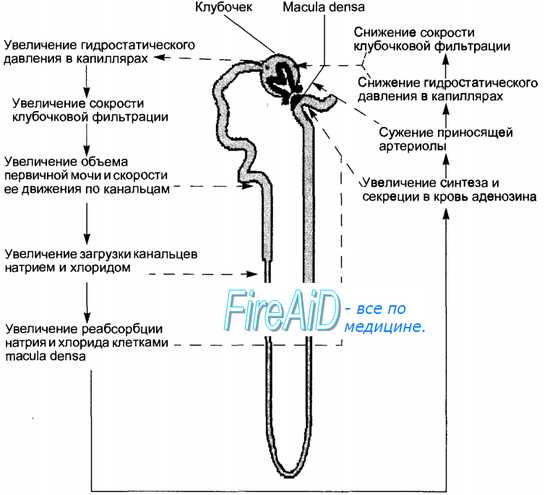
2) канальцево-клубочковая обратная связь, приводящая к изменению соотношения тонуса приносящих и выносящих артериол клубочка. Вовлечение в регуляцию механизма обратной связи обусловлено изменением доставки с фильтратом в область плотного пятна (macula densa) ионов натрия и хлора, что ведет к изменению продукции в ЮГА гуморальных регуляторов: аденозина (суживающий афферентные артериолы фактор), NO (дилатирующий артериолы фактор), ренина и ангиотензина-П, кининов и простагландинов (рис. 14.6);
3) изменения числа функционирующих нефронов. Первые два механизма поддерживают постоянство кровотока в клубочках и фильтрационное давление, гуморальные регуляторы могут менять площадь фильтрационной поверхности и функции подоцитов, третий механизм определяет конечный эффект ауторегуляции СКФ в органе, что в итоге обеспечивает постоянство объема образуемой первичной мочи.
СКФ определяют в результате сопоставления концентрации определенного вещества в плазме крови и моче. При этом используемое вещество должно выделяться вместе с водой только путем фильтрации и не всасываться в нефроне обратно в кровь. Таким условиям больше всего соответствует полисахарид фруктозы инулин. Исходя из концентрации инулина в плазме [Пин], и, определив его концентрацию в определенном объеме (V) конечной мочи [Мин], рассчитывают, какой объем первичной мочи соответствует найденной концентрации инулина. Насколько выросла концентрация инулина в конечной моче по сравнению с его концентрацией в плазме, во столько раз больше объем профильтровавшейся плазмы (т. е. первичной мочи) объема конечной мочи. Этот показатель получил название «клиренса» инулина или коэффициента очищения и рассчитывается по формуле:
показывающей, в каком объеме плазмы крови в единицу времени выделилось в мочу найденное количество инулина или какой объем плазмы «очистился» от инулина. По мере прохождения мочи по канальцам вода всасывается обратно в кровь и концентрация инулина растет, что и находят в конечной моче.
Поскольку инулин в организме отсутствует, для определения СКФ его необходимо капельно вводить в кровоток, создавая постоянную концентрацию. Это затрудняет исследование, поэтому в клинике обычно используют эндогенное вещество креатинин, концентрация которого в крови довольно стабильна.
Сравнивая клиренс инулина с клиренсом других веществ, определяют процессы, участвующие в выделении этих веществ с мочой. Если клиренс определенного вещества равен клиренсу инулина, значит вещество выделяется почками только путем фильтрации в клубочках. Если клиренс вещества больше клиренса инулина, следовательно, вещество выделяется не только за счет фильтрации, но и секрецией эпителием канальцев. Если клиренс вещества меньше, чем у инулина,— вещество после фильтрации реабсорбируется в канальцах.
В норме СКФ составляет у мужчин около 125 мл/мин, а у женщин — 110 мл/мин. В сутки образуется около 180 л первичной мочи, а за 25 мин фильтруется примерно 3 л плазмы крови, т. е. весь циркулирующий ее объем. За сутки этот объем плазмы крови фильтруется, т. е. очищается, примерно 60 раз. Так как объем конечной мочи составляет около 1,5 л в сутки, очевидно, что из объема первичной мочи за это время всасывается в канальцах обратно в кровь примерно 178,5 л жидкости.
Почечный клиренс что это
Определение клиренса эндогенного креатинина – исследование, применяемое для оценки уровня клубочковой фильтрации.
Скорость клубочковой фильтрации, СКФ.
Синонимы английские
Test of renal function, creatinine clearance test, Rehberg test.
Кинетический метод (метод Яффе).
Мкмоль/л (микромоль на литр), ммоль/сут. (миллимоль в сутки), мл (миллилитр), мл/мин. (миллилитр в минуту), % (проценты).
Какой биоматериал можно использовать для исследования?
Венозную кровь, суточную мочу.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Вся кровь человека сотни раз в день проходит через почки. Они пропускают жидкую часть крови через крохотные фильтры (нефроны), затем большая часть жидкости реабсорбируется обратно в кровь. Жидкие отходы, которые не реабсорбируются почками, удаляются из организма с мочой.
Креатинин (от греческого kreas – «плоть») – продукт распада креатинфосфата в мышечной ткани. Количество его в организме достаточно постоянно и зависит от мышечной массы человека. По химической структуре он является циклическим производным креатина.
Креатинин фильтруется из крови почками, и небольшое его количество активно выделяется с мочой. Канальцевая реабсорбция креатинина минимальна. Если фильтрующая способность почек недостаточна, то уровень креатинина в крови увеличивается. Зная уровни креатинина в моче и крови, можно вычислить клиренс креатинина, который отражает уровень клубочковой фильтрации. Клиренс креатинина (от англ. clearance – «очищение», т. е. очищение от креатинина, его выведение) – количество крови, которое почки могут очистить от креатинина за одну минуту. У здорового молодого человека он составляет около 125 мл в минуту, это значит, что его почки каждую минуту очищают от креатинина 125 мл крови.
Уровень клубочковой фильтрации – сумма уровней фильтрации во всех функционирующих нефронах. Этот показатель позволяет определить количество этих нефронов в почках. Он имеет важное клиническое значение, поскольку является основной характеристикой функции почек.
В случаях тяжелого нарушения функции почек клиренс креатинина повышается, поскольку при активной секреции креатинина выделяется его более крупная фракция.
Кетоновые кислоты, циметидин и триметоприм ограничивают канальцевую секрецию креатинина и снижают точность определения клубочковой фильтрации, особенно при тяжелой почечной недостаточности.
Клиренс креатинина можно определить двумя способами: измерением количества креатинина в крови человека и суточной моче. На практике чаще применяется анализ крови, поскольку это исследование удобнее для пациента.
Если у пациента низкий уровень клубочковой фильтрации, то лечащий врач разработает программу дополнительного обследования для выяснения причины этого патологического состояния. Основными причинами хронических болезней почек являются артериальная гипертония и сахарный диабет. Если они не выявлены, то необходимо дальнейшее обследование для выяснения причины заболевания почек.
Систематическое определение клиренса креатинина позволяет доктору следить за изменением функции почек пациента в динамике и корректировать медикаментозную терапию в зависимости от полученных данных.
Для чего используется исследование?
Когда назначается исследование?
Проба Реберга (клиренс эндогенного креатинина)
Определение клиренса эндогенного креатинина – исследование, применяемое для оценки уровня клубочковой фильтрации.
Скорость клубочковой фильтрации, СКФ.
Синонимы английские
Test of renal function, creatinine clearance test, Rehberg test.
Кинетический метод (метод Яффе).
Мкмоль/л (микромоль на литр), ммоль/сут. (миллимоль в сутки), мл (миллилитр), мл/мин. (миллилитр в минуту), % (проценты).
Какой биоматериал можно использовать для исследования?
Венозную кровь, суточную мочу.
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Вся кровь человека сотни раз в день проходит через почки. Они пропускают жидкую часть крови через крохотные фильтры (нефроны), затем большая часть жидкости реабсорбируется обратно в кровь. Жидкие отходы, которые не реабсорбируются почками, удаляются из организма с мочой.
Креатинин (от греческого kreas – «плоть») – продукт распада креатинфосфата в мышечной ткани. Количество его в организме достаточно постоянно и зависит от мышечной массы человека. По химической структуре он является циклическим производным креатина.
Креатинин фильтруется из крови почками, и небольшое его количество активно выделяется с мочой. Канальцевая реабсорбция креатинина минимальна. Если фильтрующая способность почек недостаточна, то уровень креатинина в крови увеличивается. Зная уровни креатинина в моче и крови, можно вычислить клиренс креатинина, который отражает уровень клубочковой фильтрации. Клиренс креатинина (от англ. clearance – «очищение», т. е. очищение от креатинина, его выведение) – количество крови, которое почки могут очистить от креатинина за одну минуту. У здорового молодого человека он составляет около 125 мл в минуту, это значит, что его почки каждую минуту очищают от креатинина 125 мл крови.
Уровень клубочковой фильтрации – сумма уровней фильтрации во всех функционирующих нефронах. Этот показатель позволяет определить количество этих нефронов в почках. Он имеет важное клиническое значение, поскольку является основной характеристикой функции почек.
В случаях тяжелого нарушения функции почек клиренс креатинина повышается, поскольку при активной секреции креатинина выделяется его более крупная фракция.
Кетоновые кислоты, циметидин и триметоприм ограничивают канальцевую секрецию креатинина и снижают точность определения клубочковой фильтрации, особенно при тяжелой почечной недостаточности.
Клиренс креатинина можно определить двумя способами: измерением количества креатинина в крови человека и суточной моче. На практике чаще применяется анализ крови, поскольку это исследование удобнее для пациента.
Если у пациента низкий уровень клубочковой фильтрации, то лечащий врач разработает программу дополнительного обследования для выяснения причины этого патологического состояния. Основными причинами хронических болезней почек являются артериальная гипертония и сахарный диабет. Если они не выявлены, то необходимо дальнейшее обследование для выяснения причины заболевания почек.
Систематическое определение клиренса креатинина позволяет доктору следить за изменением функции почек пациента в динамике и корректировать медикаментозную терапию в зависимости от полученных данных.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Причины пониженного клиренса креатинина:
Причины повышенного клиренса креатинина:
Что может влиять на результат?
Кто назначает исследование?
Врач общей практики, терапевт, нефролог, уролог.
Литература
Подписка на новости
Оставьте ваш E-mail и получайте новости, а также эксклюзивные предложения от лаборатории KDLmed
Почечный клиренс что это
а) Использование методики клиренса для количественной оценки функции почки. Оценка интенсивности, с которой плазма «очищается» от различных веществ, предоставляет хорошую возможность количественно определить эффективность их выделения почками (просим вас изучить таблицу ниже).
Почечным клиренсом данного вещества называют объем плазмы крови, который с помощью почек освобождается от вещества за единицу времени. Это определение является отчасти отвлеченным, поскольку объема плазмы, который полностью освобождается от данного вещества, в отдельности не существует. Тем не менее, почечный клиренс позволяет исследовать выделительную функцию почек и, как рассмотрим далее, может использоваться для количественного определения почечного кровотока, а также для оценки основных функций почек, таких как клубочковая фильтрация, канальцевая реабсорбция и канальцевая секреция.
Проиллюстрируем принцип клиренса на следующем примере: если в каждом миллилитре плазмы, протекающей через почки, содержится 1 мг вещества и если каждую минуту 1 мг этого вещества выделяется с конечной мочой, «очищение» плазмы в данном случае составит 1 мл/мин. Таким образом, клиренс (коэффициент «очищения») имеет отношение к объему плазмы, который должен пройти через почки и доставить необходимое количество вещества для выделения его с мочой в единицу времени. Математически клиренс выражают формулой:
где Св — клиренс вещества; Рв — концентрация вещества в плазме; Uв — концентрация вещества в моче; V — объем мочи.
Преобразовав уравнение, клиренс может представить как: Св = Uв х V / Pв.
Таким образом, клиренс вещества равен интенсивности выделения данного вещества с мочой (Uв x V), деленного на концентрацию его в плазме.
б) Клиренс инулина можно использовать для оценки СКФ. Если вещество свободно, как и вода, фильтруется в клубочке, не реабсорбируется и не секретируется почечными канальцами, тогда интенсивность его выделения с мочой (Uв x V) будет равна скорости фильтрации вещества в клубочках (СКФ х Рв). Таким образом: СКФ х Рв = Uв х V.
СКФ может быть вычислена путем определения клиренса вещества: СКФ = (Uв x V) / Pв = Св.
Веществом, удовлетворяющим перечисленным критериям, является инулин — полисахарид с молекулярной массой около 5200. Инулин в организме не синтезируется, он присутствует в корнях определенных растений, для изучения СКФ его следует вводить внутривенно.
На рисунке выше приведены данные по содержанию инулина в различных сегментах нефрона. В этом примере концентрация инулина в плазме — 1 мг/мл, в моче — 125 мг/мл, интенсивность образования мочи — 1 мл/мин. Следовательно, за 1 мин в мочу попадают 125 мг инулина. Затем подсчитывают клиренс инулина через отношение его содержания в моче к концентрации в плазме, что составит 125 мл/мин. Следовательно, количество плазмы, проходящей через почечные сосуды и профильтрованной в клубочках для доставки такого количества инулина в конечную мочу, должно составить 125 мл.
Инулин — не единственное вещество, которое может применяться для определения СКФ. Другие соединения, используемые в клинике для оценки СКФ, включают радиоактивный иоталамат и креатинин.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Клиренс лекарственных средств
Клиренс лекарственных средств [ править | править код ]
Клиренс — важнейший фармакокинетический параметр, позволяющий подобрать длительное лечение. Чтобы обеспечить нужный терапевтический эффект и свести к минимуму риск побочного действия, средняя сывороточная концентрация препарата в стационарном состоянии должна находиться в пределах терапевтического диапазона. Если биодоступность равна 100%, в стационарном состоянии скорость элиминации препарата равна скорости его поступления.
Скорость поступления = С1 х Ссредн, (1.1)
где скорость поступления — количество введенного препарата в единицу времени, С1 — суммарный клиренс, а Ссредн — средняя сывороточная концентрация препарата в стационарном состоянии. Если известна требуемая средняя сывороточная концентрация, скорость поступления можно рассчитать по клиренсу.
Важнейшая с клинической точки зрения особенность клиренса — он, как правило, не зависит от концентрации препарата. Дело в том, что системы, отвечающие за элиминацию большинства лекарственных средств (ферментные, транспортные), обычно не насыщаются, и абсолютная скорость элиминации линейно зависит от сывороточной концентрации препарата. Иными словами, элиминация подчиняется кинетике первого порядка — доля препарата, удаляемая за единицу времени, постоянна. Если же системы элиминации насыщаются, постоянна не доля, а количество препарата, удаляемое за единицу времени. При этом элиминация подчиняется кинетике нулевого порядка, а клиренс зависит от сывороточной концентрации препарата:
где Кm — концентрация препарата, при которой скорость элиминации составляет половину от максимальной, а Vm — максимальная скорость элиминации.
Это уравнение аналогично уравнению Михаэлиса— Ментен, выражающему соотношение между скоростью ферментативной реакции и концентрацией субстрата. Подобрать схему лечения препаратами, элиминация которых не подчиняется кинетике первого порядка (то есть клиренс зависит от сывороточной концентрации), гораздо труднее (см. ниже).
Понятие клиренса лекарственного средства аналогично понятию клиренса в физиологии почек. Так, клиренс креатинина равен отношению скорости экскреции креатинина с мочой к концентрации креатинина в плазме. В общем случае клиренс лекарственного средства равен отношению скорости элиминации вещества всеми органами к концентрации препарата в биологической жидкости.
Cl=Скорость элиминации/ С (1.3)
Если клиренс постоянен, скорость элиминации прямо пропорциональна концентрации лекарственного средства. Важно отметить, что клиренс отражает не количество элиминировавшегося препарата, а объем биологической жидкости (плазма или цельная кровь), полностью очищающийся отданного вещества за единицу времени. Можно рассчитать клиренс для плазмы или цельной крови, а также клиренс свободного препарата.
Элиминация лекарственных средств осуществляется почками, печенью и другими органами. Рассчитав клиренс для каждого органа как отношение скорости элиминации данным органом к концентрации препарата (например, в плазме) и просуммировав клиренсы для всех органов, получим суммарный клиренс.
Clпоч + Сlпеч + Сlпр = Сl(1.4)
где Сlпоч — почечный клиренс, Сlпеч — печеночный клиренс, Сlпр — клиренс для прочих органов (лекарственные средства могут метаболизироваться в других органах, выводиться с калом, потом, слюной).
В стационарном состоянии суммарный клиренс можно определить с помощью уравнения 1.1. При однократном введении препарата, биодоступность которого равна 100%, а элиминация подчиняется кинетике первого порядка, суммарный клиренс можно рассчитать на основании закона сохранения массы и интегрирования уравнения 1.3 по времени.
где ПФК — площадь под фармакокинетической кривой, описывающей зависимость сывороточной концентрации препарата от времени.
Примеры. Клиренс цефалексина (для плазмы) составляет 4,3 мл/мин/кг (Приложение II). У больного весом 70 кг клиренс цефалексина составит 300 мл/мин. Поскольку 90% препарата выводится с мочой в неизмененном виде, можно сказать, что за 1 мин почки очищают от цефалексина 270 мл крови. Если функция почек не меняется, клиренс постоянен, а скорость элиминации цефалексина зависит от сывороточной концентрации препарата (уравнение 1.3). Клиренс пропранолола (для цельной крови) составляет 16 мл/мин/кг (1120 мл/мин при весе 70 кг). Препарат элиминируется преимущественно печенью, то есть за 1 мин печень очищает от пропранолола 1120 мл крови. Клиренс не всегда соответствует плазмотоку (или кровотоку) через орган, отвечающий за элиминацию. Если препарат связывается с эритроцитами, скорость его доставки в этот орган существенно выше, чем можно предположить исходя из концентрации препарата в плазме. В стационарном состоянии соотношение клиренса для плазмы и цельной крови выглядит следующим образом:
где Сlп — клиренс для плазмы, Сlк — клиренс для цельной крови, Сп — концентрация препарата в плазме, Ск — концентрация препарата в цельной крови, Сэ — концентрация препарата в эритроцитах, Ht — гематокрит.
Таким образом, клиренс для цельной крови равен частному от деления клиренса для плазмы на отношение концентраций препарата в цельной крови и плазме. Это соотношение, в свою очередь, можно рассчитать, зная гематокрит (в норме около 0,45) и соотношение концентраций препарата в эритроцитах и плазме. В большинстве случаев клиренс для цельной крови меньше печеночного кровотока (если препарат элиминируется печенью) или суммы печеночного и почечного кровотока (если препарат элиминируется печенью и почками). Клиренс такролимуса, который метаболизируется преимущественно в печени, для плазмы составляет 2 л/мин; иными словами, он более чем вдвое превышает печеночный плазмоток и даже превосходит печеночный кровоток (1,5 л/мин). Однако поскольку такролимус в значительной степени связывается с эритроцитами, его клиренс для цельной крови равен всего 63 мл/мин. Следовательно, на самом деле такролимус удаляется из крови гораздо медленнее. Иногда рассчитанный для цельной крови клиренс препаратов, которые элиминируются путем метаболизма, превышает печеночный кровоток. Это означает, что препарат метаболизируется и вне печени. Так, клиренс эсмолола для цельной крови (11,9 л/мин) превышает сердечный выброс, поскольку препарат интенсивно метаболизируется эритроцитарными эстеразами.
Понятие клиренса очень важно и для оценки влияния различных физиологических и патологических состояний на элиминацию лекарственных средств отдельными органами. Скорость доставки препарата в орган равна произведению кровотока через этот орган (Q) на концентрацию препарата в артериальной крови (Са), а скорость удаления из органа — произведению кровотока через этот орган на концентрацию препарата в венозной крови (Q,). Разница между этими скоростями в стационарном состоянии и есть скорость элиминации данным органом:
Скорость элиминации = QxCa — QxCv = = Q х (Са — Cv). (1.7)
Разделив обе части этого уравнения на Са, получим клиренс препарата для данного органа (Сlорг).
Clopr = Q X ((Са-Cv)/Ca) = Q x E
Печеночный клиренс [ править | править код ]
В действительности ситуация может оказаться сложнее. Уравнение 1.8 не учитывает ни связывание лекарственных средств с компонентами крови и тканей, ни способность печени элиминировать лекарственные средства (вне зависимости от печеночного кровотока) — так называемый внутренний печеночный клиренс. Для лекарственных средств, элиминация которых подчиняется кинетике первого порядка, внутренний клиренс характеризует отношение констант, входящих в уравнение 1.2, Vm / Кm. В нескольких моделях, описывающих печеночную элиминацию, уравнение 1.8 было расширено с учетом связывания лекарственного средства с белками плазмы и внутреннего печеночного клиренса (Morgan and Smallwood, 1990). Согласно этим моделям, если способность печени метаболизировать препарат велика по сравнению со скоростью его доставки с кровью, клиренс примерно равен печеночному кровотоку. В противном случае клиренс зависит от концентрации свободного препарата в крови и внутреннего печеночного клиренса. С помощью таких моделей можно объяснить некоторые противоречивые результаты экспериментальных исследований на животных. Так, индукция микросомальных ферментов или заболевания печени могут приводить к изменению скорости метаболизма некоторых лекарственных средств in vitro, но суммарный клиренс in vivo при этом может не меняться. Это объясняется тем, что индукция микросомальных ферментов и заболевания печени приводят к изменению внутреннего печеночного клиренса, а клиренс препаратов с высоким коэффициентом экстракции ограничен только печеночным кровотоком и практически не зависит от внутреннего клиренса. Кроме того, при высоком коэффициенте экстракции на клиренс не влияет и связывание препарата с белками плазмы, которое может меняться, например, при различных патологических состояниях или конкуренции за участки связывания. Клиренс лекарственных средств с низким коэффициентом экстракции, напротив, чувствителен к изменению внутреннего печеночного клиренса и связывания с белками плазмы, но почти не зависит от печеночного кровотока (Wilkinson and Shand, 1975).
Почечный клиренс [ править | править код ]
Этот показатель отражает экскрецию лекарственного средства с мочой и позволяет оценить изменение фармакокинетики препарата при заболеваниях почек. Лекарственные средства выводятся почками путем клубочковой фильтрации, канальцевой секреции и канальцевой реабсорбции. Скорость фильтрации препарата зависит от СКФ и концентрации свободного препарата в плазме (препарат, связанный с белками плазмы, не проходит через клубочковый фильтр). Скорость канальцевой секреции определяется способностью транспортных систем канальцев секретировать препарат. Эта способность, в свою очередь, зависит от связывания препарата с белками плазмы, степени насыщения транспортных систем и скорости доставки препарата к канальцам. И наконец, лекарственное средство может реабсорбироваться из канальцев обратно в кровь. На почечный клиренс влияют те же факторы, что и на печеночный клиренс — связывание препарата с белками плазмы, почечный кровоток и внутренний почечный клиренс (последний, в свою очередь, зависит от числа функционирующих нефронов).